Clear Sky Science · pl
Podejście in vitro do symulacji rozbieżnej O-glikozylacji Golgiego MUC1 związanego z nowotworem w porównaniu z MUC1 normalnym
Dlaczego „cukrowe okrywy” na białkach mają znaczenie w raku
Nasze komórki nieustannie dekorują swoje białka krótkimi łańcuchami cukrów, tworząc rodzaj molekularnej „okrywy”, która wpływa na wzrost komórek, komunikację i interakcje z układem odpornościowym. W wielu nowotworach to pokrycie cukrowe zmienia się w charakterystyczny sposób, zwłaszcza na białku MUC1, obfitym na komórkach nabłonkowych i powierzchniach guzów. W tym badaniu zbudowano model laboratoryjny naśladujący sposób dodawania tych cukrów, co pozwala naukowcom szczegółowo zobaczyć, jak normalne wzorce glikozylacji MUC1 rozgałęziają się w formy związane z nowotworem, które sprzyjają wzrostowi nowotworów i unikaniu wykrycia.
Budowanie sterowalnego modelu „cukrowej fabryki” komórki
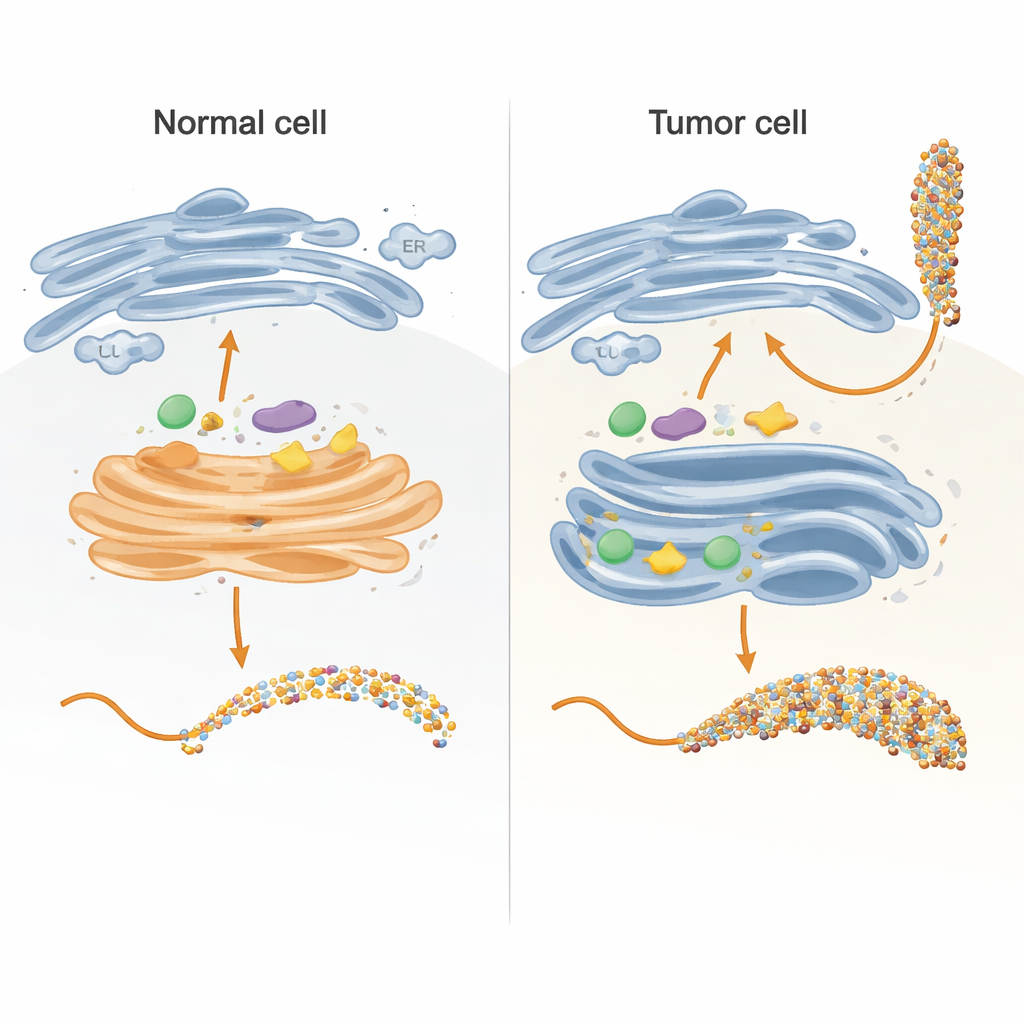
W komórkach łańcuchy cukrowe powstają głównie w dwóch przedziałach: siateczce śródplazmatycznej (ER) i aparacie Golgiego, które działają jak wieloetapowa linia montażowa. Autorzy odtworzyli kluczowe elementy tej linii w probówce, używając starannie zaprojektowanej wersji białka MUC1 związanej z nośnikiem. Wyeksprymowali ten białkowy fuzjat w bakteriach, oczyszczono go, a następnie wystawiono na działanie ludzkich enzymów, które normalnie dodają cukry w komórkach. Projektując fragment MUC1 tak, aby każde z pięciu miejsc przyłączania cukru występowało tylko raz i w naturalnej sekwencji, mogli śledzić dokładnie, które miejsce modyfikował dany enzym i w jakiej kolejności, używając czułych pomiarów kinetycznych oraz spektrometrii mas.
Jak rozdzielają się ścieżki normalne i nowotworowe
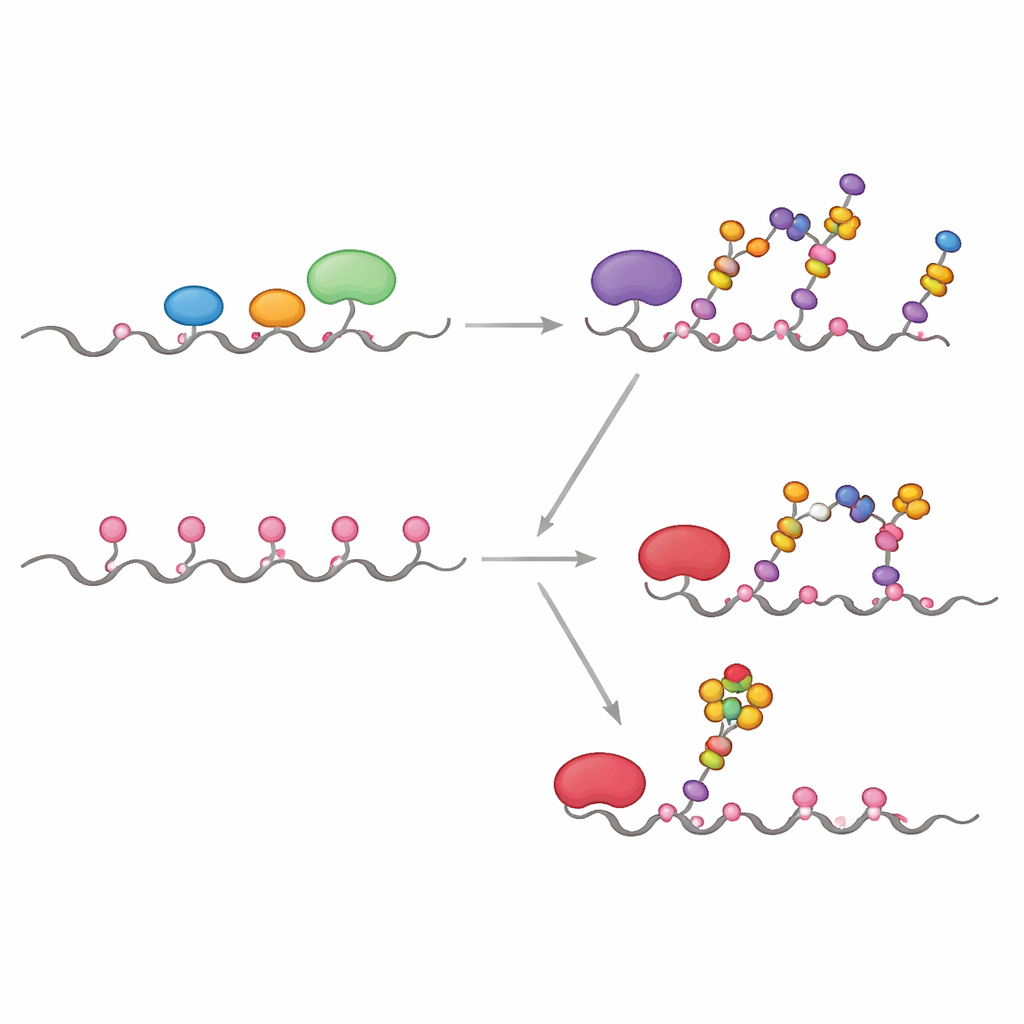
W zdrowych komórkach pierwsze enzymy w tym procesie, zwane GALNT, zwykle znajdują się we wczesnej części Golgiego i działają obok innych enzymów wydłużających lub zamykających początkowe jednostki cukrowe. Zespół pokazał, że w tych „współlokalizowanych” warunkach GALNT modyfikują głównie podzbiór miejsc na MUC1 — autorzy nazywają je miejscami bezpośrednimi — podczas gdy dwa wolniejsze miejsca zależne od lektyn pozostają w dużej mierze niezmienione. Gdy tylko pierwszy cukier (GalNAc) zostanie dodany w miejscach bezpośrednich, enzymy dalszego rzutu, takie jak C1GALT1, szybko je wydłużają, albo ST6GALNAC1 i inne sialylotransferazy dodają kwas sjalowy, skutecznie blokując mechanizm lektynowy GALNT przed masowym wypełnieniem pozostałych miejsc. W rezultacie powstaje skromniejszy, kontrolowany wzór glikozylacji typowy dla nabłonkowego MUC1.
Symulowanie nowotworowego przemeblowania enzymów
W wielu guzach obserwuje się wyraźne przemieszczanie enzymów GALNT z Golgiego z powrotem do ER, wraz ze zmianami w poziomach kilku enzymów glikozylacyjnych. Badacze naśladowali to, pozwalając GALNT działać najpierw dłużej i izolowanie, zanim wprowadzili enzymy dalszego rzutu. W takich warunkach początkowe cukry stopniowo rozprzestrzeniały się z łatwych, bezpośrednich miejsc na wolniejsze, zależne od lektyn miejsca, aż ostatecznie zajęły wszystkie pięć pozycji na MUC1. Dopiero po tym etapie nasycenia dodawano enzymy wydłużające i zamykające. Taki scenariusz przypominający ER dał silnie „ubrany” MUC1 przypominający MUC1 związany z nowotworem, bogaty w tak zwane antygeny Tn i sialyl-Tn (sTn), które korelują z progresją raka, ucieczką przed układem odpornościowym i przerzutami.
Skupienie się na jednym „gorącym” miejscu
Jedną z klinicznie najistotniejszych cech nowotworowego MUC1 jest obecność sialyl-Tn, krótkiego cukru zakończonego kwasem sjalowym, przyłączonego bezpośrednio do GalNAc. Aby zobaczyć dokładnie, gdzie pojawia się ten modyfikator na MUC1, zespół połączył eksperymenty kinetyczne, dokowanie komputerowe i hybrydowe symulacje kwantowo-klasyczne. Stwierdzili, że enzym ST6GALNAC1 jest jednoznacznie odpowiedzialny za dodanie kwasu sjalowego w wiązaniu α2-6 do antygenów Tn i T na MUC1, i że wykazuje silne preferencje wobec jednego konkretnego resztu treoniny w regionie PDTR (oznaczonego w artykule jako T13), gdy wszystkie pięć miejsc nosi już GalNAc. Modele strukturalne i symulacje ścieżki reakcyjnej pokazują, że w tym miejscu cukier i aminokwasy katalityczne ustawiają się w geometrii, która obniża barierę energetyczną reakcji bardziej niż w sąsiednich miejscach, wyjaśniając, dlaczego sTn pojawia się tam najwcześniej i najsilniej.
Co to oznacza dla zrozumienia i celowania w raka
Razem te eksperymenty i symulacje pokazują, że różnica między normalnym a nowotworowo związanym MUC1 jest napędzana mniej przez to, które enzymy są obecne, a bardziej przez to, gdzie się znajdują w komórce i jak długo mogą działać zanim zostaną przerwane. Gdy GALNT są ograniczone do Golgiego z konkurującymi enzymami, ozdabiają głównie tylko szybkie miejsca, dając typowe cukry rdzeniowe 1 i ograniczoną sialylację. Kiedy są przemieszczone do ER, jak w wielu nowotworach, zyskują czas, by wypełnić zarówno szybkie, jak i wolne miejsca, tworząc gęsto pokryty GalNAc MUC1, który staje się wyjątkowo dobrym substratem dla ST6GALNAC1 w miejscu T13, co gwałtownie zwiększa poziom sTn. To systemowe spojrzenie łączy lokalizację enzymów, czas reakcji i geometrię molekularną w jedno ramy wyjaśniające, jak pozornie subtelna zmiana w „cukrowej fabryce” komórki może wygenerować silne markery specyficzne dla nowotworu i sugeruje bardziej precyzyjne cele dla diagnostyki, szczepionek oraz terapii przeciwnowotworowych ukierunkowanych na glikany.
Cytowanie: Nashed, A., Dilsook, K., Senapathi, T. et al. An in vitro approach for simulating divergent Golgi O-glycosylation of tumor-associated MUC1 from normal MUC1. Nat Commun 17, 3619 (2026). https://doi.org/10.1038/s41467-026-72151-y
Słowa kluczowe: glikozylacja białek, MUC1, markerów nowotworowych, aparatu Golgiego, antygen sialyl-Tn