Clear Sky Science · nl
Een in vitro-benadering om divergente Golgi O-glycosylering van tumor-geassocieerde MUC1 te simuleren ten opzichte van normale MUC1
Waarom suikerlagen op eiwitten van belang zijn bij kanker
Onze cellen versieren hun eiwitten voortdurend met korte ketens suikers, waardoor als het ware een moleculaire "jas" ontstaat die bepaalt hoe cellen groeien, communiceren en omgaan met het immuunsysteem. Bij veel vormen van kanker veranderen deze suikerpatronen op kenmerkende manieren, vooral op een eiwit dat MUC1 heet en overvloedig aanwezig is op epitheelcellen en tumoren. Deze studie bouwt een laboratoriummodel dat nabootst hoe cellen deze suikers toevoegen, waardoor onderzoekers in detail kunnen zien hoe normale suikerpatronen op MUC1 uiteenlopen naar tumor-geassocieerde vormen die tumoren helpen groeien en detectie te ontwijken.
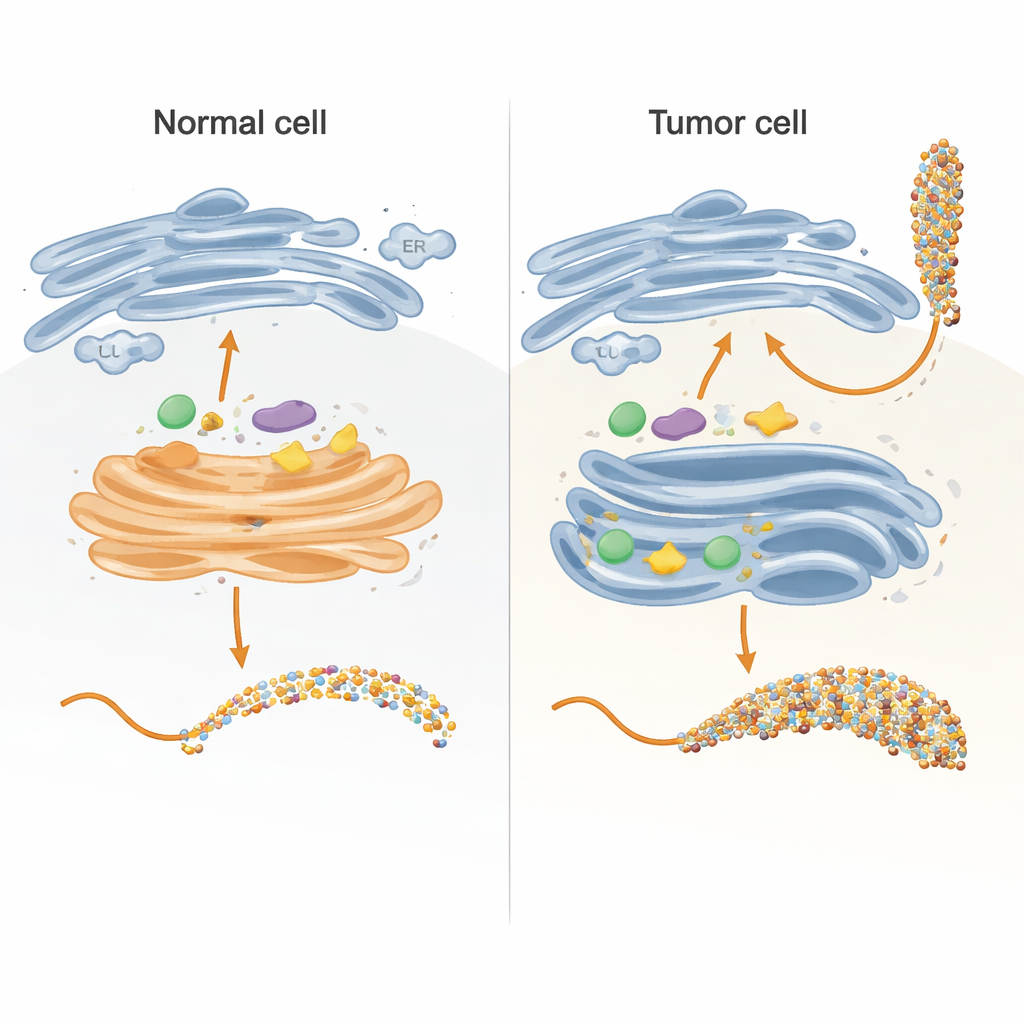
Een beheersbaar model van de suikermakerij in de cel bouwen
In cellen worden suikerketens voornamelijk opgebouwd in twee compartimenten: het endoplasmatisch reticulum (ER) en het Golgi-apparaat, die als een meertraps assemblagelijn functioneren. De auteurs reconstrueerden essentiële onderdelen van deze lijn in een reageerbuis met een zorgvuldig ontworpen versie van het MUC1-eiwit gekoppeld aan een draagtag. Ze brachten dit fusie-eiwit tot expressie in bacteriën, zuiverden het en stelden het vervolgens bloot aan menselijke enzymen die normaal gesproken suikers in cellen toevoegen. Door het MUC1-fragment zo te ontwerpen dat elk van de vijf suikeraanhangplaatsen slechts één keer voorkomt en in een natuurlijke volgorde, konden ze precies volgen welke plaats elk enzym wijzigde, en in welke volgorde, met behulp van gevoelige kinetische metingen en massaspectrometrie.
Hoe normale en tumorpaden uit elkaar lopen
In gezonde cellen bevinden de eerste enzymen in het proces, de GALNTs, zich grotendeels in een vroeg deel van het Golgi en werken ze naast andere enzymen die de initiële suikerunits verlengen of afsluiten. Het team toonde aan dat onder deze "gekolokaliseerde" omstandigheden GALNTs vooral een subset van plaatsen op MUC1 modificeren — wat de auteurs directe plaatsen noemen — terwijl twee langzamere, lectine-afhankelijke plaatsen grotendeels ongemoeid blijven. Zodra de eerste suiker (GalNAc) op de directe plaatsen is toegevoegd, verlengen downstream-enzymen zoals C1GALT1 deze snel, of voegen ST6GALNAC1 en andere sialyltransferasen siaalzuur toe, waarmee GALNTs effectief worden verhinderd hun lectine-gebaseerde mechanisme te gebruiken om alle overgebleven plaatsen dicht te vullen. Het resultaat is een meer bescheiden, gecontroleerd suikerpatroon dat typisch is voor normale epitheliale MUC1.
Het kankerachtige herschikken van enzymen nabootsen
Veel tumoren vertonen een opvallende verplaatsing van GALNT-enzymen van het Golgi terug naar het ER, samen met veranderingen in de niveaus van verschillende glycosyleringsenzymen. De onderzoekers imiteerden dit door GALNTs eerst geïsoleerd en langer te laten werken voordat ze de downstream-enzymen introduceerden. Onder deze omstandigheden verspreidden de initiële suikers zich geleidelijk van de gemakkelijk te bereiken directe plaatsen naar de langzamere lectine-afhankelijke plaatsen, en bezetten uiteindelijk alle vijf posities op MUC1. Pas na deze verzadigingsstap werden verleng- en afsluitenzymen toegevoegd. Dit ER-achtige scenario leverde een sterk versierde MUC1 op die leek op tumor-geassocieerde MUC1, rijk aan de zogenaamde Tn- en sialyl-Tn (sTn)-antigenen die geassocieerd zijn met kankerprogressie, immuunontwijking en metastase.
Inzoomen op één kritieke plaats
Een van de klinisch meest relevante kenmerken van tumor-MUC1 is de aanwezigheid van sialyl-Tn, een korte, met siaalzuur afgesloten suiker die direct aan GalNAc is gekoppeld. Om precies te zien waar dit op MUC1 verschijnt, combineerde het team kinetische experimenten, computerdocking en hybride kwantum/klassieke simulaties. Ze vonden dat het enzym ST6GALNAC1 uniek verantwoordelijk is voor het toevoegen van siaalzuur in een α2-6-binding aan Tn- en T-antigenen op MUC1, en dat het een sterke voorkeur toont voor één specifieke threonineplaats in het PDTR-gebied (in het artikel T13 genoemd) zodra alle vijf plaatsen GalNAc dragen. Structurele modellen en reactiepadsimulaties tonen aan dat op deze plaats de suiker en de katalytische aminozuren in een geometrie liggen die de energiebarrière voor de reactie sterker verlaagt dan op aangrenzende plaatsen, wat verklaart waarom sTn daar eerst en het meest prominent verschijnt.
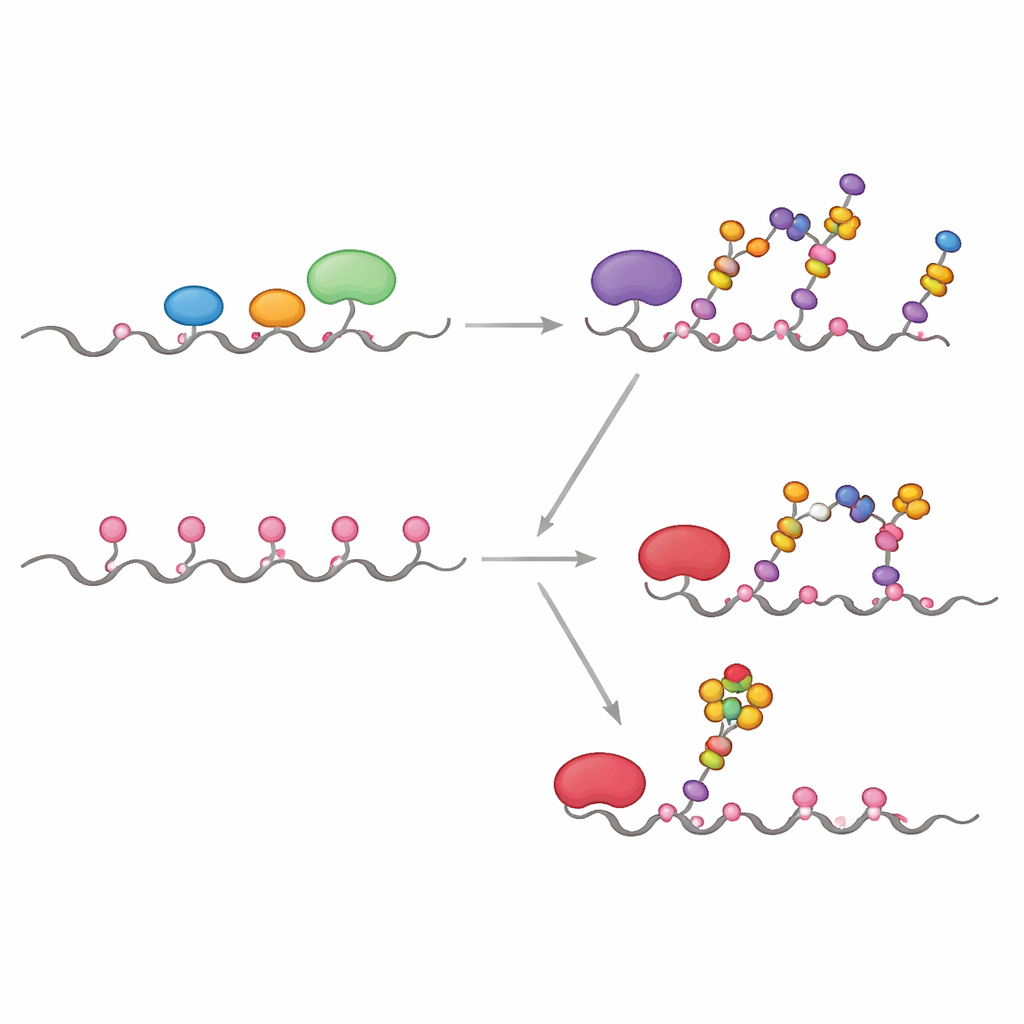
Wat dit betekent voor het begrijpen en gericht aanpakken van kanker
Gezamenlijk tonen deze experimenten en simulaties aan dat het verschil tussen normale en tumor-geassocieerde MUC1 minder wordt bepaald door welke enzymen aanwezig zijn en meer door waar ze zich in de cel bevinden en hoe lang ze kunnen werken voordat ze worden onderbroken. Wanneer GALNTs in het Golgi blijven met concurrerende enzymen, versieren ze voornamelijk alleen de snelle plaatsen, wat leidt tot typisch core-1-suikers en beperkte sialisering. Wanneer ze naar het ER verplaatsen, zoals in veel kankers, krijgen ze de tijd om zowel snelle als trage plaatsen te vullen, waardoor een dicht met GalNAc bedekte MUC1 ontstaat die een bijzonder goed substraat wordt voor ST6GALNAC1 op de T13-plaats, wat de sTn-niveaus scherp verhoogt. Dit systeemniveauperspectief verbindt enzymlokalisatie, reactietiming en moleculaire geometrie in één raamwerk dat helpt verklaren hoe een ogenschijnlijk subtiele verandering in de suikermakerij van de cel krachtige tumor-specifieke markers kan genereren en suggereert nauwkeuriger doelen voor diagnostiek, vaccins en op glycans gerichte kankertherapieën.
Bronvermelding: Nashed, A., Dilsook, K., Senapathi, T. et al. An in vitro approach for simulating divergent Golgi O-glycosylation of tumor-associated MUC1 from normal MUC1. Nat Commun 17, 3619 (2026). https://doi.org/10.1038/s41467-026-72151-y
Trefwoorden: proteïneglycosylering, MUC1, kankerbiomarkers, Golgi-apparaat, sialyl-Tn antigeen