Clear Sky Science · ja
正常なMUC1から腫瘍関連MUC1への分岐するゴルジO-グリコシル化を模擬するin vitroアプローチ
がんでタンパク質の糖鎧が重要な理由
細胞は常にタンパク質に短い糖鎖を付け、分子レベルの「コート」を形成して細胞の増殖、情報伝達、免疫系との相互作用に影響を与えています。多くのがんではこの糖化が特徴的に変化し、とくに上皮細胞や腫瘍表面に豊富に存在するMUC1というタンパク質で顕著です。本研究は、細胞がこれらの糖を付加する過程を模倣する実験室モデルを構築し、正常なMUC1の糖パターンがどのように腫瘍関連の様式へと分岐するかを詳しく観察できるようにします。
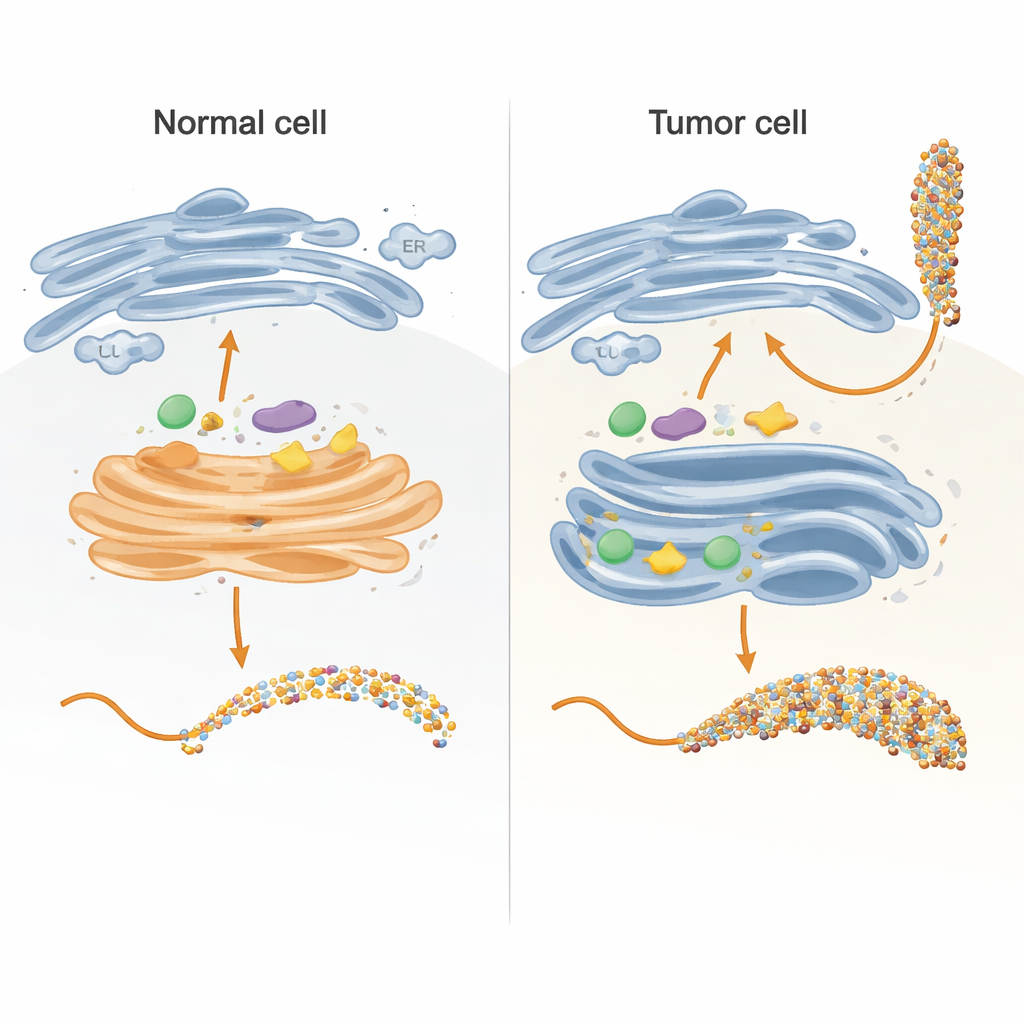
細胞の糖工場を制御可能なモデルとして再現する
細胞内では糖鎖は主に小胞体(ER)とゴルジ体という2つの区画で作られ、段階的な組み立てラインのように働きます。著者らは、このラインの主要部分を試験管内で再現するため、MUC1の慎重に設計した断片をキャリアタグに結合した形で用いました。この融合タンパク質を細菌で発現・精製し、細胞内で通常糖を付加するヒト酵素に暴露させました。MUC1断片は5つの糖付加部位がそれぞれ一度だけ自然な配列で現れるように設計されているため、感度の高い動力学測定と質量分析を用いて各酵素がどの部位を、どの順序で修飾したかを正確に追跡できます。
正常経路と腫瘍経路がどう分かれるか
健常な細胞では、過程の最初の酵素であるGALNT群は主にゴルジの早期区画に局在し、初期の糖ユニットを伸長・キャップする他の酵素と並んで働きます。研究チームは、こうした「共局在」条件下でGALNTがMUC1の一部の部位、著者が直接部位と呼ぶ箇所を主に修飾し、二つのより遅いレクチン依存部位はほとんど手付かずのままであることを示しました。直接部位に最初の糖(GalNAc)が付加されると、下流の酵素であるC1GALT1が迅速に伸長したり、ST6GALNAC1などのシアル転移酵素がシアル酸を付加して、GALNTがレクチンベースの機構で残りの部位を密に埋めるのを実質的に阻害します。その結果、正常な上皮MUC1に典型的な、控えめで制御された糖パターンが生じます。
がん様の酵素再配置を模擬する
多くの腫瘍ではGALNT酵素がゴルジから小胞体(ER)へ顕著に再配置され、いくつかのグリコシル化酵素の量も変化します。研究者らは、まずGALNTを単独でより長時間作用させてから下流の酵素を追加することでこれを模倣しました。この条件下では、初期の糖が容易に修飾される直接部位から遅いレクチン依存部位へ徐々に広がり、最終的にMUC1の全五箇所を占有しました。この飽和が起きた後でのみ伸長・キャッピング酵素が加えられました。ER様のこのシナリオは、腫瘍に関連するMUC1に類似した高度に糖鎧されたMUC1を生み出し、がん進展、免疫回避、転移と相関することが知られるTnおよびシアル化Tn(sTn)抗原が豊富に含まれていました。
単一のホットスポット部位に注目する
腫瘍MUC1の臨床的に重要な特徴の一つは、GalNAcに直接結合した短いシアル酸キャップ糖であるsialyl-Tnの存在です。これがMUC1のどこに現れるかを正確に明らかにするため、チームは動力学実験、コンピュータードッキング、ハイブリッド量子/古典シミュレーションを組み合わせました。その結果、酵素ST6GALNAC1がMUC1上のTnおよびT抗原にα2-6結合でシアル酸を付加する唯一の酵素であり、全五箇所がGalNAcを持つ状態になると、PDTR領域の特定のスレオニン部位(論文中でT13と呼ばれる)に強い選好性を示すことが分かりました。構造モデルと反応経路シミュレーションは、この部位で糖と触媒残基が近接して反応のエネルギー障壁を隣接部位よりも大きく下げる幾何学配列をとることを示し、sTnがそこで最初かつ最も強く現れる理由を説明します。
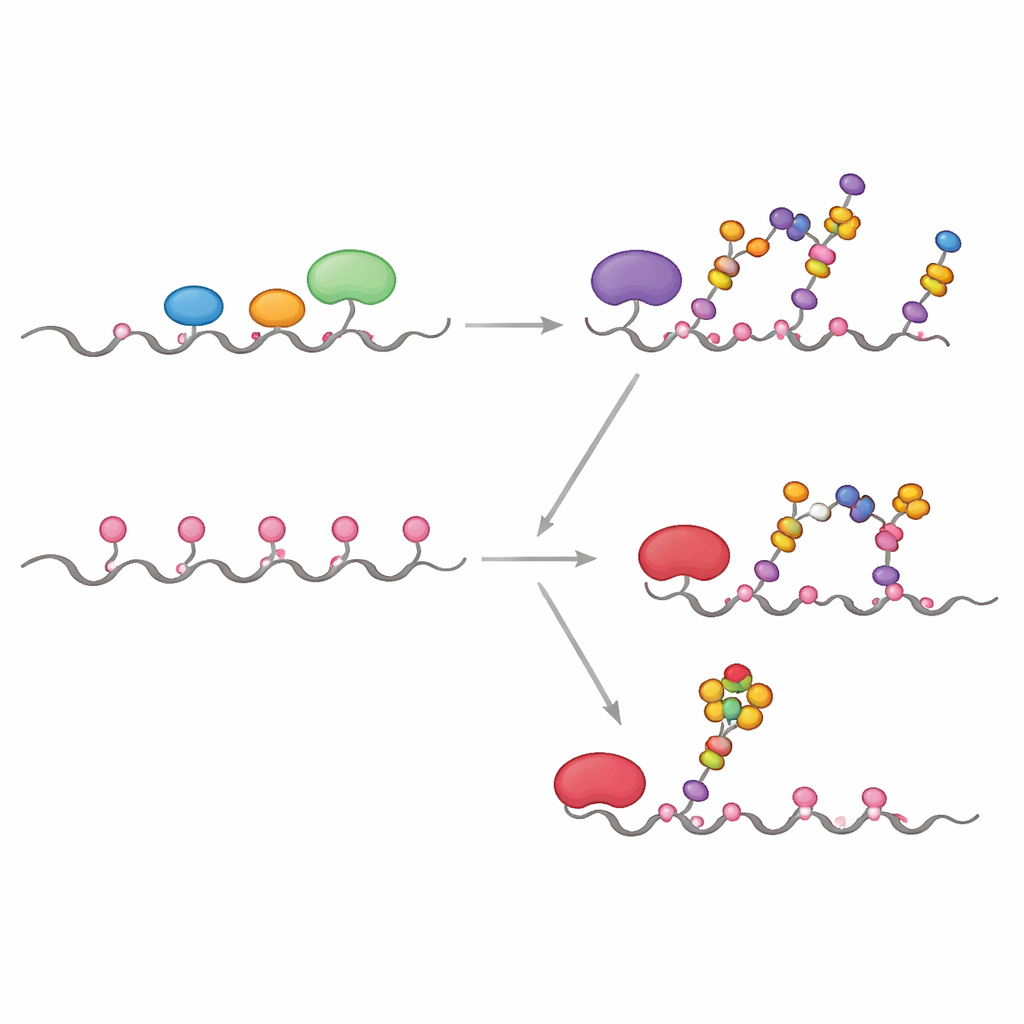
がんの理解と標的化にとっての意義
これらの実験とシミュレーションを総合すると、正常なMUC1と腫瘍関連MUC1の違いは、どの酵素が存在するかよりも、酵素が細胞内のどこに位置し、どれだけ長く作用できるかによって主に決まることが示されます。GALNTが競合する酵素とともにゴルジに留まる場合、それらは主に高速な部位だけを飾り、典型的なコア1糖と限定的なシアル化を生じさせます。多くのがんで見られるようにGALNTがERに再配置されると、速い部位と遅い部位の両方を埋める時間を得て、GalNAcで密に覆われたMUC1を作り出します。これがT13部位でのST6GALNAC1にとって極めて良い基質となり、sTnレベルを急激に高めます。このシステムレベルの見方は、酵素の局在、反応の時間軸、分子幾何学を一つの枠組みに結び付け、細胞の糖工場における一見わずかな変化がどのように強力な腫瘍特異的マーカーを生み出すかを説明し、診断、ワクチン、グリカンに焦点を当てたがん治療のより精密な標的を示唆します。
引用: Nashed, A., Dilsook, K., Senapathi, T. et al. An in vitro approach for simulating divergent Golgi O-glycosylation of tumor-associated MUC1 from normal MUC1. Nat Commun 17, 3619 (2026). https://doi.org/10.1038/s41467-026-72151-y
キーワード: タンパク質のグリコシル化, MUC1, がんバイオマーカー, ゴルジ体, シアル酸化Tn抗原