Clear Sky Science · zh
可遗传编码的可编程钙通道抑制结合体的工程化
调低细胞的音量旋钮
许多细胞依赖短暂的钙突发来决定何时移动、分裂或发动免疫攻击。当这种钙信号过度活跃时,可能导致罕见的遗传性疾病、慢性炎症,甚至削弱抗癌 T 细胞的功能。本研究介绍了一组定制的蛋白工具,称为 CRABs,它们像可编程的阻尼器一样作用于细胞中一条主要的钙进入通路,为基础研究和未来治疗打开了新可能。
细胞如何将钙用作开关
在大多数非神经细胞中,钙的主要通道是称为 CRAC 的结构,由两部分组成:感知内源储存钙浓度的 STIM,以及位于外膜上的孔道 ORAI。当内部储存钙耗尽时,STIM 改变构象,迁移到内外膜接触区并抓住 ORAI。通道随之开放,钙涌入并触发从短期运动到长期基因活动改变的响应。在免疫细胞中,这一路径对激活诸如 NFAT 之类的转录因子至关重要,这些因子开启所需的防御基因,但若失控则可引发疾病。
当钙信号出错时
遗传突变使 STIM 或 ORAI 持续处于“开启”状态,会导致多系统疾病,如 Stormorken 综合征,其特征包括血小板减少、出血、肌无力等。较轻但长期的该通路过度激活会促成自身免疫、癌症进展以及用于白血病治疗的工程化 CAR‑T 细胞的功能耗竭。药物开发者曾尝试用小分子阻断 CRAC 通道,但许多化合物也作用于其它离子通道或器官,导致副作用并阻碍临床进展。一直缺乏一种更特异、可调且能遗传靶向地抑制 CRAC 活性的手段。
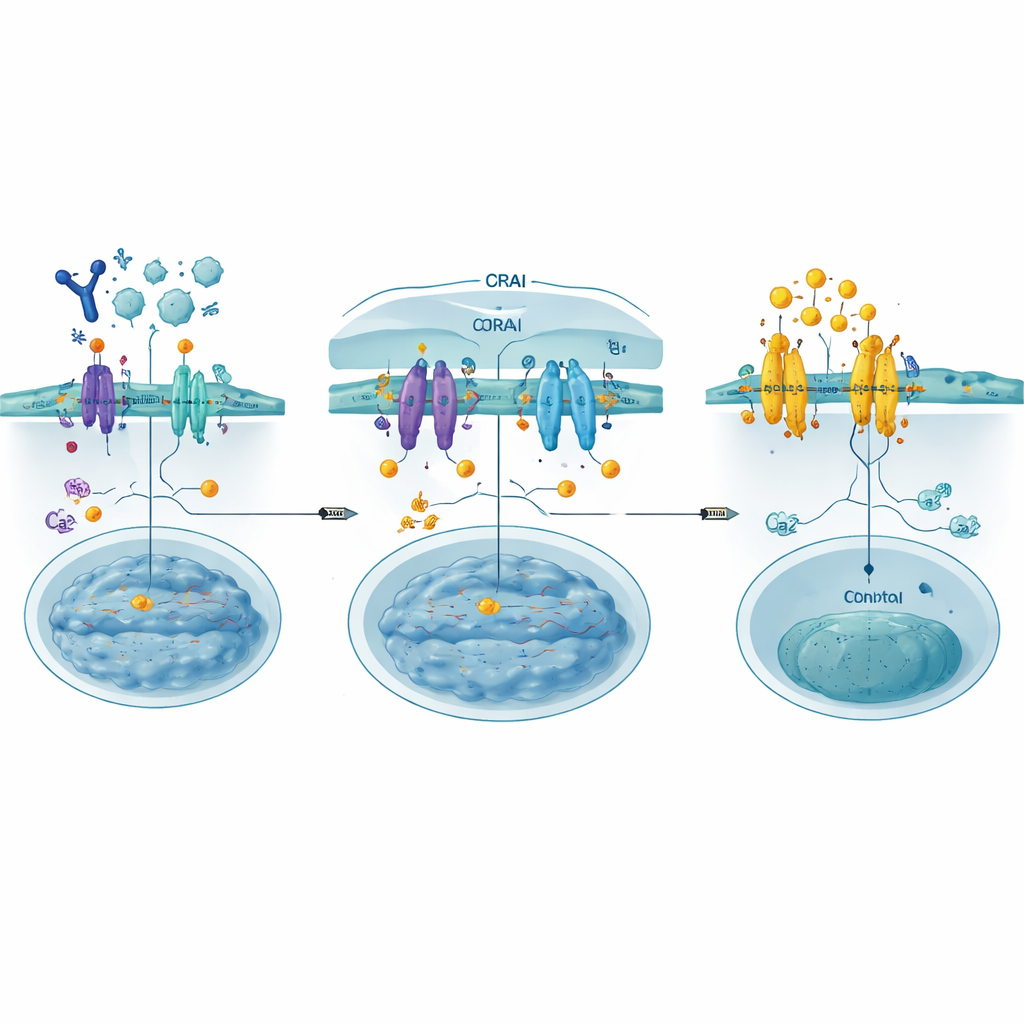
构建障位以堵住闸门
作者设计了 CRABs(CRAC 通道抑制结合体),它们是短小的、可遗传编码的蛋白片段,模仿 ORAI 上 STIM 正常结合的区域。这些诱饵锚定在细胞膜上,在 STIM 接触到真实 ORAI 通道之前先将活化的 STIM 捕获,从而在钙流入的上游有效关闭闸门。通过深度突变扫描——系统性地测试数百种小的序列变化——他们识别出一种结合力特别强的变体,命名为 PM‑CRAB,在人细胞中强烈降低了钙进入和 NFAT 向细胞核的转位。结构建模提示,单个氨基酸替换使 CRAB 肽更紧密地契合 STIM 的结合槽,稳定了这种配对并增强了阻断效果。
从鱼类血小板到可编程调光器
为证明 CRABs 在活体中有效,研究团队使用了带有导致 CRAC 通道持续开启的致病 STIM1 突变的斑马鱼,模拟 Stormorken 综合征。这些鱼的荧光标记血栓细胞(类似血小板)显著减少。当共表达 PM‑CRAB 时,这些细胞的生成在很大程度上恢复,表明诱饵可以抵消有害的钙超载。研究者随后创建了一系列强度不同的 CRAB 变体:单体、二聚体和四聚体,逐步增强通道抑制力。关键是,他们还构建了可被蓝光开启的版本(Opto‑CRAB)以及可被雷帕霉素或一种无免疫抑制活性的类似物激活的版本(Chemo‑CRAB)。在培养细胞中,这些开关允许根据光或药物的时序对钙进入和 NFAT 激活进行快速且可逆的控制。
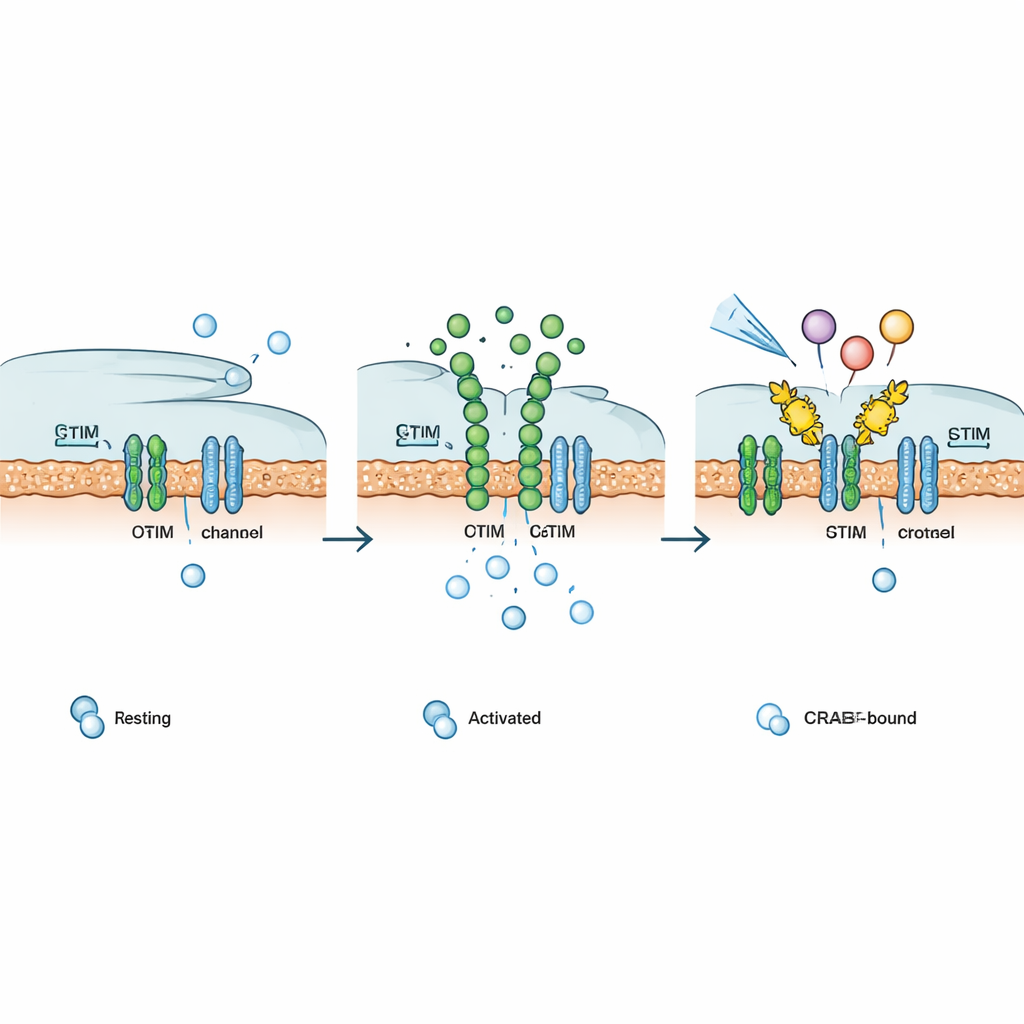
按需调节免疫和信号通路
因为体内许多表面受体——如某些激素、促生长因子受体和 G 蛋白偶联受体——最终依赖 CRAC 通道维持钙信号,作者测试了 Chemo‑CRAB 是否能在多样通路中发挥作用。一旦由化学触发激活,Chemo‑CRAB 抑制了由工程化的光或咖啡因门控钙激活器、合成和天然促生长因子受体以及若干不同的 G 蛋白偶联受体驱动的钙响应。在 T 细胞中,膜锚定的 CRAB 消除了 CRAC 电流并显著降低 NFAT 依赖的基因活性。在靶向 CD19 阳性肿瘤细胞的人类 CAR‑T 细胞中,PM‑CRAB 减少了关键炎性细胞因子的释放,而 Chemo‑CRAB 则实现了剂量依赖的按需抑制,提示能够在不永久禁用细胞的情况下限制耗竭与毒性。
这对未来治疗可能意味着什么
对于非专业读者,CRABs 可被视为对钙信号的高度特异性、可遗传编码的音量旋钮。通过作用于 STIM 与 ORAI 之间的精确“握手”处,它们关闭了一条中心的钙进入通路,而不会广泛干扰其他通道或上游受体。该工作展示了这些工具能够纠正斑马鱼中的类似疾病表型、剖析细胞内复杂的信号网络,并以可编程方式调控工程化的免疫细胞。尽管仍面临挑战——例如安全递送基因以及避免在健康组织中过度长期阻断——该研究搭建了一个多用途平台,未来可能有助于治疗罕见的钙通道疾病并微调像 CAR‑T 这样强大但脆弱的疗法。
引用: Liu, X., Ali, S., Lan, TH. et al. Engineering of genetically encoded programmable calcium channel inhibitory binders. Nat Commun 17, 3472 (2026). https://doi.org/10.1038/s41467-026-71769-2
关键词: 钙信号, CRAC 通道, 光遗传学, 化学遗传学, CAR-T 细胞