Clear Sky Science · nl
Ontwerpen van genetisch gecodeerde programmeerbare remmers van calciumkanalen
De volumeknoppen van cellen iets lager zetten
Veel van onze cellen vertrouwen op korte calciumpulsen om te beslissen wanneer ze zich verplaatsen, delen of een immuunreactie starten. Wanneer dit calciumsignaal te sterk wordt, kan het zeldzame erfelijke aandoeningen voeden, chronische ontsteking veroorzaken en zelfs de werking van kankervreters zoals T‑cellen beperken. Deze studie introduceert een reeks op maat gemaakte proteïnegereedschappen, CRABs genoemd, die fungeren als programmeerbare dempers op een belangrijke calciuminlaatroute in cellen en nieuwe mogelijkheden openen voor zowel fundamenteel onderzoek als toekomstige therapieën.
Hoe cellen calcium gebruiken als een aan‑uit‑schakelaar
In de meeste niet‑zenuwachtige cellen is een hoofdtoegang voor calcium het CRAC‑kanaal, gevormd door twee partners: STIM, dat de calciumniveaus in een intern opslagcompartiment detecteert, en ORAI, een porie in het buitenste celmembraan. Wanneer de interne voorraad laag raakt, verandert STIM van vorm, beweegt naar regio’s waar het interne en buitenmembraan elkaar raken en hecht zich aan ORAI. Dit opent het kanaal, waardoor calcium naar binnen stroomt en reacties uitlokt die variëren van kortstondige beweging tot langdurige veranderingen in genactiviteit. In immuuncellen is deze route essentieel voor het activeren van transcriptiefactoren zoals NFAT die genen inschakelen die nodig zijn voor verdediging; blijft het ongeremd, dan kan het ziekte veroorzaken.
Wanneer calciumsignalering ontspoort
Erfelijke veranderingen die STIM of ORAI permanent in de “aan”‑stand zetten, kunnen multipele systeemstoornissen veroorzaken, zoals het Stormorken‑syndroom, gekenmerkt door lage plaatjestellingen, bloedingsproblemen, spierzwakte en andere klachten. Mildere maar chronische overactivatie van hetzelfde pad draagt bij aan auto‑immuniteit, tumorprogressie en uitputting van kunstmatig gemaakte CAR‑T‑cellen die bij leukemiebehandeling worden ingezet. Geneesmiddelontwikkelaars hebben geprobeerd CRAC‑kanalen met kleine moleculen te blokkeren, maar veel van die verbindingen werken ook op andere ionkanalen en organen, wat bijwerkingen geeft en de klinische voortgang belemmert. Er ontbrak een specifieker, aanpasbaar en genetisch te richten middel om CRAC‑activiteit te beteugelen.
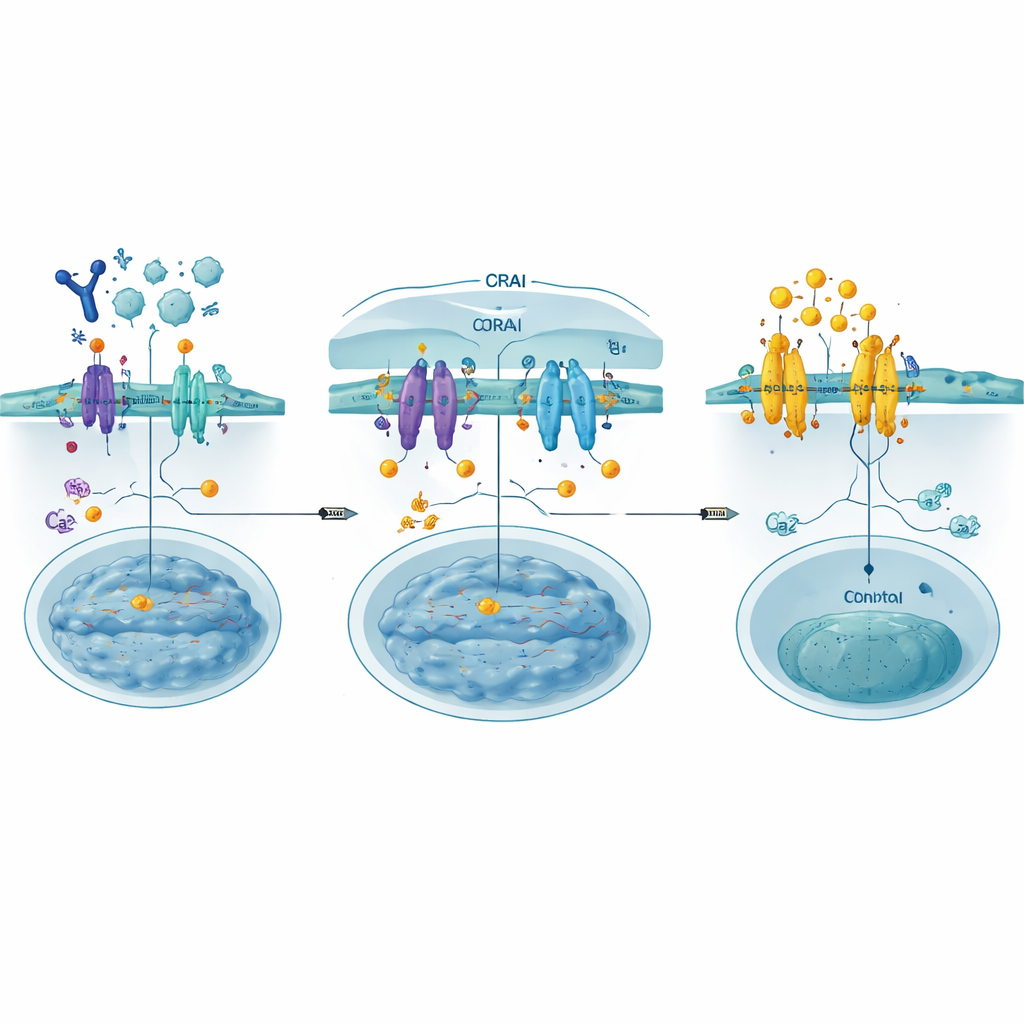
Lokmiddelen bouwen om de poort te blokkeren
De auteurs ontwierpen CRABs (CRAC‑kanaal remmende binders) als korte, genetisch gecodeerde eiwitfragmenten die een deel van ORAI nabootsen waar STIM normaal aan bindt. Aan het celmembraan verankerd vangen deze lokmiddelen geactiveerd STIM op voordat het zich aan echte ORAI‑kanalen kan vasthechten, en sluiten zo de poort stroomopwaarts van de calciuminstroom. Met behulp van deep mutational scanning — het systematisch testen van honderden kleine sequentieveranderingen — identificeerden ze een bijzonder sterke binder, PM‑CRAB genoemd, die de calciuminvoer en de verplaatsing van NFAT naar de kern in menselijke cellen krachtig verminderde. Structurele modellering wees erop dat een enkele aminozuurwissel het CRAB‑peptide nauwer in STIM’s bindingsgroef laat passen, waardoor het partnerschap wordt gestabiliseerd en de blokkerende werking verbetert.
Van visplaatjes tot programmeerbare dimmers
Om te demonstreren dat CRABs in levende organismen werken, gebruikte het team zebravissen die zodanig waren aangepast dat ze een ziekteveroorzakende STIM1‑mutatie dragen die CRAC‑kanalen openhoudt en het Stormorken‑syndroom nabootst. Deze vissen hebben aanzienlijk minder fluorescent gemarkeerde thrombocyten (plaatjesachtige cellen). Wanneer PM‑CRAB mede‑tot expressie werd gebracht, herstelde de productie van deze cellen grotendeels, wat aangeeft dat het lokmiddel de schadelijke calciumoverbelasting kon tegengaan. De onderzoekers creëerden vervolgens een familie van CRAB‑varianten met verschillende sterktes: monomeren, dimeren en tetrameren die geleidelijk de kanaalremming verhoogden. Belangrijk is dat ze ook uitvoeringen bouwden die kunnen worden ingeschakeld door blauw licht (Opto‑CRAB) of door kleine moleculen zoals rapamycine of een niet‑immunosuppressief analoog (Chemo‑CRAB). In gekweekte cellen maakten deze schakelaars snelle, omkeerbare controle van calciuminstroom en NFAT‑activatie mogelijk in reactie op licht of medicatietiming.
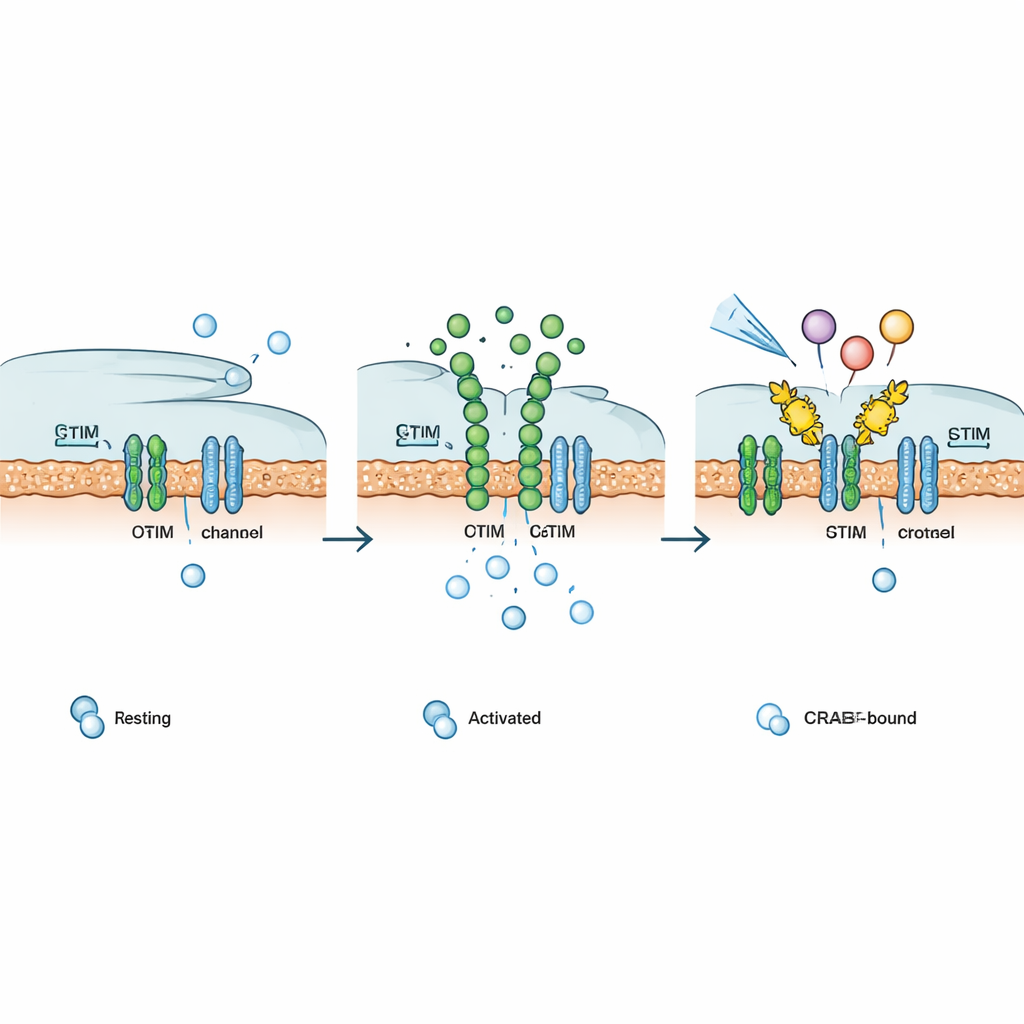
Immune en signaalroutes naar wens afstemmen
Aangezien veel receptoren aan het celoppervlak — zoals bepaalde hormoon‑, groeifactor‑ en G‑eiwit‑gekoppelde receptoren — uiteindelijk afhankelijk zijn van CRAC‑kanalen om calciumsignalen te onderhouden, testten de auteurs of Chemo‑CRAB in diverse pathways kon ingrijpen. Eenmaal geactiveerd door zijn chemische trigger dempte Chemo‑CRAB calciumreacties die werden aangedreven door geprogrammeerde licht‑ of cafeïne‑gestuurde calciumactuatoren, synthetische en natuurlijke groeifactorreceptoren en verschillende G‑eiwit‑gekoppelde receptoren. In T‑cellen schafte een aan het membraan verankerde CRAB CRAC‑stromen af en verlaagde sterk NFAT‑afhankelijke genactiviteit. In humane CAR‑T‑cellen die CD19‑positieve kankercellen aanvielen, verminderde PM‑CRAB de afgifte van belangrijke ontstekingscytokinen, terwijl Chemo‑CRAB dosisafhankelijke, op‑aanvraag demping van activatie mogelijk maakte, wat hint naar een manier om uitputting en toxiciteit te beperken zonder de cellen permanent uit te schakelen.
Wat dit kan betekenen voor toekomstige therapieën
Voor niet‑specialisten kunnen CRABs worden gezien als zeer specifieke, genetisch gecodeerde volumeknoppen voor calciumsignalering. Door in te grijpen precies bij het contactpunt tussen STIM en ORAI, schakelen ze een centrale calciuminlaatroute uit zonder breed andere kanalen of upstreamreceptoren te verstoren. Het werk toont aan dat deze hulpmiddelen ziekteachtige kenmerken in zebravissen kunnen corrigeren, complexe signaalnetwerken in cellen kunnen ontleden en geprogrammeerd immuuncellen kunnen moduleren. Hoewel er uitdagingen blijven — zoals het veilig afleveren van de genen en het vermijden van overmatige langdurige blokkade in gezonde weefsels — legt de studie een veelzijdig platform bloot dat uiteindelijk kan helpen bij de behandeling van zeldzame calciumkanaalaandoeningen en het verfijnen van krachtige maar kwetsbare therapieën zoals CAR‑T‑cellen.
Bronvermelding: Liu, X., Ali, S., Lan, TH. et al. Engineering of genetically encoded programmable calcium channel inhibitory binders. Nat Commun 17, 3472 (2026). https://doi.org/10.1038/s41467-026-71769-2
Trefwoorden: calciumsignaal, CRAC-kanalen, optogenetica, chemogenetica, CAR-T‑cellen