Clear Sky Science · pl
Inżynieria genetycznie kodowanych programowalnych inhibitorów kanałów wapniowych
Ściszanie komórkowych pokręteł głośności
Wiele naszych komórek polega na krótkich impulsach wapnia, aby zdecydować, kiedy się przemieszczać, dzielić lub uruchomić odpowiedź immunologiczną. Gdy ta sygnalizacja wapniowa jest nadmiernie aktywna, może napędzać rzadkie choroby genetyczne, przewlekłe stany zapalne, a nawet ograniczać siłę komórek T walczących z nowotworem. W tym badaniu przedstawiono zestaw zaprojektowanych białkowych narzędzi nazwanych CRAB, które działają jak programowalne tłumiki głównego szlaku napływu wapnia do komórek, otwierając nowe możliwości zarówno dla badań podstawowych, jak i przyszłych terapii.
Jak komórki używają wapnia jako wyłącznika
W większości komórek nie‑nerwowych głównym „wejściem” dla wapnia jest struktura znana jako kanał CRAC, utworzona przez dwóch partnerów: STIM, który wyczuwa poziom wapnia w wewnętrznym zbiorniku, oraz ORAI, por w zewnętrznej błonie komórkowej. Gdy zapasy wewnętrzne się wyczerpują, STIM zmienia kształt, przemieszcza się do miejsc styku błon wewnętrznej i zewnętrznej i przyczepia się do ORAI. To otwiera kanał, pozwalając wapniowi napłynąć i wywołać reakcje od krótkotrwałego ruchu po długotrwałe zmiany aktywności genów. W komórkach układu odpornościowego ten szlak jest kluczowy do aktywacji czynników transkrypcyjnych, takich jak NFAT, które włączają geny potrzebne do obrony, ale jeśli wymknie się spod kontroli, może prowadzić do choroby.
Gdy sygnalizacja wapniowa idzie nie tak
Zmiany dziedziczne, które trwale ustawiają STIM lub ORAI w pozycji „włączonej”, mogą powodować wieloukładowe zaburzenia, takie jak zespół Stormorkena, charakteryzujący się niską liczbą płytek, skłonnościami do krwawień, osłabieniem mięśni i innymi problemami. Łagodniejsze, lecz przewlekłe nadmierne pobudzenie tego samego szlaku przyczynia się do chorób autoimmunologicznych, progresji nowotworów i wyczerpania inżynieryjnych komórek CAR‑T stosowanych w terapii białaczki. Twórcy leków próbowali blokować kanały CRAC za pomocą małych cząsteczek, ale wiele z tych związków oddziałuje też na inne kanały jonowe i narządy, powodując skutki uboczne i zatrzymanie postępów klinicznych. Brakowało bardziej specyficznego, regulowanego i genetycznie ukierunkowanego sposobu ograniczania aktywności CRAC.
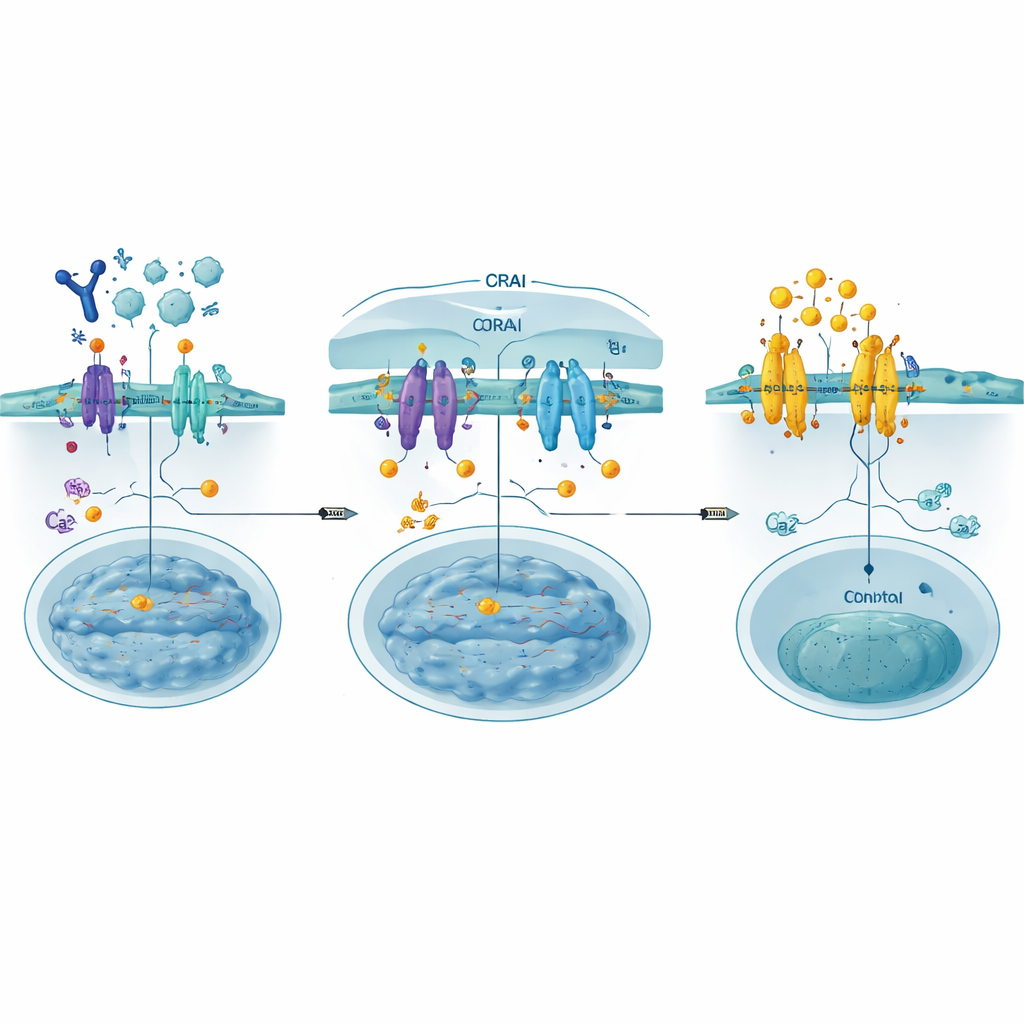
Budowanie przynęt, by zablokować bramę
Autorzy zaprojektowali CRABy (CRAC channel inhibitory binders) jako krótkie, genetycznie kodowane fragmenty białkowe naśladujące część ORAI, do której normalnie wiąże się STIM. Zakotwiczone w błonie komórkowej te „przynęty” łapią aktywowany STIM, zanim ten zdąży przyłączyć się do prawdziwych kanałów ORAI, skutecznie zamykając bramę upstream od przepływu wapnia. Korzystając z głębokiego skanowania mutacyjnego — systematycznego testowania setek drobnych zmian sekwencji — zidentyfikowali szczególnie silny egzemplarz, nazwany PM‑CRAB, który efektywnie zmniejszał napływ wapnia i przemieszczanie się NFAT do jądra w komórkach ludzkich. Modele strukturalne sugerowały, że pojedyncza zamiana aminokwasu sprawia, że peptyd CRAB lepiej dopasowuje się do rowka wiążącego STIM, stabilizując partnerstwo i zwiększając moc blokady.
Od płytek ryb do programowalnych ściemniaczy
Aby pokazać, że CRABy działają u żywych organizmów, zespół użył zebrafish zmodyfikowanych genetycznie tak, by niosły mutację STIM1 powodującą utrzymanie kanałów CRAC w stanie otwartym i naśladującą zespół Stormorkena. U tych ryb liczba fluorescencyjnie znakowanych trombocytów (komórek podobnych do płytek) była wyraźnie zmniejszona. Gdy współekspresowano PM‑CRAB, produkcja tych komórek w dużej mierze się odnowiła, co wskazuje, że przynęta mogła przeciwdziałać szkodliwemu przeciążeniu wapniem. Naukowcy stworzyli następnie rodzinę wariantów CRAB o różnych siłach: monomery, dimery i tetramery, które stopniowo zwiększały hamowanie kanału. Co kluczowe, opracowali też wersje, które można przełączać światłem niebieskim (Opto‑CRAB) lub małymi cząsteczkami, takimi jak rapamycyna lub jej nieimmunosupresyjny analog (Chemo‑CRAB). W hodowlach komórek te przełączniki umożliwiały szybkie, odwracalne sterowanie napływem wapnia i aktywacją NFAT w odpowiedzi na światło lub podanie leku.
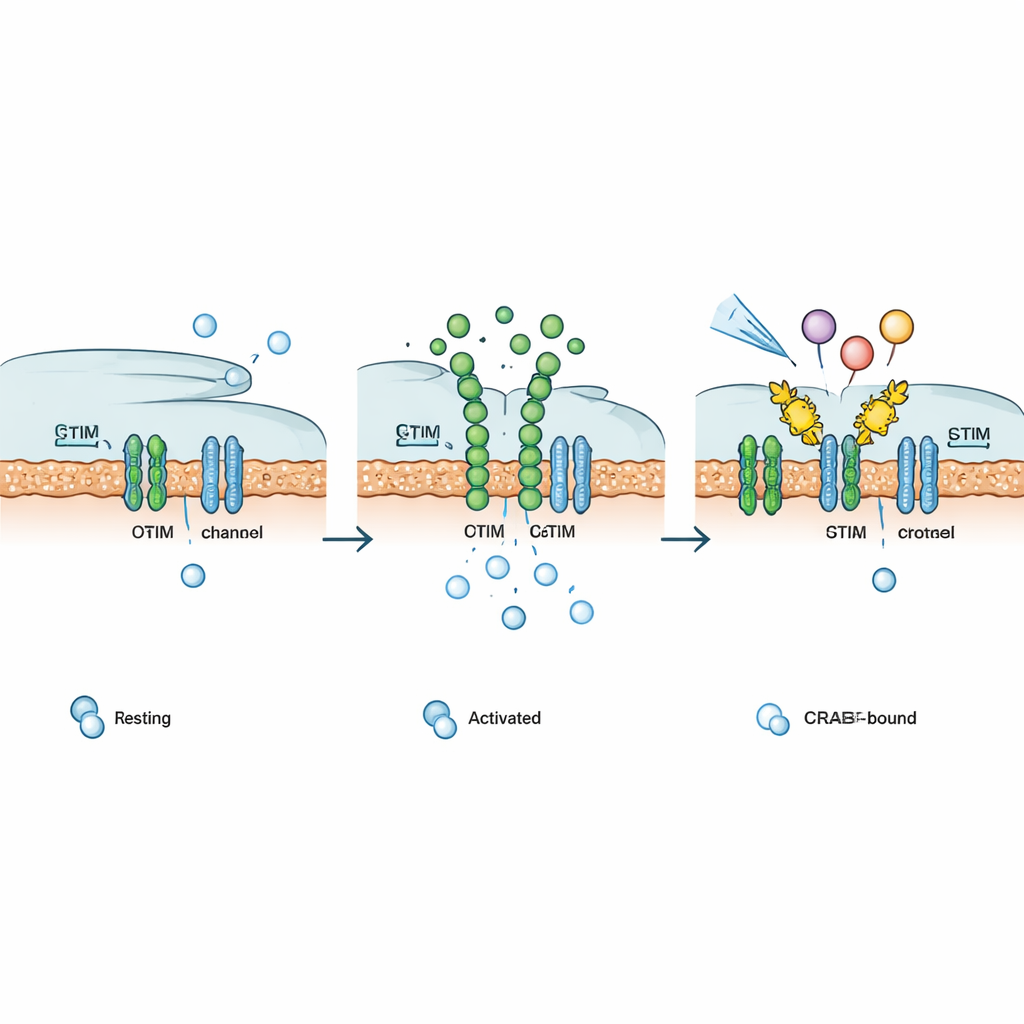
Dostrajanie dróg odporności i sygnalizacji na żądanie
Ponieważ wiele receptorów powierzchniowych w organizmie — takich jak niektóre receptory hormonów, czynników wzrostu i sprzężone z białkami G — ostatecznie polega na kanałach CRAC, aby podtrzymać sygnały wapniowe, autorzy sprawdzili, czy Chemo‑CRAB może interweniować w różnych ścieżkach. Po aktywacji przez wyzwalacz chemiczny Chemo‑CRAB stłumił odpowiedzi wapniowe indukowane przez zaprojektowane aktywatory wapniowe wrażliwe na światło lub kofeinę, syntetyczne i naturalne receptory czynników wzrostu oraz kilka różnych receptorów sprzężonych z białkami G. W komórkach T, CRAB zakotwiczony w błonie znosił prądy CRAC i wyraźnie obniżał aktywność genów zależnych od NFAT. W ludzkich komórkach CAR‑T skierowanych przeciw komórkom CD19‑pozytywnym, PM‑CRAB zmniejszył uwalnianie kluczowych cytokin zapalnych, podczas gdy Chemo‑CRAB umożliwił dawko‑zależne, na‑żądanie tłumienie aktywacji, co sugeruje sposób ograniczania wyczerpania i toksyczności bez trwałego wyłączania komórek.
Co to może znaczyć dla przyszłych terapii
Dla osoby niebędącej specjalistą CRABy można uznać za wysoce specyficzne, genetycznie kodowane pokrętła głośności sygnalizacji wapniowej. Działając dokładnie na styku STIM‑ORAI, wyłączają centralną drogę napływu wapnia bez szerokiego zakłócania innych kanałów czy receptorów upstream. Praca wykazuje, że te narzędzia mogą korygować cechy podobne do chorób w zebrafish, rozkładać złożone sieci sygnałowe w komórkach i programowalnie modulować inżynieryjne komórki odpornościowe. Mimo że pozostają wyzwania — takie jak bezpieczne dostarczanie genów i unikanie nadmiernej, długotrwałej blokady w zdrowych tkankach — badanie przedstawia wszechstronną platformę, która w przyszłości może pomóc leczyć rzadkie zaburzenia kanałów wapniowych oraz precyzyjnie dostrajać potężne, lecz delikatne terapie, takie jak komórki CAR‑T.
Cytowanie: Liu, X., Ali, S., Lan, TH. et al. Engineering of genetically encoded programmable calcium channel inhibitory binders. Nat Commun 17, 3472 (2026). https://doi.org/10.1038/s41467-026-71769-2
Słowa kluczowe: sygnalizacja wapniowa, kanały CRAC, optogenetyka, chemogenetyka, komórki CAR‑T