Clear Sky Science · ja
遺伝子でコード化されたプログラム可能なカルシウムチャネル阻害バインダーの設計
細胞のボリュームつまみを下げる
多くの細胞は、移動、分裂、あるいは免疫応答を引き起こすかどうかを決めるために微小なカルシウムの急増に依存しています。このカルシウムシグナルが過剰になると、稀な遺伝性疾患や慢性炎症を助長し、がんと闘うT細胞の性能を制限することさえあります。本研究はCRABと呼ばれる一連の特注タンパク質ツールを紹介します。これらは細胞内の主要なカルシウム流入経路に対するプログラム可能なダンパーとして働き、基礎研究や将来の治療法に新たな可能性を開きます。
細胞がカルシウムをオン・オフスイッチとして使う仕組み
多くの非神経細胞では、カルシウムの主要な出入口はCRACチャネルと呼ばれる構造で、内部貯蔵のカルシウム濃度を感知するSTIMと、細胞外膜の孔であるORAIという二つのパートナーから成ります。内部貯蔵が枯渇するとSTIMは形を変え、内膜と外膜が接する領域に移動してORAIに結合します。これがチャネルを開き、カルシウムが流入して短期的な運動から長期的な遺伝子発現の変化まで様々な応答を引き起こします。免疫細胞では、この経路がNFATなどの転写因子を活性化し防御に必要な遺伝子をオンにするために不可欠ですが、制御が効かなくなると病態を促進します。
カルシウムシグナルが誤作動するとき
STIMやORAIが恒常的に「オン」状態になる遺伝的変化は、ストルモルケン症候群のような多系統障害を引き起こし、血小板減少、出血傾向、筋力低下などを伴います。同じ経路の軽度だが慢性的な過活動は自己免疫疾患、がん進行、白血病治療に用いるCAR‑T細胞の枯渇(エグゾースト)にも寄与します。薬剤開発者は小分子でCRACチャネルを阻害しようとしてきましたが、多くの化合物は他のイオンチャネルや臓器にも作用し、副作用や臨床開発の停滞を招きました。より特異的で調整可能かつ遺伝子的に標的化されたCRAC制御法はこれまで欠けていました。
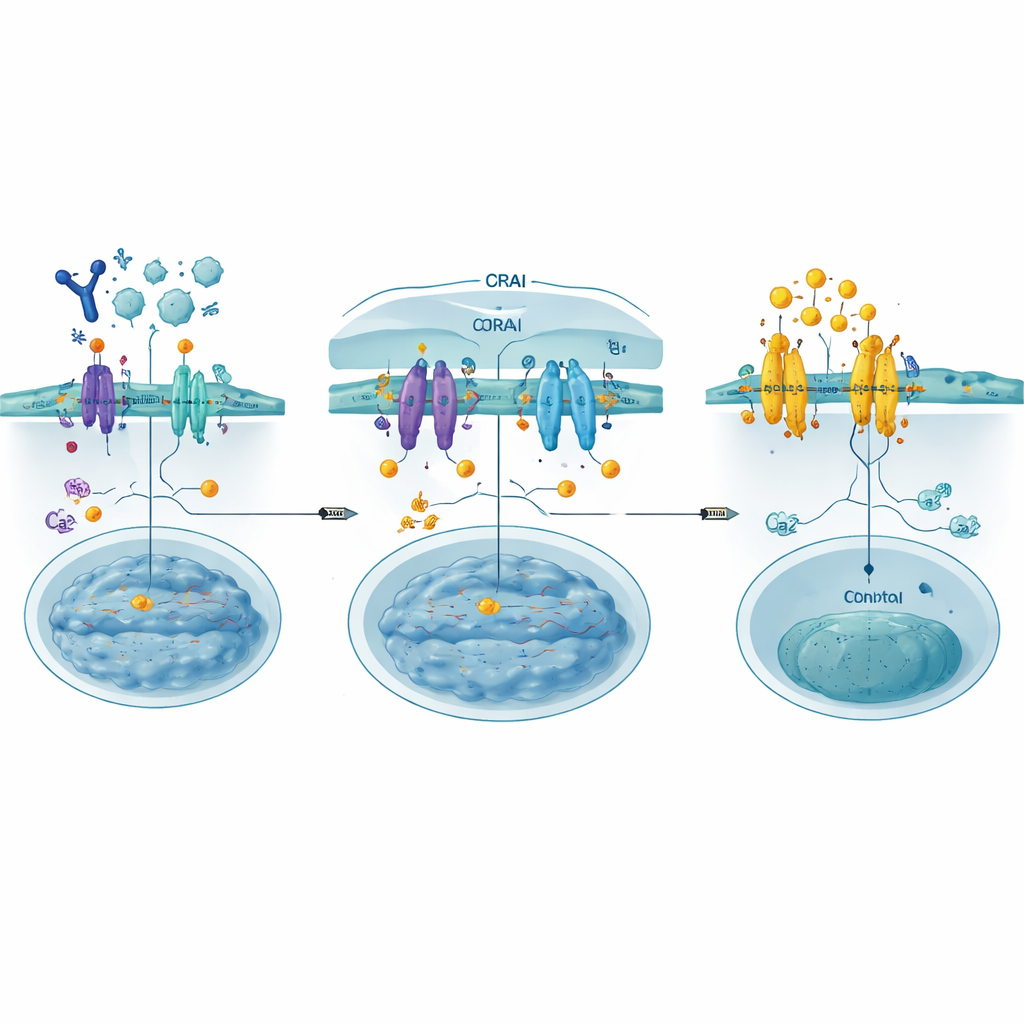
門をふさぐためのデコイを構築する
著者らはCRAB(CRAC channel inhibitory binders)を設計しました。これはSTIMが通常結合するORAIの一部を模倣する短い遺伝子コード化タンパク質断片です。細胞膜に固定されたこれらのデコイは、活性化したSTIMを本物のORAIに結合する前に捕まえ、上流でチャネルを閉じる効果を発揮します。ディープミューテーショナルスキャンニング—何百もの小さな配列変化を系統的に試す手法—を用いて、ヒト細胞でカルシウム流入と核内へのNFAT移行を強力に抑える高親和性のバインダー、PM‑CRABを同定しました。構造モデル解析は、単一のアミノ酸置換がCRABペプチドをSTIMの結合溝によりぴったりはめ込み、複合体を安定化して阻害力を高めることを示唆しました。
魚の血小板からプログラム可能なディマーへ
CRABが生体内で機能することを示すために、研究チームはCRACチャネルが恒常的に開いている病因性STIM1変異を持ち、ストルモルケン症候群を模倣するゼブラフィッシュを用いました。これらの魚は蛍光標識された血栓細胞(血小板様細胞)が著しく少なくなります。PM‑CRABを共発現させると、これらの細胞の産生が大部分回復し、デコイが有害なカルシウム過負荷に対抗できることを示しました。研究者らは次に、阻害強度の異なるCRABバリアント群を作成しました:モノマー、ダイマー、テトラマーで段階的にチャネル阻害を強める構成です。重要なことに、青色光でオンにできるバージョン(Opto‑CRAB)やラパマイシンや免疫抑制作用のない類縁体で作動するバージョン(Chemo‑CRAB)も構築しました。培養細胞では、これらのスイッチにより光や薬剤のタイミングに応じた迅速で可逆的なカルシウム流入とNFAT活性の制御が可能でした。
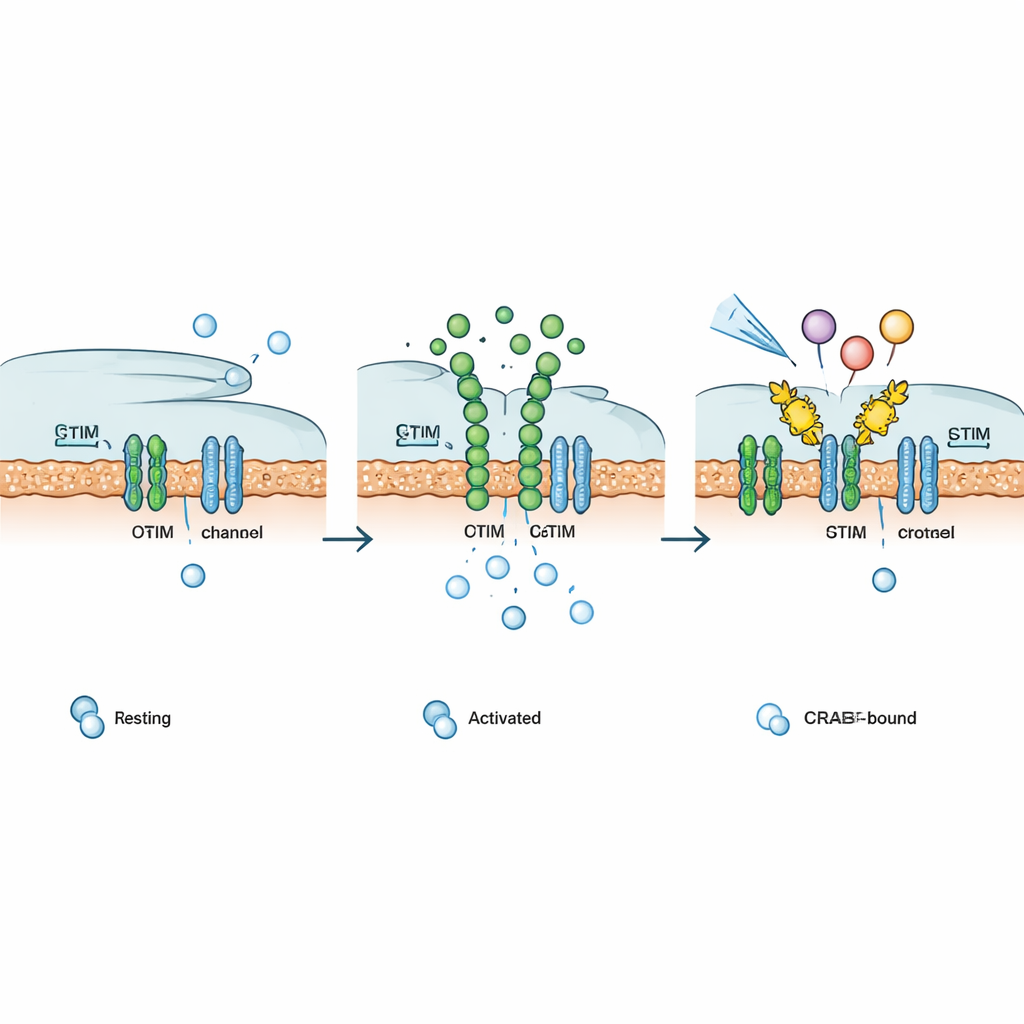
免疫とシグナル経路を必要に応じて調整する
体内の多くの表面受容体—ある種のホルモン、成長因子、Gタンパク質共役受容体など—は最終的に持続的なカルシウムシグナルを維持するためにCRACチャネルに依存するため、著者らはChemo‑CRABが多様な経路に介入できるかどうかを検証しました。化学的トリガーで活性化されると、Chemo‑CRABは人工的な光またはカフェインで作動するカルシウムアクチュエータ、合成および自然の成長因子受容体、複数の異なるGタンパク質共役受容体によるカルシウム応答を鈍らせました。T細胞では膜に固定されたCRABがCRAC電流を消失させ、NFAT依存の遺伝子活性を大幅に低下させました。CD19陽性がん細胞を標的とするヒトCAR‑T細胞では、PM‑CRABが主要な炎症性サイトカインの放出を減らし、Chemo‑CRABは投与量に応じてオンデマンドで活性化を抑えることを可能にし、細胞を恒久的に無効化することなく枯渇や毒性を制限する手段の可能性を示しました。
将来の治療にとっての意義
専門外の方にとって、CRABはカルシウムシグナル伝達のための非常に特異的な遺伝子コード化のボリュームつまみと考えることができます。STIMとORAIの正確な握手に作用することで、他のチャネルや上流受容体に広く干渉することなく中心的なカルシウム流入経路を遮断します。本研究は、これらのツールがゼブラフィッシュの病態様表現型を矯正し、細胞内の複雑なシグナルネットワークを解析し、プログラム可能な方法で改変免疫細胞を調整できることを示しています。遺伝子の安全な送達や健常組織における過度の長期的遮断を避けるといった課題は残りますが、この研究は希少なカルシウムチャネル障害の治療や、CAR‑T細胞のような強力だが繊細な治療法の微調整に将来役立つ可能性のある多用途プラットフォームを提示しています。
引用: Liu, X., Ali, S., Lan, TH. et al. Engineering of genetically encoded programmable calcium channel inhibitory binders. Nat Commun 17, 3472 (2026). https://doi.org/10.1038/s41467-026-71769-2
キーワード: カルシウムシグナル伝達, CRACチャネル, オプトジェネティクス, ケモジェネティクス, CAR-T細胞