Clear Sky Science · de
Entwicklung genetisch codierbarer, programmierbarer Inhibitor‑Bindemittel für Kalziumkanäle
Die Lautstärke der Zelle herunterregeln
Viele unserer Zellen verlassen sich auf winzige Kalziumausbrüche, um zu entscheiden, wann sie sich bewegen, teilen oder eine Immunreaktion auslösen. Wenn diese Kalziumsignale übermäßig stark werden, können sie seltene genetische Erkrankungen, chronische Entzündungen fördern und sogar die Leistungsfähigkeit krebsbekämpfender T‑Zellen einschränken. Diese Studie stellt eine Reihe maßgeschneiderter Proteinwerkzeuge vor, genannt CRABs, die wie programmierbare Dämpfer an einer wichtigen Kalziumeintrittspforte in Zellen wirken und neue Möglichkeiten für Grundlagenforschung und künftige Therapien eröffnen.
Wie Zellen Kalzium als Ein‑/Ausschalter nutzen
In den meisten nicht‑neuralen Zellen ist eine Hauptpforte für Kalzium der sogenannte CRAC‑Kanal, bestehend aus zwei Partnern: STIM, das den Kalziumgehalt eines internen Speichersensors misst, und ORAI, einer Porenstruktur in der äußeren Zellmembran. Wenn die internen Speicher leerer werden, ändert STIM seine Konformation, wandert zu Bereichen, in denen innere und äußere Membran aufeinandertreffen, und bindet an ORAI. Dadurch öffnet sich der Kanal, Kalzium strömt ein und löst Reaktionen aus, die von kurzfristiger Bewegung bis zu langfristigen Veränderungen der Genaktivität reichen. In Immunzellen ist dieser Weg entscheidend für die Aktivierung von Transkriptionsfaktoren wie NFAT, die Gene für die Abwehr einschalten; bleibt die Aktivität jedoch ungezügelt, kann sie Krankheiten antreiben.
Wenn Kalziumsignale außer Kontrolle geraten
Erbliche Veränderungen, die STIM oder ORAI dauerhaft in eine „ein“-Position versetzen, können multisystemische Erkrankungen verursachen, etwa das Stormorken‑Syndrom, das sich durch niedrige Thrombozytenzahlen, Blutungsneigung, Muskelschwäche und weitere Probleme auszeichnet. Milder, aber chronischer Überaktivierung desselben Weges trägt zu Autoimmunerkrankungen, Tumorprogression und zur Erschöpfung von konstruierten CAR‑T‑Zellen in der Leukämiebehandlung bei. Arzneimittelentwickler haben versucht, CRAC‑Kanäle mit kleinen Molekülen zu blockieren, doch viele dieser Verbindungen beeinflussen auch andere Ionenkanäle und Organe, was zu Nebenwirkungen und stagnierenden klinischen Studien geführt hat. Es fehlte an einem spezifischeren, einstellbaren und genetisch zielgerichteten Weg, die CRAC‑Aktivität zu drosseln.
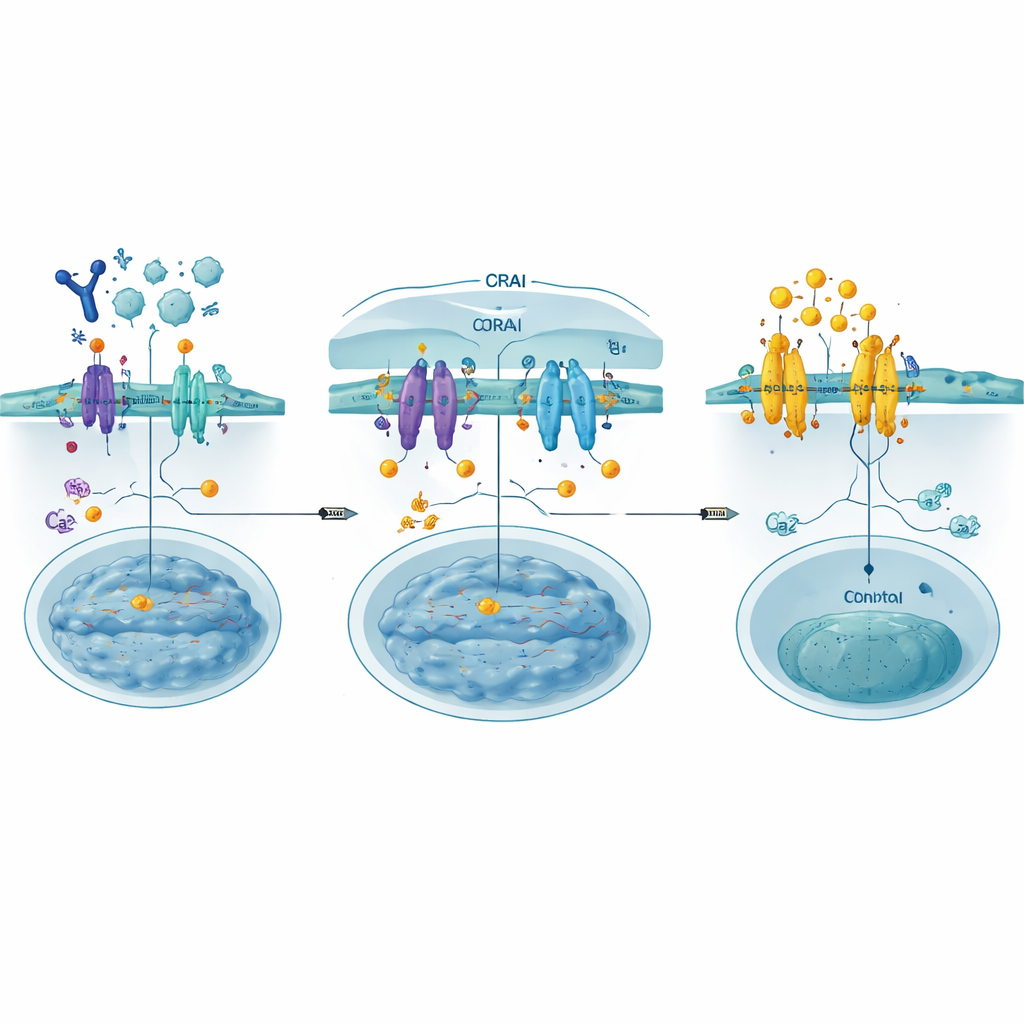
Lockmittel bauen, um das Tor zu blockieren
Die Autorinnen und Autoren entwickelten CRABs (CRAC channel inhibitory binders) als kurze, genetisch codierte Proteinfragmente, die einen Teil von ORAI nachahmen, an den STIM normalerweise bindet. An der Zellmembran verankert, fangen diese Täuschkörper aktiviertes STIM ab, bevor es an echte ORAI‑Kanäle andocken kann, und schließen so das Tor stromaufwärts des Kalziumflusses. Mithilfe von Deep‑Mutational‑Scanning — systematischem Testen hunderter kleiner Sequenzänderungen — identifizierten sie einen besonders starken Binder, genannt PM‑CRAB, der den Kalziumeinstrom und die NFAT‑Translokation in den Zellkern beim Menschen deutlich verringerte. Strukturmodellierungen deuten darauf hin, dass ein einziger Aminosäureaustausch das CRAB‑Peptid enger in STIMs Bindungsfurche einpasst, die Partnerschaft stabilisiert und die Blockierwirkung verbessert.
Von Fisch‑Thrombozyten zu programmierbaren Dimmerschaltern
Um zu zeigen, dass CRABs in lebenden Organismen funktionieren, verwendete das Team Zebrafische, die so verändert wurden, dass sie eine krankheitsverursachende STIM1‑Mutation tragen, welche die CRAC‑Kanäle offenhält und das Stormorken‑Syndrom nachahmt. Diese Fische zeigen deutlich weniger fluoreszent markierte Thrombozyten‑ähnliche Zellen. Bei Koinexpression von PM‑CRAB stellte sich die Bildung dieser Zellen weitgehend wieder her, was darauf hinweist, dass der Täuschkörper die schädliche Kalziumüberladung ausgleichen kann. Die Forschenden erzeugten anschließend eine Familie von CRAB‑Varianten mit unterschiedlichen Wirkstärken: Monomere, Dimere und Tetramere, die die Kanalhemmung schrittweise verstärkten. Entscheidenderweise bauten sie auch Varianten, die per Blaulicht (Opto‑CRAB) oder durch kleine Moleküle wie Rapamycin bzw. ein nicht‑immunsuppressives Analogon (Chemo‑CRAB) eingeschaltet werden können. In kultivierten Zellen ermöglichten diese Schalter eine schnelle, reversible Steuerung des Kalziumeinstroms und der NFAT‑Aktivierung in Abhängigkeit von Licht‑ oder Wirkstoffzufuhr.
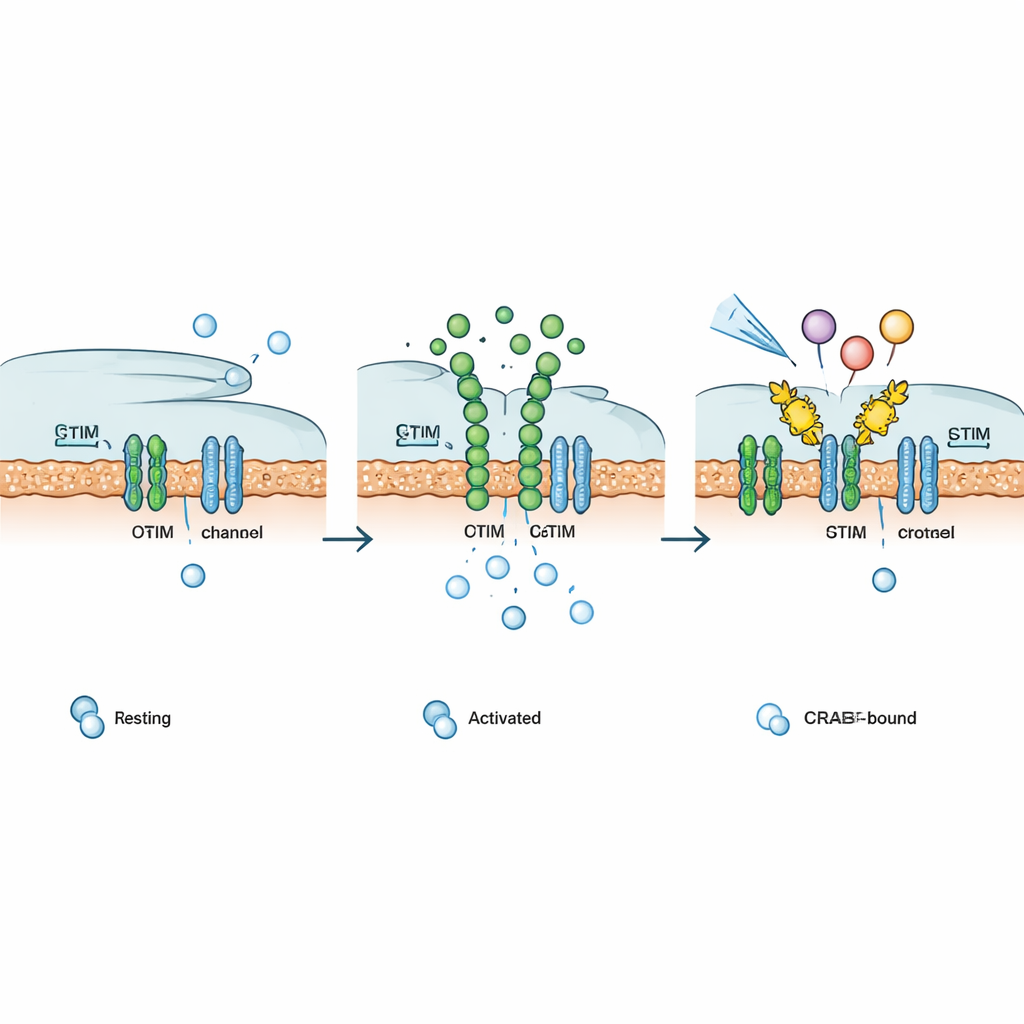
Signalwege des Immunsystems nach Bedarf justieren
Da viele Oberflächenrezeptoren im Körper — etwa bestimmte Hormon‑, Wachstumsfaktor‑ und G‑Protein‑gekoppelte Rezeptoren — letztlich auf CRAC‑Kanäle angewiesen sind, um Kalziumsignale aufrechtzuerhalten, prüften die Autoren, ob Chemo‑CRAB in unterschiedliche Pfade eingreifen kann. Nach Aktivierung durch seinen chemischen Auslöser schwächte Chemo‑CRAB Kalziumantworten ab, die durch gentechnisch veränderte Licht‑ oder Koffein‑gesteuerte Kalziumaktoren, synthetische und natürliche Wachstumsfaktorrezeptoren sowie mehrere verschiedene G‑Protein‑gekoppelte Rezeptoren hervorgerufen wurden. In T‑Zellen beseitigte ein membranverankertes CRAB CRAC‑Ströme und senkte die NFAT‑abhängige Genaktivität deutlich. In menschlichen CAR‑T‑Zellen, die CD19‑positive Krebszellen anvisieren, verringerte PM‑CRAB die Freisetzung wichtiger entzündungsfördernder Zytokine, während Chemo‑CRAB eine dosisabhängige, bedarfsgerechte Abschwächung der Aktivierung erlaubte — ein Hinweis auf eine Möglichkeit, Erschöpfung und Toxizität zu begrenzen, ohne die Zellen dauerhaft zu deaktivieren.
Was das für künftige Therapien bedeuten könnte
Für Nicht‑Expertinnen und Nicht‑Experten lassen sich CRABs als hochspezifische, genetisch codierte Lautstärkeregler für Kalziumsignale beschreiben. Indem sie an der präzisen Schnittstelle zwischen STIM und ORAI eingreifen, schalten sie eine zentrale Kalziumeintrittsroute ab, ohne breit andere Kanäle oder upstream‑Rezeptoren zu stören. Die Arbeit zeigt, dass diese Werkzeuge krankheitsähnliche Merkmale bei Zebrafischen korrigieren, komplexe Signalkanetze in Zellen auseinandernehmen und programmierbar eingreifen können, um gentechnisch veränderte Immunzellen zu modulieren. Trotz verbleibender Herausforderungen — etwa der sicheren Genabgabe und der Vermeidung einer übermäßigen langfristigen Blockade in gesundem Gewebe — legt die Studie eine vielseitige Plattform dar, die eines Tages helfen könnte, seltene Kalziumkanalerkrankungen zu behandeln und empfindliche, aber wirksame Therapien wie CAR‑T‑Zellen zu verfeinern.
Zitation: Liu, X., Ali, S., Lan, TH. et al. Engineering of genetically encoded programmable calcium channel inhibitory binders. Nat Commun 17, 3472 (2026). https://doi.org/10.1038/s41467-026-71769-2
Schlüsselwörter: Kalziumsignalgebung, CRAC‑Kanäle, Optogenetik, Chemogenetik, CAR‑T‑Zellen