Clear Sky Science · he
הנדסה של חלבונים מקודדים גנטית המעכבים באופן מתוכנת תעלות סידן
הנמכת כפתורי עוצמה תאיים
רבים מתאי הגוף מסתמכים על פרצי סידן זעירים כדי להחליט מתי לנוע, להתחלק או להשיק תגובה חיסונית. כשאותות הסידן האלה עוברים לתודעה גבוהה מדי, הם יכולים להזין הפרעות גנטיות נדירות, דלקת כרונית ואף להגביל את כוחם של תאי T שנלחמים בסרטן. המחקר מציג קבוצה של כלי חלבון מותאמים בשם CRABs, שפועלים כדמפרים מתוכנתים על מסלול כניסת סידן מרכזי בתאים — ופותחים אפשרויות חדשות למחקר בסיסי ולתרפיות עתידיות.
איך תאים משתמשים בסידן כמתג הדלקה/כיבוי
ברוב התאים שאינם עצביים, פתחה עיקרית לסידן היא מבנה הידוע כתעלת CRAC, המורכבת משני שותפים: STIM, החושש את רמות הסידן במחסן פנימי, ו‑ORAI, נקב בממברנת התא החיצונית. כאשר המאגרים הפנימיים מתרוקנים, STIM משנה צורה, נודד לאזורים שבהם הממברנות הפנימית והחיצונית נוגעות, ונאחז ב‑ORAI. הדבר פותח את התעלה ומאפשר לסידן להיכנס וליזום תגובות שנעות מתנועות קצרות טווח ועד שינויים ארוכי טווח בפעילות הגנים. בתאים חיסוניים, מסלול זה חיוני להפעלת גורמי שעתוק כמו NFAT שמפעילים גנים חיוניים להגנה, אך כשהוא דוהר ללא בקרה הוא עלול להניע מחלות.
כאשר איתות הסידן משתבש
שינויים תורשתיים שמחזיקים את STIM או ORAI במצב "פועל" קבוע עלולים לגרום להפרעות רב‑מערכתיות, כמו תסמונת סטורמורקן, המתאפיינת בספירת טסיות נמוכה, בעיות דימום, חולשת שרירים ואפיונים נוספים. הפעלה כרונית מתונה אך ממושכת של אותו מסלול תורמת למחלת חיסון עצמית, להתקדמות סרטן ולשחיקה של תאי CAR‑T מהונדסים המשמשים בטיפול בלוקמיה. מפתחים ניסו לחסום תעלות CRAC בעזרת מולקולות קטנות, אך רבות מהתרכובות האלה משפיעות גם על תעלות יוניות ואיברים אחרים, מה שמוביל לתופעות לוואי ולעיכובים בפיתוח הקליני. היה חסר אמצעי ממוקד, מתכוונן ומיועד גנטית לשלוט בפעילות CRAC.
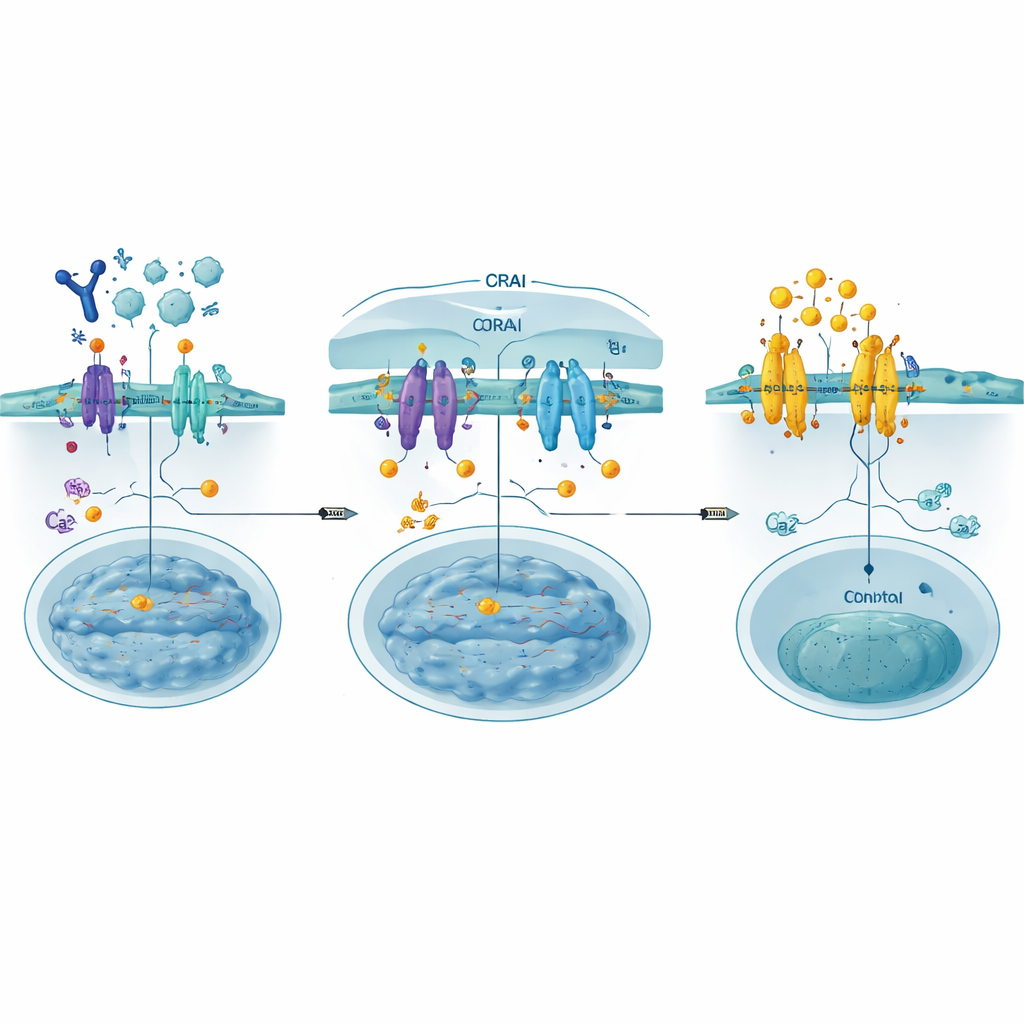
בניית דמויים לחסימת השער
המחברים תכננו את ה‑CRABs (CRAC channel inhibitory binders) כחתיכות חלבון קצרות המקודדות גנטית ומחקות חלק של ORAI שבו STIM בדרך כלל נקשר. עוגנים בממברנת התא, דמויים אלה תופסים את STIM המופעל לפני שהוא יכול להיאחז ב‑ORAI האמיתי, ובכך סוגרים את השער מעלה לזרימת הסידן. באמצעות סריקה עמוקה של מוטציות — בדיקה שיטתית של מאות שינויים קטנים ברצף — זוהה קושר חזק במיוחד, שכונה PM‑CRAB, שהקטין באופן יעיל את כניסת הסידן ואת תנועת NFAT לגרעין בתאים אנושיים. מודלים מבניים הציעו שמחליף חומצת אמינו יחיד גורם לפפטיד CRAB להתאים ביתר הדוק לאתר הקישור של STIM, לייצב את השותפות ולשפר את עוצמת החסימה.
מטסות דגים עד דימרים מתוכנתים
כדי להראות שה‑CRABs פועלים בחיות חיות, הצוות השתמש בדג הזברה מהונדס לשאת מוטציה ב‑STIM1 שגורמת לתעלות CRAC להישאר פתוחות ומחקה את תסמונת סטורמורקן. לדגים אלה יש פחות תאים טסיתיים (דמויי‑platelet) המסומנים בצורה זוהרת. כשה‑PM‑CRAB הובע במקביל, ייצור התאים האלה התאושש ברובו, מה שמעיד שהדמוי יכול לנטרל עודף סידן מזיק. החוקרים יצרו משפחה של וריאנטים של CRAB בעוצמות שונות: מונומרים, דימרים וטטראמרים שהגבירו בהדרגה את עיכוב התעלה. חשוב מכך, הם גם בנו גרסאות שניתן להדליק אותן באור כחול (Opto‑CRAB) או באמצעות מולקולות קטנות כמו ראפמיצין או אנלוג שאינו מדכא חיסונית (Chemo‑CRAB). בתרביות תאים, מתגים אלה איפשרו בקרה מהירה והפיכה של כניסת הסידן והפעלת NFAT כתלות בזמן האור או התרופה.
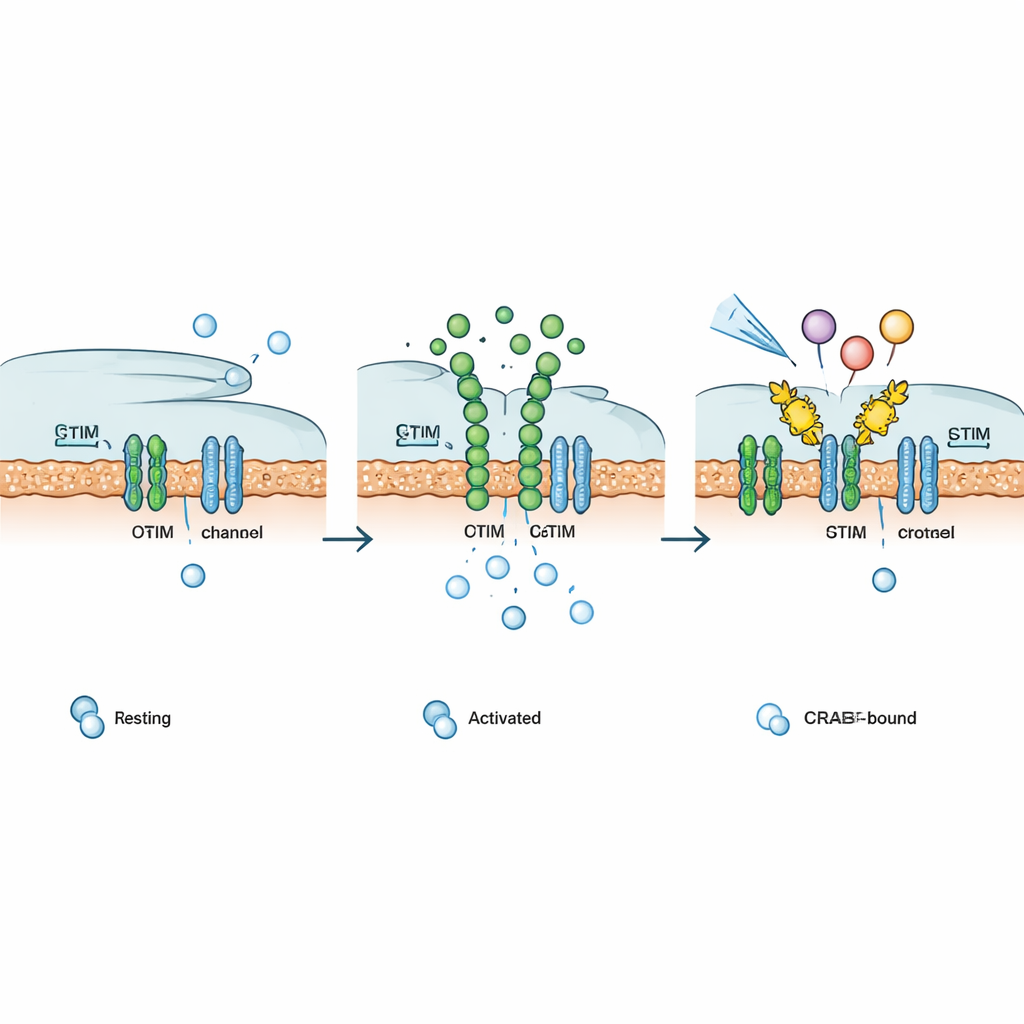
כיוונון מסלולי חיסון ואיתות לפי דרישה
מכיוון שרבים מהקולטן על המשטח — כגון קולטי הורמונים, גורמי גדילה וקולטי G‑protein‑coupled — תלויים בסופו של דבר בתעלות CRAC לשמירה על אותות סידן, המחברים בדקו האם Chemo‑CRAB יכול להתערב במסלולים שונים. לאחר הפעלה על ידי המגרה הכימי שלו, Chemo‑CRAB החליש תגובות סידן המונעות על ידי מועברי סידן הניתנים לאור או לקפאין, קולטי גורמי גדילה סינתטיים וטבעיים, ומספר קולטי G‑protein‑coupled שונים. בתאי T, CRAB בעוגן ממברנלי ביטל את הזרמים של CRAC והוריד בצורה חדה את פעילות הגנים התלויה ב‑NFAT. בתאי CAR‑T אנושיים המכוונים לתאים סרטניים בעלי CD19, PM‑CRAB הקטין את שחרור הציטוקינים הדלקתיים המרכזיים, בעוד Chemo‑CRAB איפשר דיכוי כמותי, לפי מינון ובזמנית, של ההפעלה — רמז לאפשרות להגביל שחיקה ורעילות בלי לנטרל את התאים לצמיתות.
מה משמעות הדבר לתרפיות עתידיות
ללא מומחיות פרטנית, ניתן לחשוב על CRABs ככלי כיוונון עוצמה גנטי ומדויק לאותות סידן. על‑ידי פגיעה בידית המדויקת שבין STIM ל‑ORAI, הם סוגרים מסלול כניסה מרכזי לסידן מבלי להפריע ללא הבחנה לתעלות או קולטים שמעליו. העבודה מדגימה שאמצעים אלה יכולים לתקן מאפיינים דמויי‑מחלה בדג הזברה, לנתח רשתות איתות מורכבות בתאים ולמודול תאים חיסוניים מהונדסים בצורה מתוכנתת. למרות שעדיין קיימים אתגרים — כגון אספקת הגנים בבטחה והימנעות מחסימה ממושכת מופרזת ברקמות בריאות — המחקר מציב פלטפורמה גמישה שעשויה בסופו של דבר לסייע בטיפול בהפרעות נדירות של תעלות סידן ולדייק תרפיות עוצמתיות אך עדינות כמו תאי CAR‑T.
ציטוט: Liu, X., Ali, S., Lan, TH. et al. Engineering of genetically encoded programmable calcium channel inhibitory binders. Nat Commun 17, 3472 (2026). https://doi.org/10.1038/s41467-026-71769-2
מילות מפתח: אותות סידן, תעלות CRAC, אופטוגנטיקה, כימוגנטיקה, תאי CAR‑T