Clear Sky Science · sv
Ingenjörskonst för genetiskt kodade, programmerbara hämmare av kalciumkanaler
Sänka cellernas volymreglage
Många av våra celler förlitar sig på små kalciumutbrott för att avgöra när de ska röra sig, dela sig eller sätta igång en immunattack. När denna kalciumsignalering går för hög kan den driva sällsynta genetiska sjukdomar, kronisk inflammation och till och med begränsa kraften hos cancerbekämpande T‑celler. Den här studien introducerar en uppsättning skräddarsydda proteiner kallade CRABs som fungerar som programmerbara dämpare på en huvudkanal för kalciuminträde i celler, och öppnar nya möjligheter för både grundforskning och framtida terapier.
Hur celler använder kalcium som en av/på‑brytare
I de flesta icke‑neurala celler är en huvudgenomgång för kalcium en struktur känd som CRAC‑kanalen, bildad av två parter: STIM, som känner av kalciumnivåer i ett internt lagringsutrymme, och ORAI, en por i den yttre cellmembranen. När de interna förråden blir tömda ändrar STIM form, förflyttar sig till regioner där de interna och yttre membranen möts och hakar i ORAI. Detta öppnar kanalen och tillåter kalcium att strömma in och utlösa svar som sträcker sig från kortvarig rörelse till långvariga förändringar i genaktivitet. I immunceller är denna väg avgörande för att aktivera transkriptionsfaktorer som NFAT som slår på gener som behövs för försvar, men om den lämnas okontrollerad kan den driva sjukdom.
När kalciumsignalering går fel
Ärftliga förändringar som permanent vrider STIM eller ORAI till en "på"‑position kan orsaka multisystemsjukdomar, som Stormorken‑syndromet, kännetecknat av lågt antal blodplättar, blödningsproblem, muskelsvaghet och andra besvär. Mildare men kronisk överaktivering av samma väg bidrar till autoimmun sjukdom, cancerprogression och utmattning av konstruerade CAR‑T‑celler som används vid leukemibehandling. Läkemedelsutvecklare har försökt blockera CRAC‑kanaler med små molekyler, men många av dessa föreningar påverkar också andra jonkanaler och organ, vilket leder till biverkningar och stoppad klinisk utveckling. Ett mer specifikt, justerbart och genetiskt målinriktat sätt att tygla CRAC‑aktivitet har saknats.
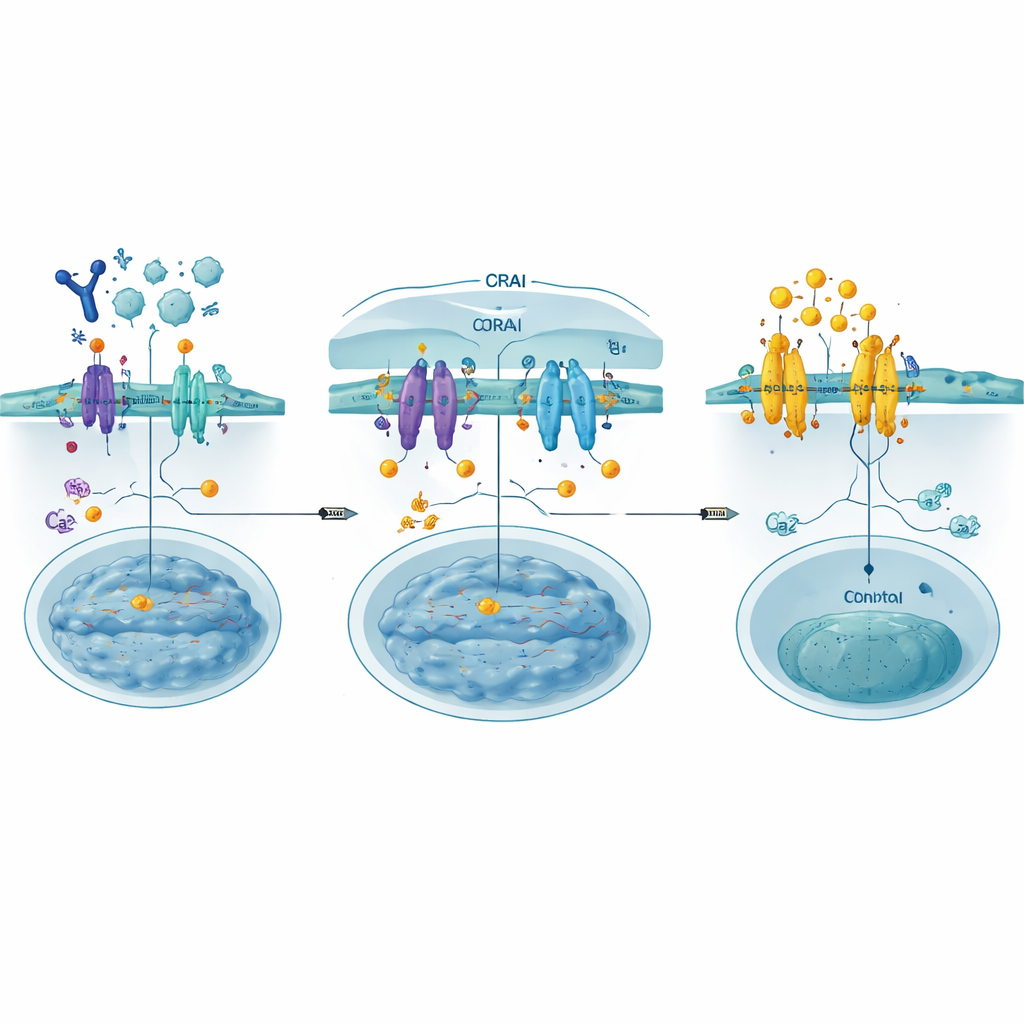
Bygga lockbeten för att blockera porten
Författarna designade CRABs (CRAC channel inhibitory binders) som korta, genetiskt kodade proteinfragment som imiterar en del av ORAI där STIM normalt binder. Förankrade vid cellmembranet fångar dessa lockbeten aktiverad STIM innan den kan haka i riktiga ORAI‑kanaler, och stänger därigenom porten uppströms från kalciumflödet. Genom användning av djup mutational scanning — systematiska tester av hundratals små sekvensändringar — identifierade de en särskilt stark bindare, döpt PM‑CRAB, som kraftigt minskade kalciumintaget och NFAT:s förflyttning in i kärnan i mänskliga celler. Strukturell modellering föreslog att ett enda aminosyrautbyte gör CRAB‑peptiden mer passande i STIM:s bindningsfåra, stabiliserar partnerskapet och förbättrar dess blockerande förmåga.
Från fiskplättar till programmerbara dimrar
För att visa att CRABs fungerar i levande djur använde teamet zebrabläckfiskar (zebrafisk) konstruerade för att bära en sjukdomsframkallande STIM1‑mutation som håller CRAC‑kanaler öppna och efterliknar Stormorken‑syndromet. Dessa fiskar har markant färre fluorescerande märkta trombocyter (plättliknande celler). När PM‑CRAB samexprimerades återhämtade produktionen av dessa celler sig i hög grad, vilket indikerar att lockbetet kunde motverka den skadliga kalciumöverbelastningen. Forskarna skapade sedan en familj av CRAB‑varianter med olika styrkor: monomerer, dimerer och tetramerer som successivt ökade kanalhämningen. Avgörande nog byggde de även versioner som kan slås på med blått ljus (Opto‑CRAB) eller med små molekyler såsom rapamycin eller en icke‑immunosuppressiv analog (Chemo‑CRAB). I odlade celler gjorde dessa strömbrytare det möjligt att snabbt och reversibelt styra kalciumintaget och NFAT‑aktiveringen beroende på ljus eller läkemedelstiming.
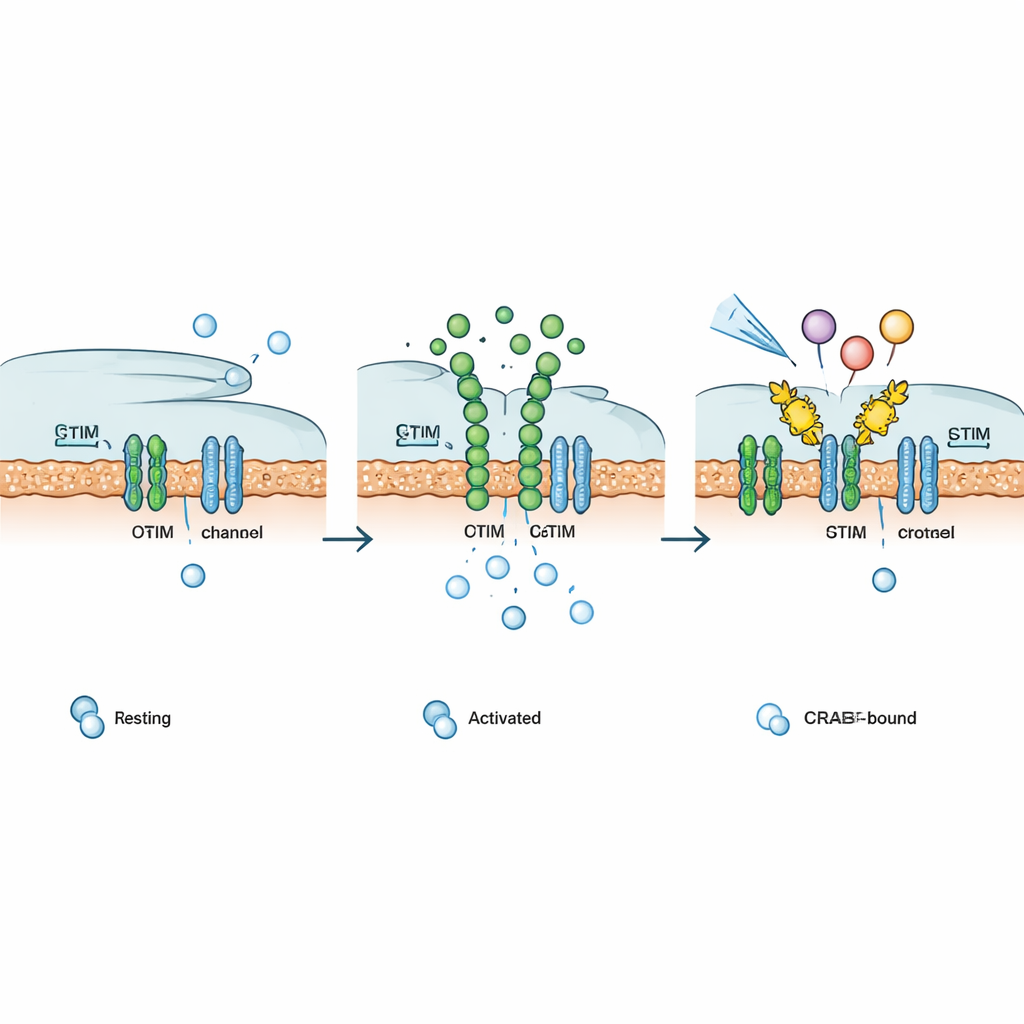
Justera immuna och signalvägar vid behov
Eftersom många ytreceptorer i kroppen — såsom vissa hormon‑, tillväxtfaktor‑ och G‑proteinkopplade receptorer — i slutändan förlitar sig på CRAC‑kanaler för att upprätthålla kalciumsignaler, testade författarna om Chemo‑CRAB kunde ingripa över olika vägar. När den aktiverades av sin kemiska utlösare dämpade Chemo‑CRAB kalciumsvar drivna av konstruerade ljus‑ eller koffein‑aktiverade kalciumaktuatorer, syntetiska och naturliga tillväxtfaktorreceptorer och flera olika G‑proteinkopplade receptorer. I T‑celler avskaffade ett membranförankrat CRAB CRAC‑strömmar och sänkte kraftigt NFAT‑beroende genaktivitet. I mänskliga CAR‑T‑celler som riktar sig mot CD19‑positiva cancerceller minskade PM‑CRAB frisättningen av viktiga inflammatoriska cytokiner, medan Chemo‑CRAB möjliggjorde dosberoende, behovsstyrd dämpning av aktivering, vilket antyder ett sätt att begränsa utmattning och toxicitet utan att permanenta inaktivera cellerna.
Vad detta kan betyda för framtida terapier
För icke‑specialisten kan CRABs betraktas som mycket specifika, genetiskt kodade volymreglage för kalciumsignalering. Genom att verka vid den precisa handskakningen mellan STIM och ORAI stänger de ner en central väg för kalciuminträde utan att brett störa andra kanaler eller uppströms receptorers funktion. Arbetet visar att dessa verktyg kan korrigera sjukdomsliknande drag i zebrafisk, dissekera komplexa signalnätverk i celler och modulera konstruerade immunceller på ett programmerbart sätt. Medan utmaningar kvarstår — såsom att säkert leverera generna och undvika överdriven långtidsblockad i friska vävnader — lägger studien fram en mångsidig plattform som så småningom skulle kunna hjälpa till att behandla sällsynta kalciumkanalsjukdomar och finjustera kraftfulla men känsliga terapier som CAR‑T‑celler.
Citering: Liu, X., Ali, S., Lan, TH. et al. Engineering of genetically encoded programmable calcium channel inhibitory binders. Nat Commun 17, 3472 (2026). https://doi.org/10.1038/s41467-026-71769-2
Nyckelord: kalciumsignalering, CRAC‑kanaler, optogenetik, kemogenetik, CAR‑T‑celler