Clear Sky Science · it
Progettazione di inibitori programmabili geneticamente codificati per canali del calcio
Abbassare le manopole del volume cellulare
Molte delle nostre cellule fanno affidamento su brevi esplosioni di calcio per decidere quando muoversi, dividersi o scatenare una risposta immunitaria. Quando questa segnalazione del calcio è troppo intensa, può alimentare malattie genetiche rare, infiammazione cronica e persino limitare l’efficacia delle cellule T antitumorali. Questo studio introduce una serie di strumenti proteici su misura chiamati CRAB che agiscono come smorzatori programmabili su una via principale di ingresso del calcio nelle cellule, aprendo nuove possibilità sia per la ricerca di base sia per future terapie.
Come le cellule usano il calcio come interruttore
Nella maggior parte delle cellule non neuronali, una porta principale per il calcio è una struttura nota come canale CRAC, formata da due partner: STIM, che rileva i livelli di calcio all’interno di un compartimento di stoccaggio interno, e ORAI, un poro nella membrana cellulare esterna. Quando le riserve interne si esauriscono, STIM cambia forma, si sposta verso le regioni in cui le membrane interne ed esterne sono a contatto e si aggancia a ORAI. Questo apre il canale, permettendo al calcio di affluire e attivare risposte che vanno dal movimento a breve termine a cambiamenti duraturi nell’attività genica. Nelle cellule immunitarie, questa via è fondamentale per attivare fattori di trascrizione come NFAT che accendono i geni necessari per la difesa, ma se non controllata può causare patologia.
Quando la segnalazione del calcio si guasta
Variazioni ereditarie che mantengono permanentemente STIM o ORAI in una posizione «accesa» possono causare disordini multisistemici, come la sindrome di Stormorken, caratterizzata da bassa conta piastrinica, problemi di sanguinamento, debolezza muscolare e altri sintomi. Una sovraattivazione più lieve ma cronica della stessa via contribuisce all’autoimmunità, alla progressione del cancro e all’esaurimento delle cellule CAR‑T ingegnerizzate impiegate nella terapia della leucemia. Gli sviluppatori di farmaci hanno cercato di bloccare i canali CRAC con piccole molecole, ma molti di questi composti colpiscono anche altri canali ionici e organi, causando effetti collaterali e rallentando il progresso clinico. Mancava un modo più specifico, regolabile e geneticamente mirato per limitare l’attività CRAC.
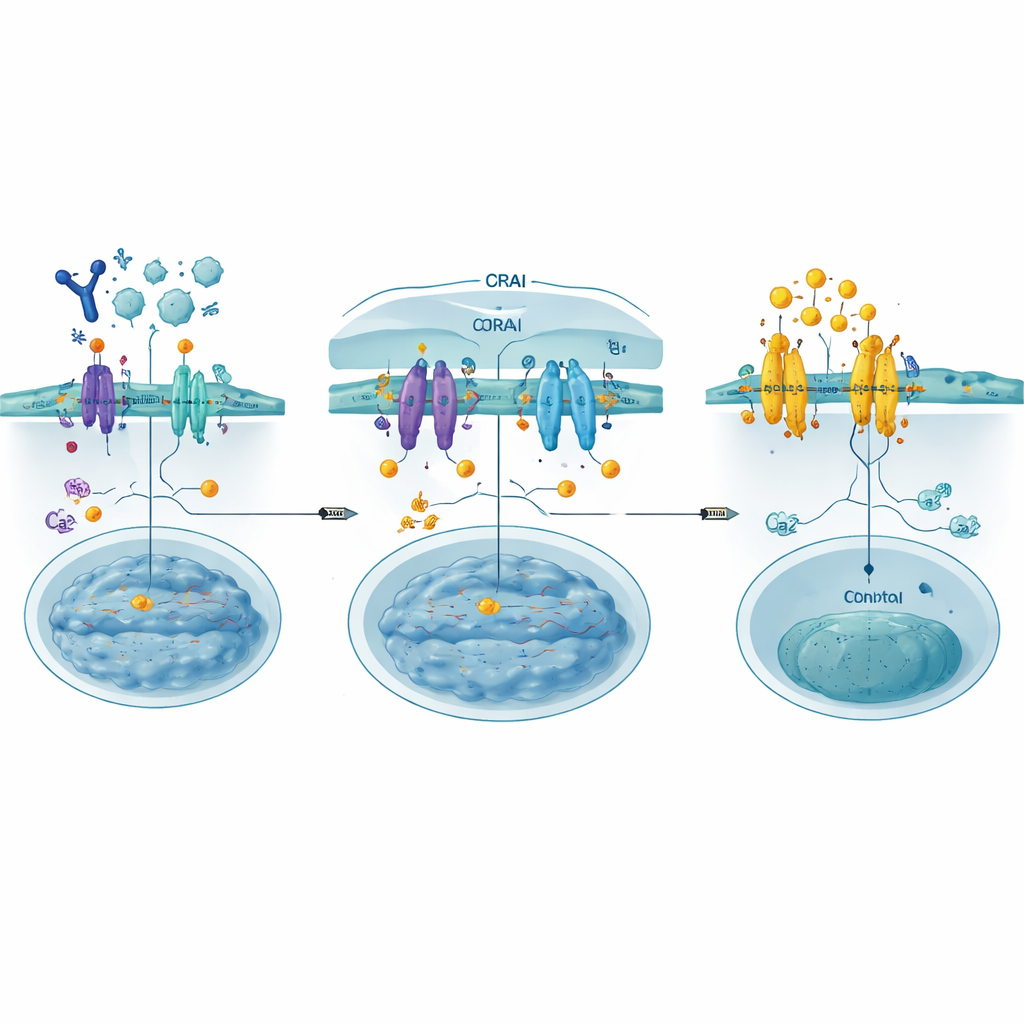
Costruire esche per bloccare il cancello
Gli autori hanno progettato i CRAB (CRAC channel inhibitory binders) come brevi frammenti proteici geneticamente codificati che imitano una parte di ORAI dove STIM normalmente si lega. Ancorate alla membrana cellulare, queste esche catturano STIM attivato prima che possa agganciarsi ai canali ORAI reali, chiudendo di fatto la porta a monte del flusso di calcio. Usando lo scanning mutazionale profondo — testando sistematicamente centinaia di piccole variazioni di sequenza — hanno identificato un legante particolarmente forte, chiamato PM‑CRAB, che riduceva potentemente l’ingresso di calcio e il trasporto di NFAT nel nucleo nelle cellule umane. La modellazione strutturale ha suggerito che una singola sostituzione di un amminoacido rende il peptide CRAB più aderente nella cavità di legame di STIM, stabilizzando l’interazione e migliorando la capacità di blocco.
Dalle piastrine di pesce a dimmer programmabili
Per dimostrare che i CRAB funzionano in organismi viventi, il team ha usato zebrafish ingegnerizzati per portare una mutazione patogena di STIM1 che mantiene i canali CRAC aperti e imita la sindrome di Stormorken. Questi pesci mostrano un numero marcatamente inferiore di trombociti (cellule simili alle piastrine) etichettati con fluorescenza. Quando PM‑CRAB è stato co‑espresso, la produzione di queste cellule si è in gran parte recuperata, indicando che l’esca poteva contrastare il sovraccarico di calcio dannoso. I ricercatori hanno poi creato una famiglia di varianti CRAB con forze diverse: monomeri, dimeri e tetrameri che aumentavano progressivamente l’inibizione del canale. Cruciale, hanno anche realizzato versioni che possono essere attivate dalla luce blu (Opto‑CRAB) o da piccole molecole come la rapamicina o un analogo non immunosoppressivo (Chemo‑CRAB). Nelle colture cellulari, questi interruttori hanno permesso un controllo rapido e reversibile dell’ingresso di calcio e dell’attivazione di NFAT in risposta al tempo di esposizione alla luce o al farmaco.
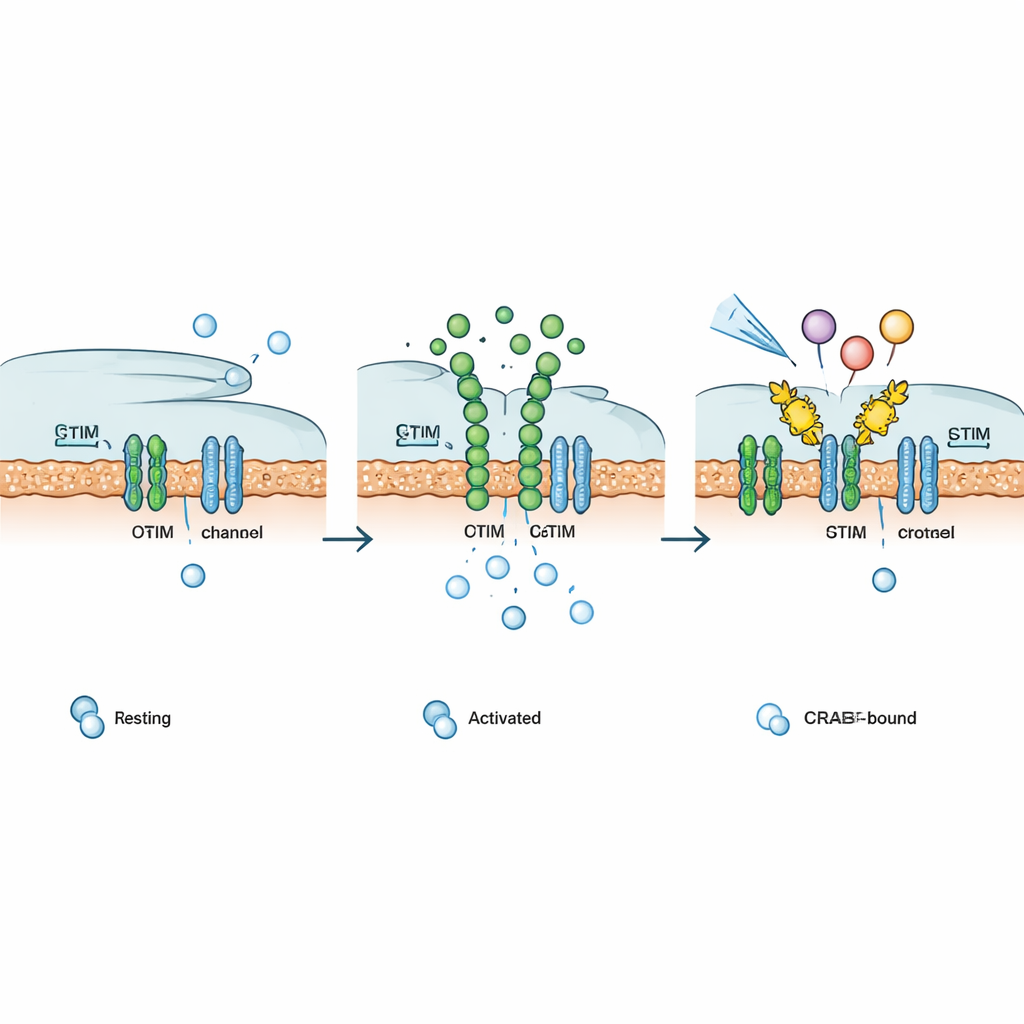
Regolare su richiesta vie immunitarie e di segnalazione
Poiché molti recettori di superficie nel corpo — come alcuni recettori ormonali, dei fattori di crescita e accoppiati a proteine G — si affidano infine ai canali CRAC per sostenere i segnali di calcio, gli autori hanno testato se Chemo‑CRAB potesse intervenire in percorsi diversi. Una volta attivato dal suo trigger chimico, Chemo‑CRAB ha attenuato le risposte di calcio indotte da attuatori di calcio ingegnerizzati sensibili alla luce o alla caffeina, recettori di fattori di crescita sintetici e naturali, e diversi recettori accoppiati a proteine G. Nelle cellule T, un CRAB ancorato alla membrana ha abolito le correnti CRAC e ridotto drasticamente l’attività genica dipendente da NFAT. Nelle cellule CAR‑T umane dirette contro cellule tumorali CD19‑positive, PM‑CRAB ha ridotto il rilascio di citochine infiammatorie chiave, mentre Chemo‑CRAB ha permesso un attenuazione dose‑dipendente e attivabile su richiesta, suggerendo un modo per limitare esaurimento e tossicità senza disabilitare permanentemente le cellule.
Cosa potrebbe significare per le terapie future
Per un non specialista, i CRAB possono essere pensati come manopole del volume altamente specifiche e geneticamente codificate per la segnalazione del calcio. Agendo sulla stretta interazione tra STIM e ORAI, interrompono una via centrale di ingresso del calcio senza interferire in modo esteso con altri canali o recettori a monte. Il lavoro dimostra che questi strumenti possono correggere caratteristiche simili a patologie negli zebrafish, analizzare reti di segnalazione complesse nelle cellule e modulare cellule immunitarie ingegnerizzate in modo programmabile. Pur restando sfide — come la consegna sicura dei geni ed evitare un blocco eccessivo a lungo termine nei tessuti sani — lo studio propone una piattaforma versatile che potrebbe in futuro aiutare a trattare disturbi rari dei canali del calcio e a perfezionare terapie potenti ma delicate come le cellule CAR‑T.
Citazione: Liu, X., Ali, S., Lan, TH. et al. Engineering of genetically encoded programmable calcium channel inhibitory binders. Nat Commun 17, 3472 (2026). https://doi.org/10.1038/s41467-026-71769-2
Parole chiave: segnalazione del calcio, canali CRAC, optogenetica, chemogenetica, cellule CAR‑T