Clear Sky Science · pt
Engenharia de ligantes programáveis geneticamente codificados que inibem canais de cálcio
Diminuindo os botões de volume celulares
Muitas de nossas células dependem de pequenos surtos de cálcio para decidir quando se mover, dividir ou desencadear um ataque imune. Quando essa sinalização por cálcio fica excessiva, pode alimentar doenças genéticas raras, inflamação crônica e até limitar a potência de células T anti‑câncer. Este estudo apresenta um conjunto de ferramentas proteicas sob medida chamadas CRABs que atuam como amortecedores programáveis em uma via principal de entrada de cálcio nas células, abrindo novas possibilidades tanto para pesquisa básica quanto para futuras terapias.
Como as células usam o cálcio como um interruptor liga‑desliga
Na maioria das células não neurais, uma porta principal para o cálcio é uma estrutura conhecida como canal CRAC, formada por dois parceiros: STIM, que detecta os níveis de cálcio em um compartimento interno de armazenamento, e ORAI, um poro na membrana plasmática. Quando os estoques internos ficam baixos, o STIM muda de forma, desloca‑se para regiões onde as membranas internas e externas se aproximam e se liga ao ORAI. Isso abre o canal, permitindo que o cálcio entre em massa e desencadeie respostas que vão do movimento de curto prazo a mudanças de longa duração na atividade gênica. Em células do sistema imune, essa via é vital para ativar fatores de transcrição como NFAT, que ligam genes necessários para a defesa, mas se deixada sem controle pode promover doenças.
Quando a sinalização por cálcio falha
Alterações herdadas que colocam permanentemente o STIM ou o ORAI na posição “ligada” podem causar distúrbios multissistêmicos, como a síndrome de Stormorken, caracterizada por baixa contagem de plaquetas, problemas de sangramento, fraqueza muscular e outras complicações. Uma ativação crônica mais branda da mesma via contribui para doenças autoimunes, progressão do câncer e exaustão de células CAR‑T desenvolvidas para terapias contra leucemia. Desenvolvedores de fármacos tentaram bloquear canais CRAC com pequenas moléculas, mas muitos desses compostos afetam outros canais iônicos e órgãos, levando a efeitos colaterais e estagnação no progresso clínico. Faltava um modo mais específico, ajustável e geneticamente direcionado de controlar a atividade dos CRAC.
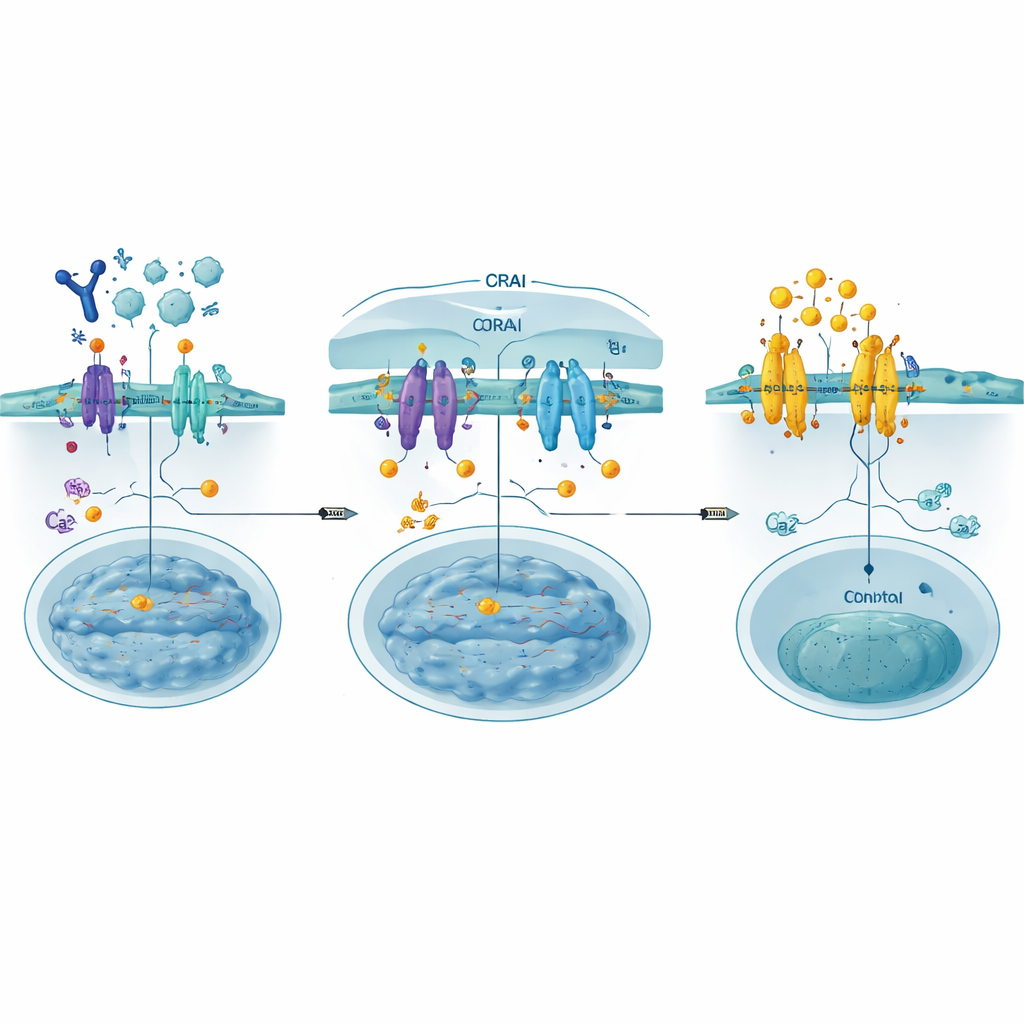
Construindo engodos para bloquear a entrada
Os autores projetaram os CRABs (ligantes inibitórios do canal CRAC) como fragmentos proteicos curtos e geneticamente codificados que imitam a região do ORAI onde o STIM normalmente se liga. Ancorados na membrana celular, esses engodos interceptam o STIM ativado antes que ele consiga se prender aos canais ORAI reais, fechando efetivamente a porta a montante do fluxo de cálcio. Usando varredura mutacional profunda — testando sistematicamente centenas de pequenas mudanças de sequência — eles identificaram um ligante particularmente eficaz, chamado PM‑CRAB, que reduziu de forma potente a entrada de cálcio e o deslocamento do NFAT para o núcleo em células humanas. Modelagem estrutural sugeriu que a troca de um único aminoácido faz o peptídeo CRAB encaixar‑se mais firmemente na fenda de ligação do STIM, estabilizando a associação e aprimorando seu poder de bloqueio.
De plaquetas de peixe a dimmers programáveis
Para demonstrar que os CRABs funcionam em animais vivos, a equipe usou zebrafish modificados para carregar uma mutação no STIM1 que mantém os canais CRAC abertos e imita a síndrome de Stormorken. Esses peixes apresentam um número marcadamente menor de trombócitos (células semelhantes a plaquetas) rotuladas por fluorescência. Quando o PM‑CRAB foi coexpressado, a produção dessas células recuperou‑se em grande parte, indicando que o engodo pôde contrariar a sobrecarga de cálcio prejudicial. Os pesquisadores então criaram uma família de variantes CRAB com diferentes potências: monômeros, dímeros e tetrâmeros que aumentaram progressivamente a inibição do canal. Crucialmente, também construíram versões que podem ser ativadas por luz azul (Opto‑CRAB) ou por pequenas moléculas como rapamicina ou um análogo não imunossupressor (Chemo‑CRAB). Em células cultivadas, esses interruptores permitiram controle rápido e reversível da entrada de cálcio e da ativação do NFAT em resposta ao timing da luz ou do fármaco.
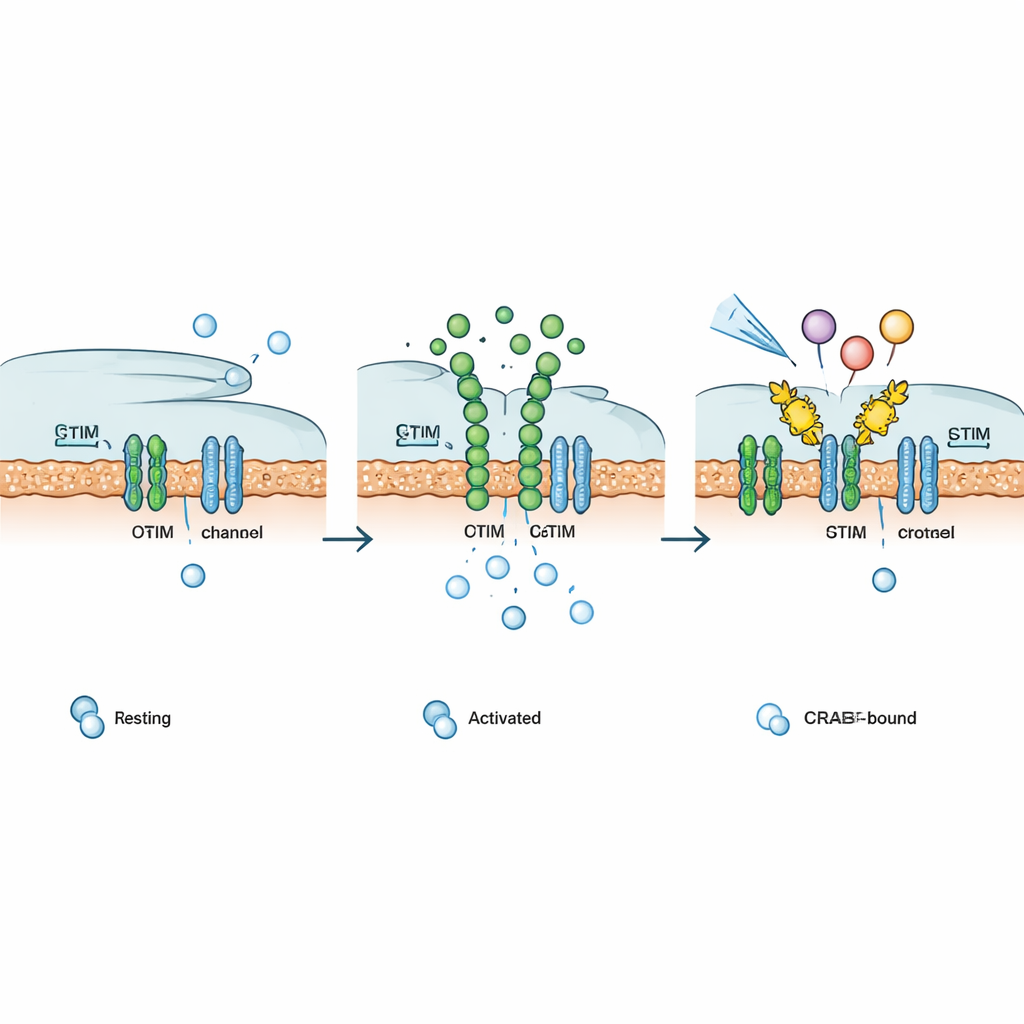
Ajustando vias imunes e de sinalização sob demanda
Como muitos receptores de superfície no organismo — como certos receptores de hormônio, fatores de crescimento e receptores acoplados a proteínas G — dependem em última análise dos canais CRAC para sustentar sinais de cálcio, os autores testaram se o Chemo‑CRAB poderia intervir em vias diversas. Uma vez ativado pelo seu gatilho químico, o Chemo‑CRAB atenuou respostas de cálcio impulsionadas por atuadores de cálcio sensíveis à luz ou à cafeína, receptores de fatores de crescimento sintéticos e naturais, e vários receptores acoplados a proteínas G distintos. Em células T, um CRAB ancorado na membrana aboliu correntes CRAC e reduziu drasticamente a atividade gênica dependente de NFAT. Em células CAR‑T humanas direcionadas a células cancerígenas CD19‑positivas, o PM‑CRAB diminuiu a liberação de citocinas inflamatórias chave, enquanto o Chemo‑CRAB permitiu atenuação dependente da dose e sob demanda da ativação, sugerindo um modo de limitar exaustão e toxicidade sem desativar permanentemente as células.
O que isso pode significar para terapias futuras
Para um não especialista, os CRABs podem ser vistos como botões de volume geneticamente codificados e altamente específicos para a sinalização por cálcio. Ao atuarem no aperto preciso entre STIM e ORAI, eles interrompem uma rota central de entrada de cálcio sem interferir amplamente em outros canais ou receptores a montante. O trabalho demonstra que essas ferramentas podem corrigir traços semelhantes a doenças em zebrafish, dissecar redes de sinalização complexas em células e modular células imunes engenheiradas de forma programável. Embora desafios permaneçam — como entregar os genes de forma segura e evitar bloqueios excessivos e prolongados em tecidos saudáveis — o estudo apresenta uma plataforma versátil que poderia, no futuro, ajudar a tratar distúrbios raros de canais de cálcio e a ajustar terapias poderosas porém delicadas, como as células CAR‑T.
Citação: Liu, X., Ali, S., Lan, TH. et al. Engineering of genetically encoded programmable calcium channel inhibitory binders. Nat Commun 17, 3472 (2026). https://doi.org/10.1038/s41467-026-71769-2
Palavras-chave: sinalização por cálcio, canais CRAC, optogenética, quimiogenética, células CAR-T