Clear Sky Science · es
Ingeniería de inhibidores programables de canales de calcio codificados genéticamente
Bajando los mandos de volumen celulares
Muchas de nuestras células dependen de pequeños impulsos de calcio para decidir cuándo moverse, dividirse o desencadenar una respuesta inmune. Cuando esta señalización por calcio se descontrola, puede alimentar enfermedades genéticas raras, inflamación crónica e incluso limitar la potencia de las células T que combaten el cáncer. Este estudio presenta un conjunto de herramientas proteicas a medida llamadas CRABs que actúan como amortiguadores programables sobre una vía principal de entrada de calcio en las células, abriendo nuevas posibilidades tanto para la investigación básica como para futuras terapias.
Cómo las células usan el calcio como un interruptor de encendido/apagado
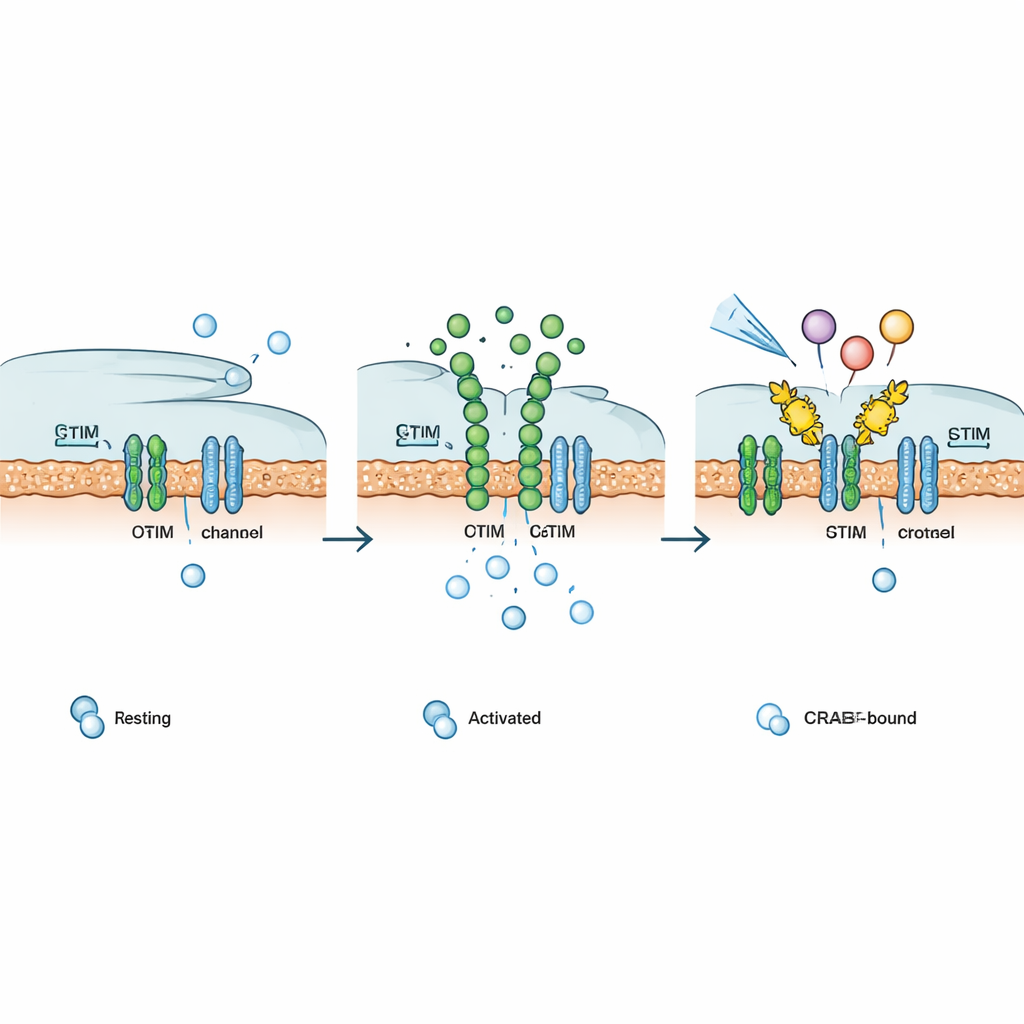
En la mayoría de las células no neuronales, una puerta principal para el calcio es una estructura conocida como el canal CRAC, formada por dos socios: STIM, que detecta los niveles de calcio en un compartimento interno de almacenamiento, y ORAI, un poro en la membrana plasmática. Cuando las reservas internas se agotan, STIM cambia de forma, se desplaza a regiones donde las membranas internas y externas se aproximan y se enlaza a ORAI. Esto abre el canal, permitiendo que entre calcio y desencadene respuestas que van desde movimientos a corto plazo hasta cambios a largo plazo en la actividad génica. En las células inmunitarias, esta vía es vital para activar factores de transcripción como NFAT que encienden genes necesarios para la defensa, pero si queda sin control puede impulsar la enfermedad.
Cuando la señalización por calcio falla
Alteraciones hereditarias que ponen de forma permanente a STIM u ORAI en una posición de “encendido” pueden causar trastornos multisistémicos, como el síndrome de Stormorken, caracterizado por bajo recuento de plaquetas, problemas de hemorragia, debilidad muscular y otras complicaciones. Una sobreactivación crónica más leve de la misma vía contribuye a enfermedades autoinmunes, progresión del cáncer y agotamiento de las células CAR‑T diseñadas para terapias contra la leucemia. Los desarrolladores de fármacos han intentado bloquear los canales CRAC con pequeñas moléculas, pero muchos de estos compuestos afectan a otros canales iónicos y órganos, provocando efectos secundarios y frenando el avance clínico. Faltaba una forma más específica, ajustable y dirigida genéticamente para controlar la actividad de CRAC.
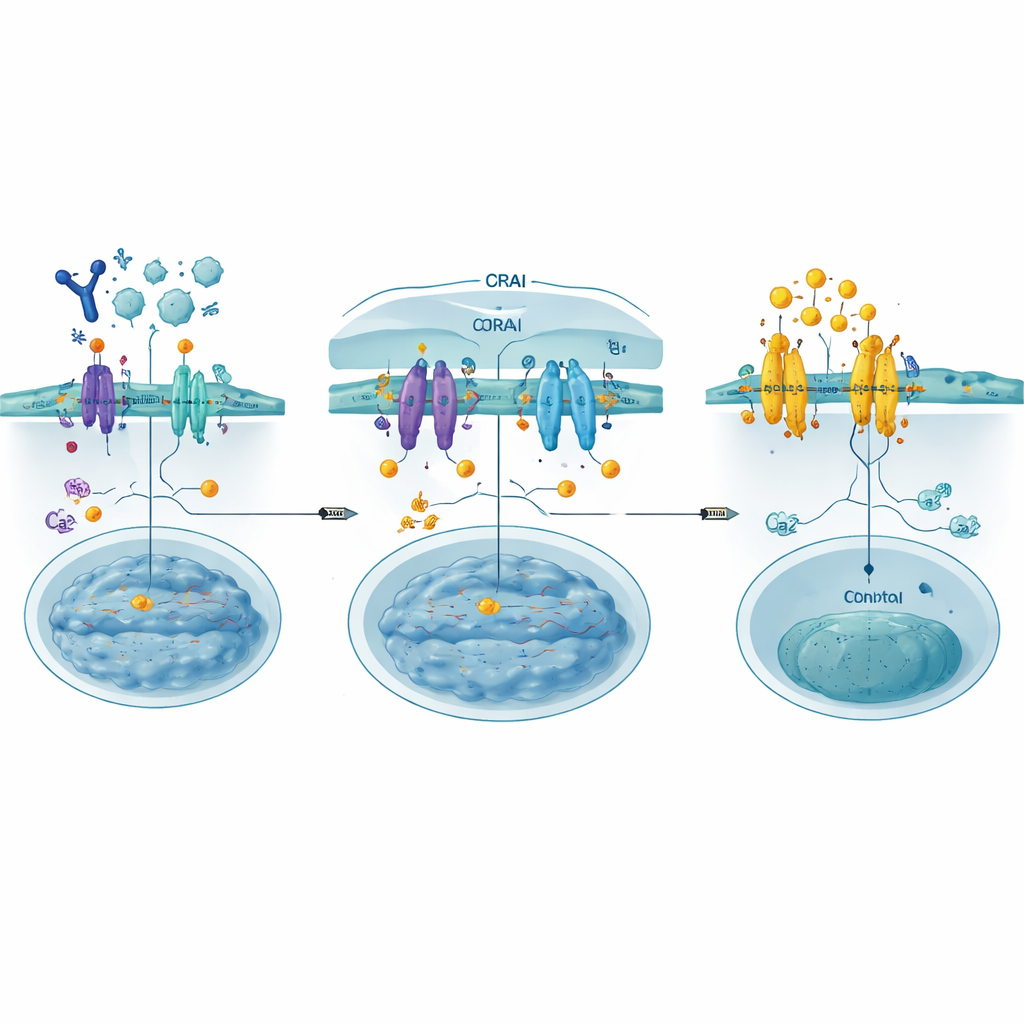
Construir señuelos para bloquear la puerta
Los autores diseñaron los CRABs (CRAC channel inhibitory binders) como fragmentos proteicos cortos codificados genéticamente que imitan la parte de ORAI donde STIM normalmente se une. Anclados en la membrana celular, estos señuelos atrapan a STIM activado antes de que pueda engancharse a los canales ORAI reales, cerrando efectivamente la puerta aguas arriba del flujo de calcio. Mediante un barrido mutacional profundo —probando sistemáticamente cientos de pequeños cambios de secuencia— identificaron un ligando particularmente potente, denominado PM‑CRAB, que redujo de forma notable la entrada de calcio y el movimiento de NFAT al núcleo en células humanas. El modelado estructural sugirió que un solo intercambio de aminoácido hace que el péptido CRAB encaje con mayor precisión en la hendidura de unión de STIM, estabilizando la interacción y mejorando su capacidad de bloqueo.
De plaquetas de pez a atenuadores programables
Para demostrar que los CRABs funcionan en animales vivos, el equipo utilizó peces cebra modificados para portar una mutación patógena de STIM1 que mantiene los canales CRAC abiertos y reproduce el síndrome de Stormorken. Estos peces presentan muchas menos trombocitos (células tipo plaqueta) marcados con fluorescencia. Cuando se coexpresó PM‑CRAB, la producción de estas células se recuperó en gran medida, lo que indica que el señuelo pudo contrarrestar la sobrecarga de calcio dañina. Los investigadores crearon luego una familia de variantes CRAB con distintas potencias: monómeros, dímeros y tetrámeros que aumentaron progresivamente la inhibición del canal. De manera crucial, también desarrollaron versiones que pueden activarse con luz azul (Opto‑CRAB) o por pequeñas moléculas como la rapamicina o un análogo no inmunosupresor (Chemo‑CRAB). En células en cultivo, estos conmutadores permitieron un control rápido y reversible de la entrada de calcio y de la activación de NFAT en respuesta al tiempo de administración de la luz o del fármaco.
Ajustar vías inmunitarias y de señalización bajo demanda
Dado que muchos receptores de superficie en el organismo —como ciertos receptores hormonales, de factores de crecimiento y acoplados a proteínas G— dependen finalmente de los canales CRAC para sostener las señales de calcio, los autores probaron si Chemo‑CRAB podía intervenir en diversas vías. Una vez activado por su disparador químico, Chemo‑CRAB atenuó las respuestas de calcio impulsadas por actuadores de calcio activados por luz o por cafeína, receptores sintéticos y naturales de factores de crecimiento y varios receptores acoplados a proteínas G distintos. En células T, un CRAB anclado a la membrana abolió las corrientes CRAC y redujo drásticamente la actividad génica dependiente de NFAT. En células CAR‑T humanas dirigidas contra células cancerosas positivas para CD19, PM‑CRAB disminuyó la liberación de citocinas inflamatorias clave, mientras que Chemo‑CRAB permitió una atenuación dependiente de dosis y bajo demanda de la activación, sugiriendo una manera de limitar el agotamiento y la toxicidad sin desactivar permanentemente las células.
Qué podría significar esto para futuras terapias
Para un no especialista, los CRABs pueden concebirse como perillas de volumen genéticamente codificadas y muy específicas para la señalización por calcio. Al actuar en el apretón preciso entre STIM y ORAI, cierran una vía central de entrada de calcio sin interferir de forma amplia con otros canales o receptores aguas arriba. El trabajo demuestra que estas herramientas pueden corregir rasgos similares a la enfermedad en peces cebra, disecar redes de señalización complejas en células y modular células inmunitarias diseñadas de forma programable. Aunque quedan desafíos —como la entrega segura de los genes y evitar un bloqueo excesivo a largo plazo en tejidos sanos—, el estudio establece una plataforma versátil que eventualmente podría ayudar a tratar trastornos raros de canales de calcio y a afinar terapias potentes pero delicadas como las células CAR‑T.
Cita: Liu, X., Ali, S., Lan, TH. et al. Engineering of genetically encoded programmable calcium channel inhibitory binders. Nat Commun 17, 3472 (2026). https://doi.org/10.1038/s41467-026-71769-2
Palabras clave: señalización por calcio, canales CRAC, quimio-genética, CART cells