Clear Sky Science · fr
Conception d’inhibiteurs programmables des canaux calciques codés génétiquement
Rabaisser les boutons de volume cellulaires
Beaucoup de nos cellules s’appuient sur de petites impulsions de calcium pour décider quand se déplacer, se diviser ou déclencher une attaque immunitaire. Lorsque cette signalisation calcique s’emballe, elle peut alimenter des maladies génétiques rares, une inflammation chronique et même limiter l’efficacité des lymphocytes T antitumoraux. Cette étude présente un ensemble d’outils protéiques sur mesure, appelés CRABs, qui agissent comme des amortisseurs programmables sur une voie majeure d’entrée du calcium dans les cellules, ouvrant de nouvelles possibilités pour la recherche fondamentale et des thérapies futures.
Comment les cellules utilisent le calcium comme interrupteur
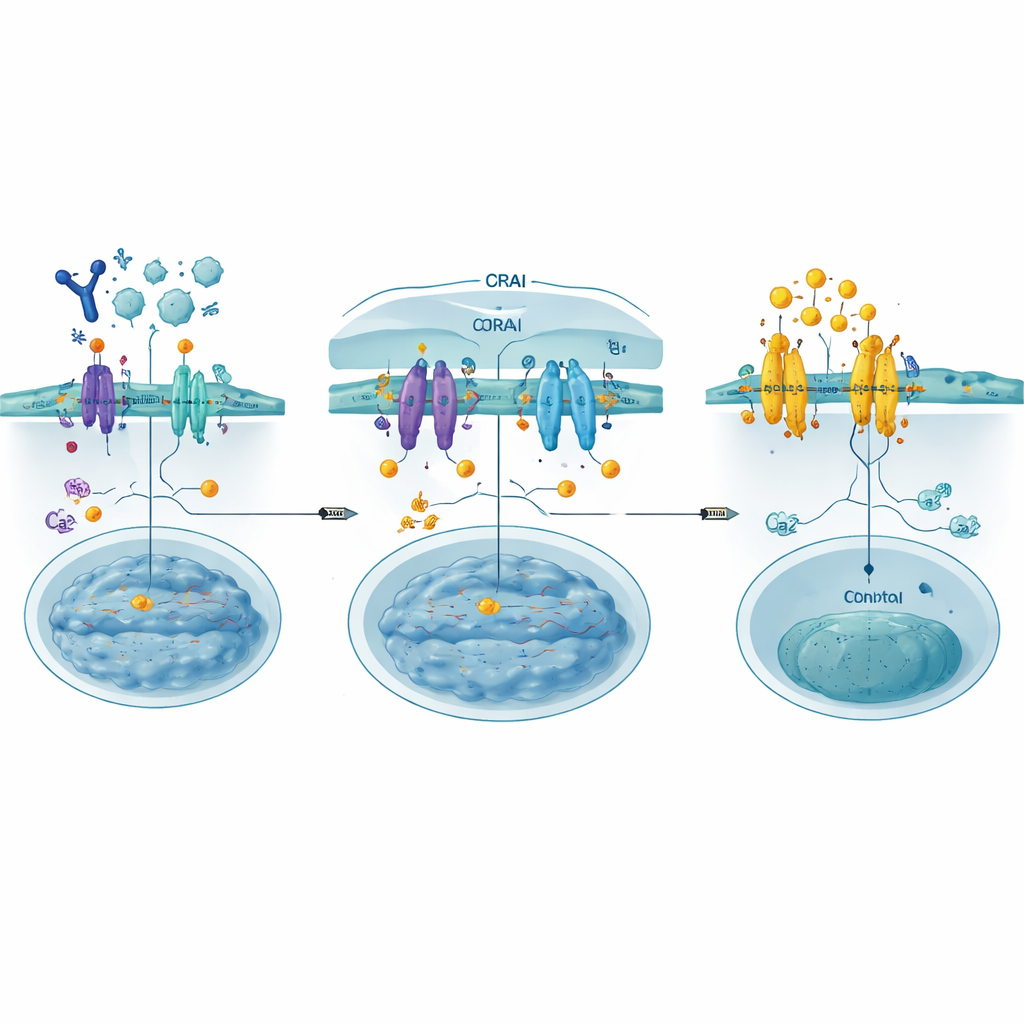
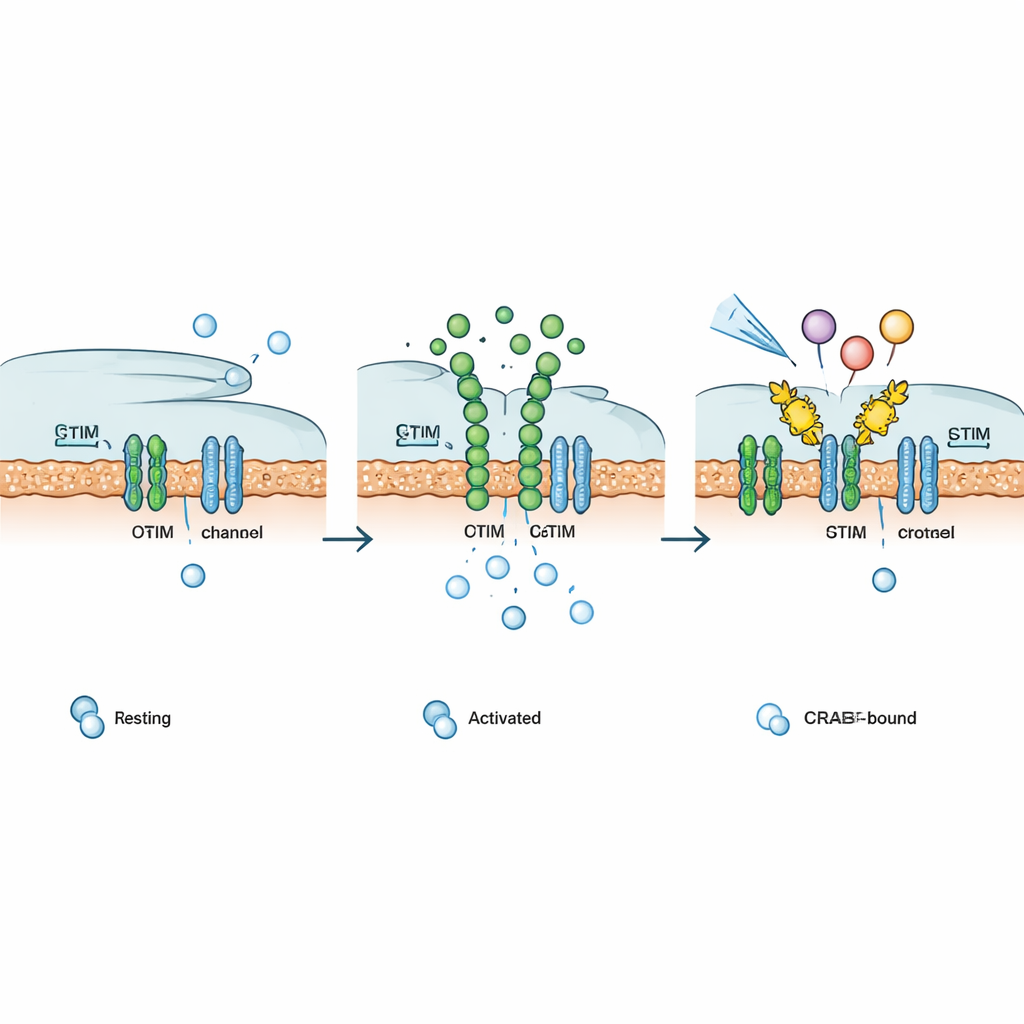
Dans la plupart des cellules non nerveuses, une porte principale pour le calcium est une structure connue sous le nom de canal CRAC, formée par deux partenaires : STIM, qui détecte les niveaux de calcium dans une réserve interne, et ORAI, un pore dans la membrane plasmique. Lorsque les réserves internes s’épuisent, STIM change de conformation, se déplace vers des régions où membranes interne et externe se mettent en contact, et se fixe à ORAI. Cela ouvre le canal, permettant au calcium d’affluer et de déclencher des réponses allant du mouvement à court terme à des modifications à long terme de l’activité génique. Dans les cellules immunitaires, cette voie est essentielle pour activer des facteurs de transcription tels que NFAT qui allument des gènes nécessaires à la défense, mais si elle n’est pas contrôlée elle peut provoquer des maladies.
Quand la signalisation calcique déraille
Des altérations héréditaires qui maintiennent STIM ou ORAI en position « activée » en permanence peuvent causer des troubles multisystémiques, comme le syndrome de Stormorken, caractérisé par un faible taux de plaquettes, des troubles hémorragiques, une faiblesse musculaire et d’autres problèmes. Une activation chronique mais plus modérée de la même voie contribue aux maladies auto‑immunes, à la progression du cancer et à l’épuisement des cellules CAR‑T conçues pour traiter certaines leucémies. Les laboratoires pharmaceutiques ont tenté de bloquer les canaux CRAC par de petites molécules, mais beaucoup atteignent d’autres canaux ioniques et organes, provoquant des effets indésirables et freinant les progrès cliniques. Il manquait une méthode plus spécifique, modulable et ciblée génétiquement pour maîtriser l’activité des CRAC.
Construire des leurres pour boucher la porte
Les auteurs ont conçu les CRABs (CRAC channel inhibitory binders) comme de courts fragments protéiques codés génétiquement qui imitent la portion d’ORAI où STIM se lie habituellement. Ancrés à la membrane cellulaire, ces leurres captent STIM activé avant qu’il ne puisse se fixer aux véritables canaux ORAI, fermant ainsi la voie en amont du flux calcique. En utilisant le deep mutational scanning — test systématique de centaines de petites variations de séquence — ils ont identifié un liant particulièrement performant, baptisé PM‑CRAB, qui réduisait fortement l’entrée de calcium et le déplacement de NFAT vers le noyau dans des cellules humaines. La modélisation structurale a suggéré qu’un simple échange d’acide aminé permet au peptide CRAB de mieux s’insérer dans la rainure de liaison de STIM, stabilisant l’association et renforçant son pouvoir bloquant.
Des plaquettes de poisson aux variateurs programmables
Pour montrer que les CRABs fonctionnent in vivo, l’équipe a utilisé des poissons zèbres modifiés pour porter une mutation pathogène de STIM1 qui maintient les canaux CRAC ouverts et imite le syndrome de Stormorken. Ces poissons présentent un nombre nettement réduit de thrombocytes (cellules de type plaquette) marqués par fluorescence. Quand PM‑CRAB a été co‑exprimé, la production de ces cellules s’est en grande partie rétablie, indiquant que le leurre pouvait contrer la surcharge calcique nocive. Les chercheurs ont ensuite créé une famille de variantes CRAB de différents niveaux : monomères, dimères et tétramères qui augmentent progressivement l’inhibition des canaux. De façon cruciale, ils ont aussi conçu des versions activables par lumière bleue (Opto‑CRAB) ou par petites molécules telles que la rapamycine ou un analogue non immunosuppresseur (Chemo‑CRAB). Dans des cellules en culture, ces interrupteurs ont permis un contrôle rapide et réversible de l’entrée de calcium et de l’activation de NFAT selon la lumière ou la chronologie d’administration du médicament.
Accorder à la demande voies immunitaires et voies de signalisation
Parce que de nombreux récepteurs de surface — tels que certains récepteurs hormonaux, de facteurs de croissance et couplés aux protéines G — dépendent en fin de compte des canaux CRAC pour soutenir les signaux calciques, les auteurs ont testé si Chemo‑CRAB pouvait intervenir sur des voies diverses. Une fois activé par son déclencheur chimique, Chemo‑CRAB a atténué les réponses calciques induites par des actionneurs calciques activés par la lumière ou par la caféine, des récepteurs de facteurs de croissance synthétiques et naturels, ainsi que plusieurs récepteurs couplés aux protéines G distincts. Dans les lymphocytes T, un CRAB ancré à la membrane abolissait les courants CRAC et réduisait fortement l’activité génique dépendante de NFAT. Dans des cellules CAR‑T humaines ciblant des cellules cancéreuses CD19‑positives, PM‑CRAB a diminué la libération de cytokines inflammatoires clés, tandis que Chemo‑CRAB permettait un affaiblissement dépendant de la dose et activable à la demande, suggérant une manière de limiter l’épuisement et la toxicité sans neutraliser définitivement les cellules.
Ce que cela pourrait signifier pour des thérapies futures
Pour le non‑spécialiste, les CRABs peuvent être considérés comme des boutons de volume génétiquement encodés, très spécifiques, pour la signalisation calcique. En agissant précisément à la poignée de main entre STIM et ORAI, ils ferment une voie centrale d’entrée du calcium sans interférer largement avec d’autres canaux ou récepteurs en amont. Le travail montre que ces outils peuvent corriger des traits de type pathologique chez le poisson zèbre, disséquer des réseaux de signalisation complexes dans les cellules et moduler de manière programmable des cellules immunitaires conçues. Si des défis subsistent — comme la livraison sûre des gènes et l’évitement d’un blocage excessif à long terme dans les tissus sains — l’étude pose une plateforme polyvalente qui pourrait à terme aider à traiter des troubles rares des canaux calciques et à affiner des thérapies puissantes mais délicates comme les CAR‑T.
Citation: Liu, X., Ali, S., Lan, TH. et al. Engineering of genetically encoded programmable calcium channel inhibitory binders. Nat Commun 17, 3472 (2026). https://doi.org/10.1038/s41467-026-71769-2
Mots-clés: signalisation calcique, canaux CRAC, optogénétique, chémogénétique, cellules CAR‑T