Clear Sky Science · tr
Genetik olarak kodlanmış programlanabilir kalsiyum kanal inhibe edici bağlayıcıların mühendisliği
Hücresel Ses Seviyesi Düğmelerini Kısma
Hücrelerimizin birçoğu, ne zaman hareket edecekleri, bölünecekleri veya bağışıklık saldırısını başlatacakları gibi kararlar vermek için küçük kalsiyum patlamalarına güvenir. Bu kalsiyum sinyallemesi aşırı aktifleştiğinde, nadir genetik bozuklukları, kronik iltihabı tetikleyebilir ve hatta kanserle savaşan T hücrelerinin gücünü sınırlayabilir. Bu çalışma, hücrelerdeki başlıca kalsiyum giriş yoluna programlanabilir bir damper gibi davranan CRAB adı verilen özel protein araç setini tanıtarak temel araştırma ve gelecekteki terapiler için yeni olanaklar açıyor.
Hücreler Kalsiyumu Nasıl Açma‑Kapatma Anahtarı Olarak Kullanır
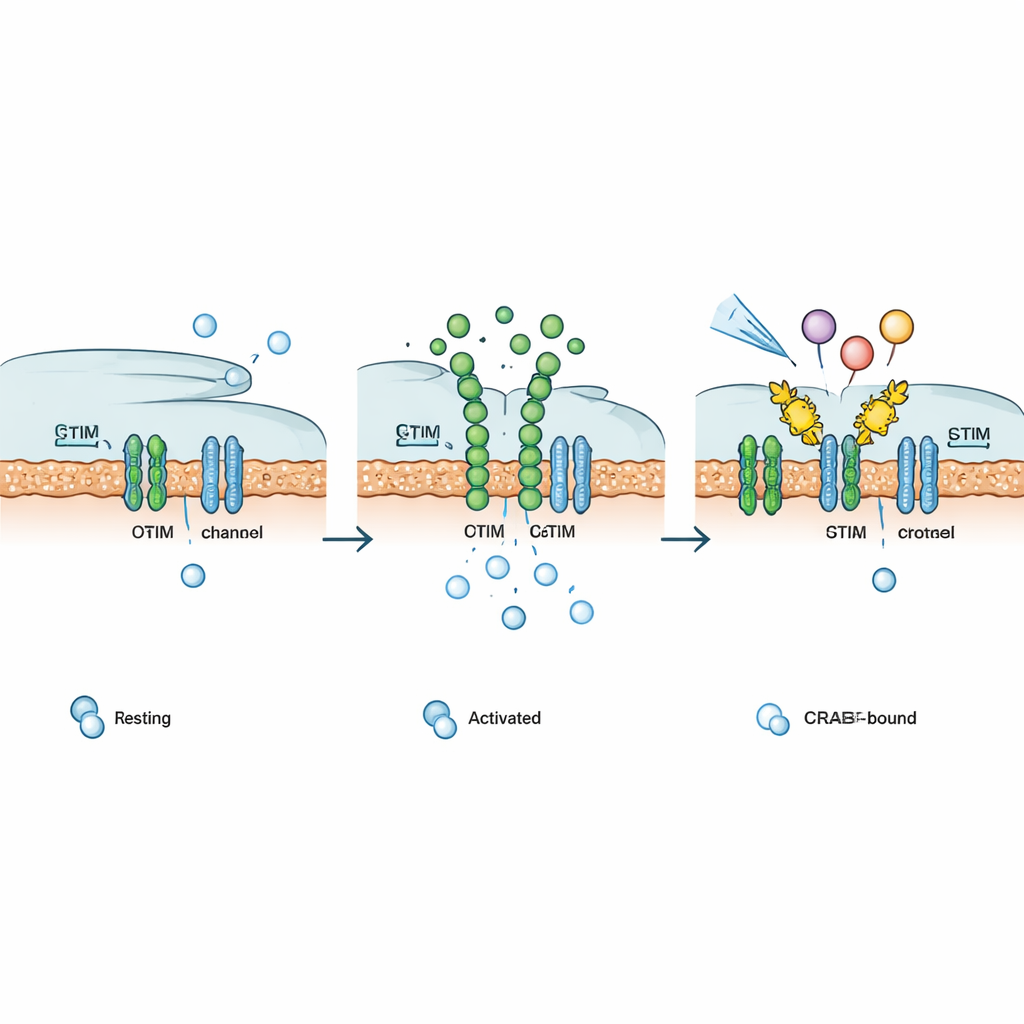
Sinir hücreleri dışındaki çoğu hücrede kalsiyum için ana kapı, CRAC kanalı olarak bilinen yapıdır; bu kanal iki ortağın bir araya gelmesiyle oluşur: iç depolama bölmesindeki kalsiyum seviyesini algılayan STIM ve dış hücre zarı üzerinde bir gözenek olan ORAI. İç depolar azaldığında STIM şekil değiştirir, iç ve dış zarların temas ettiği bölgelere taşınır ve ORAI’ye tutunur. Bu, kanalı açar; kalsiyum hızla içeri girer ve kısa vadeli hareketlerden uzun vadeli gen aktivitesi değişikliklerine kadar çeşitli yanıtları tetikler. Bağışıklık hücrelerinde bu yol, savunma için gerekli genleri açan NFAT gibi transkripsiyon faktörlerini aktifleştirmek için hayati öneme sahiptir, ancak kontrolsüz kaldığında hastalığa yol açabilir.
Kalsiyum Sinyallemesi Yanlış Gittiğinde
STIM veya ORAI’nin kalıcı olarak “açık” konuma kaymasına neden olan kalıtımsal değişiklikler, düşük trombosit sayısı, kanama problemleri, kas zayıflığı gibi belirtilerle karakterize Stormorken sendromu gibi çoklu sistem bozukluklarına yol açabilir. Aynı yolun daha hafif ama kronik aşırı aktivasyonu otoimmün hastalıklara, kanser ilerlemesine ve lösemi tedavisinde kullanılan modifiye CAR‑T hücrelerinin tükenmesine katkıda bulunur. İlaç geliştiriciler CRAC kanallarını küçük moleküllerle bloke etmeye çalıştı; ancak bu bileşiklerin çoğu diğer iyon kanallarını ve organları da etkilediğinden yan etkilere ve klinik ilerlemede duraklamaya neden oldu. CRAC aktivitesini daha özgül, ayarlanabilir ve genetik olarak hedeflenmiş bir şekilde dizginleyecek bir yöntem eksikti.
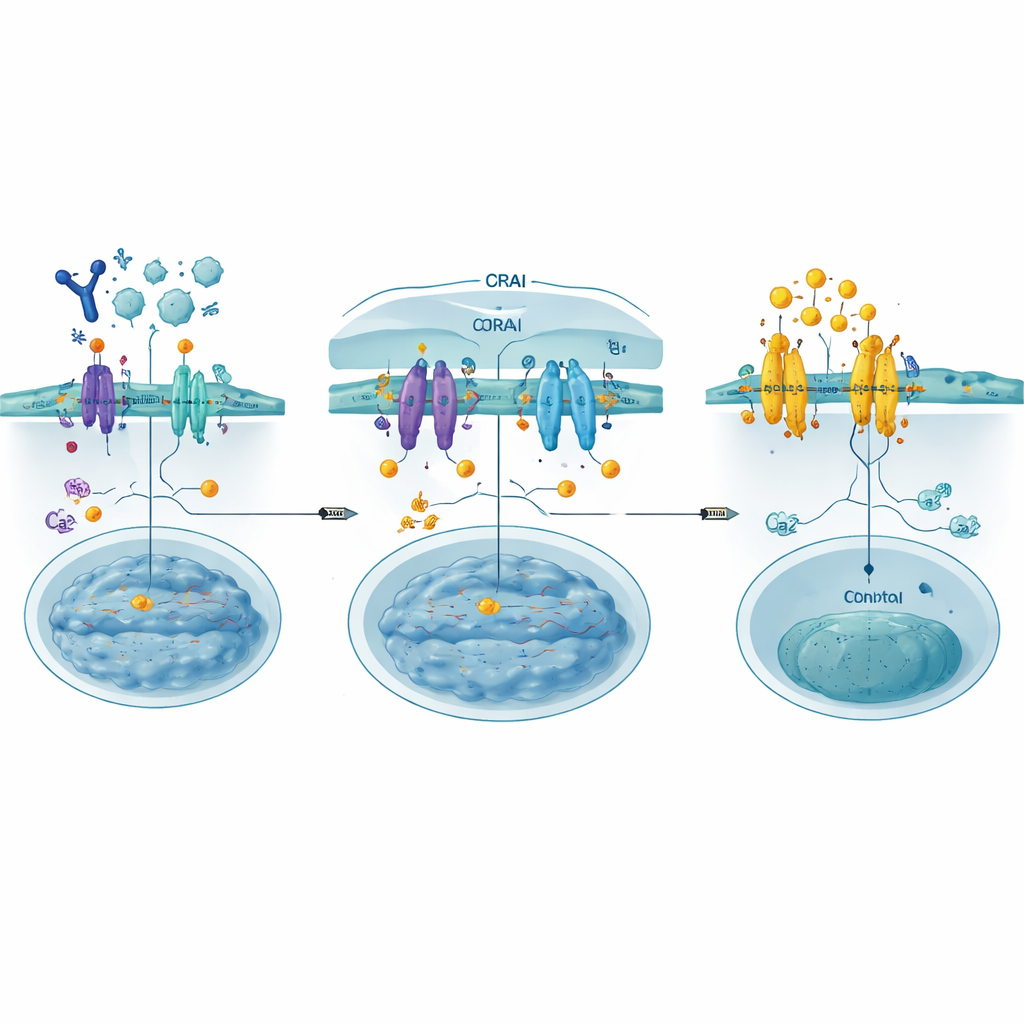
Kapiyı Engellemek İçin Tuzaklar İnşa Etmek
Yazarlar, STIM’in normalde bağlandığı ORAI parçasını taklit eden kısa, genetik olarak kodlanmış protein parçaları olarak CRAB’ları (CRAC kanal inhibitör bağlayıcılar) tasarladılar. Hücre zarına sabitlenen bu tuzaklar, aktifleşmiş STIM’i gerçek ORAI kanallarına tutunmadan önce yakalar ve böylece kalsiyum akışının üst akışında kapıyı kapatır. Yüzlerce küçük dizi değişikliğini sistematik olarak test eden derin mutasyon taraması kullanarak, insan hücrelerinde kalsiyum girişini ve NFAT’ın çekirdeğe taşınmasını güçlü şekilde azaltan özellikle kuvvetli bir bağlayıcı olan PM‑CRAB’ı tanımladılar. Yapısal modelleme, tek bir amino asit değişiminin CRAB peptidinin STIM’in bağlanma oluğuna daha sıkı oturmasını sağlayarak ortaklığı stabilize ettiğini ve engelleme gücünü artırdığını öne sürdü.
Balık Trombositlerinden Programlanabilir Sönümleyicilere
CRAB’ların canlı organizmalarda işe yaradığını göstermek için ekip, CRAC kanallarını açık tutan ve Stormorken sendromunu taklit eden hastalık yapıcı bir STIM1 mutasyonu taşıyan zebrafish kullandı. Bu balıkların floroforla işaretlenmiş trombosit benzeri thrombocyte hücre sayısı belirgin şekilde düşüktü. PM‑CRAB birlikte ifade edildiğinde, bu hücrelerin üretimi büyük ölçüde geri döndü; bu da tuzağın zararlı kalsiyum aşırı yükünü önleyebildiğini gösterdi. Araştırmacılar daha sonra farklı güçlerde bir CRAB ailesi oluşturdu: monomerler, dimerler ve kademeli olarak kanal inhibisyonunu artıran tetramerler. Kritik olarak, mavi ışıkla açılabilen sürümler (Opto‑CRAB) ve rapamisin ya da immünsüpresif olmayan bir analog gibi küçük moleküllerle etkinleştirilebilen sürümler (Chemo‑CRAB) de inşa ettiler. Kültürdeki hücrelerde bu anahtarlar, ışık veya ilaç zamanlamasına göre kalsiyum girişinin ve NFAT aktivasyonunun hızlı ve tersinir kontrolünü sağladı.
İstenildiğinde Bağışıklık ve Sinyal Yollarını Ayarlamak
Vücutta birçok yüzey reseptörü—belirli hormon, büyüme faktörü ve G‑protein‑bağlı reseptörler gibi—nihayetinde kalsiyum sinyallerini sürdürmek için CRAC kanallarına dayanır; bu nedenle yazarlar Chemo‑CRAB’ın çeşitli yollarda müdahale edip edemeyeceğini test ettiler. Kimyasal tetikleyici ile aktifleştirildiğinde, Chemo‑CRAB ışıkla ya da kafeinle kapılı kalsiyum aktüatörlerinden kaynaklanan, sentetik ve doğal büyüme faktörü reseptörlerinin ve çeşitli G‑protein‑bağlı reseptörlerin sürüklediği kalsiyum yanıtlarını zayıflattı. T hücrelerinde, zara sabitlenmiş bir CRAB CRAC akımlarını ortadan kaldırdı ve NFAT‑bağımlı gen aktivitesini keskin biçimde düşürdü. CD19‑pozitif kanser hücrelerini hedefleyen insan CAR‑T hücrelerinde PM‑CRAB önemli iltihap belirteci salımını azalttı; Chemo‑CRAB ise doz‑bağımlı, talebe göre aktifleştirilebilir sönümleme sağlayarak hücreleri kalıcı olarak devre dışı bırakmadan tükenme ve toksisiteyi sınırlama olanağına işaret etti.
Gelecek Terapiler İçin Ne Anlama Gelebilir
Uzman olmayan biri için CRAB’lar, kalsiyum sinyallemesi için son derece özgül, genetik olarak kodlanmış ses seviyesi düğmeleri olarak düşünülebilir. STIM ile ORAI arasındaki kesin el sıkışmasında etki ederek, diğer kanallara veya yukarı akış reseptörlerine geniş çaplı müdahale etmeden merkezi bir kalsiyum giriş yolunu kapatırlar. Çalışma, bu araçların zebrafish’te hastalık benzeri özellikleri düzeltebildiğini, hücrelerde karmaşık sinyal ağlarını çözümlenebileceğini ve modifiye bağışıklık hücrelerini programlanabilir şekilde düzenleyebileceğini gösteriyor. Güvenli gen teslimi sağlamak ve sağlıklı dokularda aşırı uzun süreli bloke olmaktan kaçınmak gibi zorluklar devam etse de, çalışma nadir kalsiyum kanal bozukluklarını tedavi etmeye ve CAR‑T hücreleri gibi güçlü fakat hassas terapileri ince ayarlamaya yardımcı olabilecek çok yönlü bir platform sunuyor.
Atıf: Liu, X., Ali, S., Lan, TH. et al. Engineering of genetically encoded programmable calcium channel inhibitory binders. Nat Commun 17, 3472 (2026). https://doi.org/10.1038/s41467-026-71769-2
Anahtar kelimeler: kalsiyum sinyallemesi, CRAC kanalları, optogenetik, kemogenetik, CAR‑T hücreleri