Clear Sky Science · ar
هندسة روابط مثبطة قابلة للبرمجة للتأثير على قنوات الكالسيوم المشفرة وراثياً
خفض قوة الإشارات الخلوية كأنها مقبض مستوى
تعتمد العديد من خلايا أجسامنا على اندفاعات صغيرة من الكالسيوم لتقرر متى تتحرك أو تنقسم أو تطلق هجومًا مناعيًا. عندما تشتد إشارات الكالسيوم بدرجة مفرطة، يمكن أن تغذي اضطرابات جينية نادرة، والتهابًا مزمنًا، وحتى تقلل من فعالية خلايا T المكافِحة للسرطان. تعرض هذه الدراسة مجموعة من الأدوات البروتينية المصممة خصيصًا المسماة CRABs التي تعمل كمخمدات قابلة للبرمجة في طريق رئيسي لدخول الكالسيوم إلى الخلية، مما يفتح إمكانيات جديدة للبحث الأساسي والعلاجات المستقبلية.
كيف تستخدم الخلايا الكالسيوم كمفتاح تشغيل/إيقاف
في معظم الخلايا غير العصبية، يكون المدخل الرئيسي للكالسيوم عبارة عن هيكل يعرف باسم قناة CRAC، يتشكل من شريكين: STIM الذي يستشعر مستويات الكالسيوم داخل مخزن داخلي، وORAI وهو مسام في غشاء الخلية الخارجي. عندما تنخفض المخازن الداخلية، يغير STIM شكله، وينتقل إلى مناطق تلامس فيها الأغشية الداخلية والخارجية، ويلتصق بـ ORAI. يفتح هذا القناة، مما يسمح بتدفق الكالسيوم وتحفيز استجابات تتراوح من الحركة قصيرة الأمد إلى تغييرات طويلة الأمد في نشاط الجينات. في خلايا الجهاز المناعي، هذا المسار حيوي لتنشيط عوامل النسخ مثل NFAT التي تشغّل الجينات اللازمة للدفاع، لكن إذا تُرك دون ضبط فقد يسبب مرضًا.
عندما تنحرف إشارات الكالسيوم
يمكن أن تتسبب تغييرات موروثة تجعل STIM أو ORAI في حالة "تشغيل" دائمة باضطرابات متعددة الأجهزة، مثل متلازمة ستورموركن (Stormorken)، التي تتسم بانخفاض عدد الصفائح الدموية، ومشاكل نزفية، وضعف العضلات، ومشكلات أخرى. يسهم التفعيل المزمن الأخف من نفس المسار في أمراض المناعة الذاتية، وتقدم السرطان، واستنزاف خلايا CAR‑T المهندَسة المستخدمة في علاج اللوكيميا. حاول مطورو الأدوية حجب قنوات CRAC بجزيئات صغيرة، لكن العديد من هذه المركبات يستهدف قنوات أيونية وأعضاء أخرى، مما يؤدي إلى آثار جانبية ويعيق التقدم السريري. كان هناك افتقار إلى طريقة أكثر خصوصية وقابلة للتعديل ومستهدفة جينيًا لكبح نشاط CRAC.
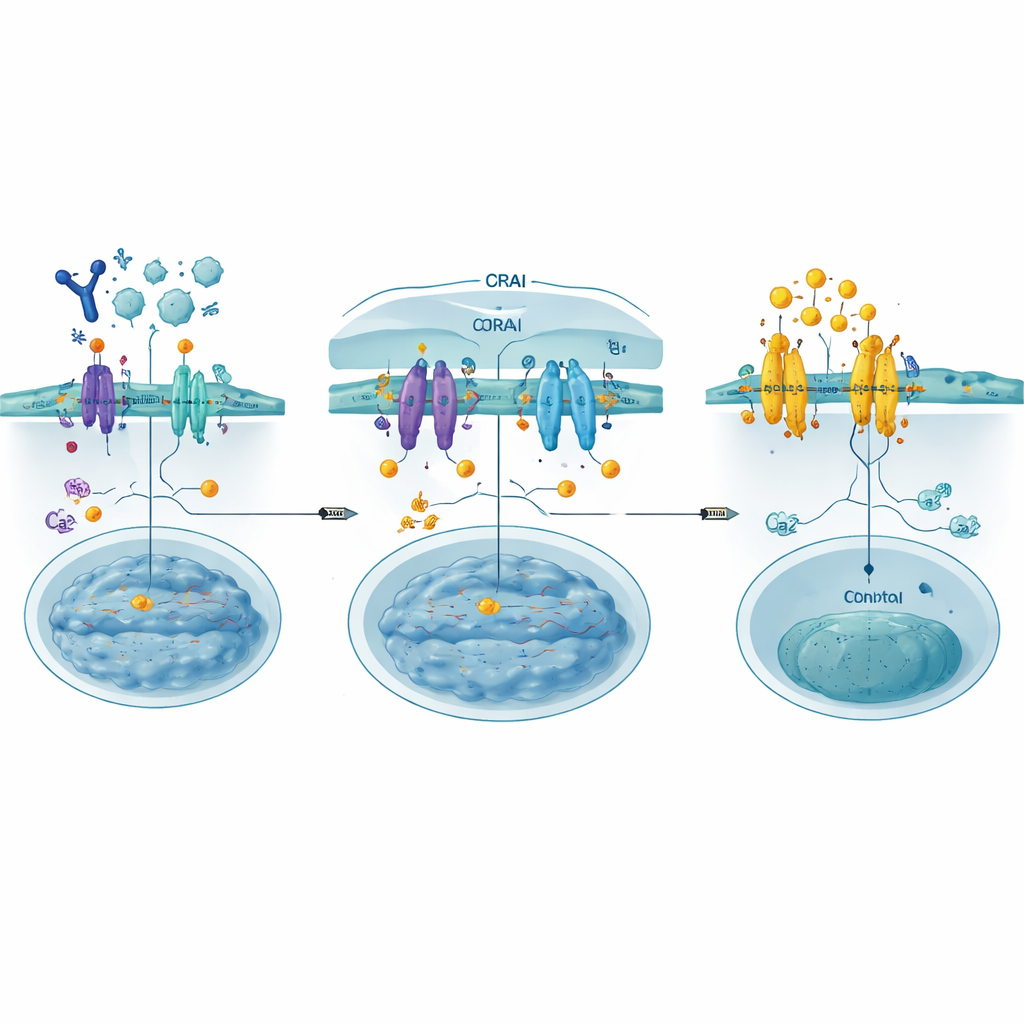
بناء طعوم لحجب البوابة
صمم الباحثون CRABs (الروابط المثبطة لقنوات CRAC) كقطع بروتينية قصيرة مشفرة جينيًا تُحاكي جزءًا من ORAI حيث يرتبط عادةً STIM. مرسوخة على غشاء الخلية، تلتقط هذه الطعوم STIM المنشط قبل أن يلتحم بقنوات ORAI الحقيقية، مغلقة البوابة فعليًا في مدخل تدفق الكالسيوم. باستخدام فحص طفرات عميق—اختبار منهجي لمئات التغيرات في التسلسل—حدّدوا رابطًا قويًا بشكل خاص أطلقوا عليه PM‑CRAB، والذي قلّل بفعالية دخول الكالسيوم وحركة NFAT إلى النواة في خلايا بشرية. أشارت النمذجة البنائية إلى أن تبادل حمض أميني واحد يجعل ببتيد CRAB يناسب أخدود ارتباط STIM بشكل أوثق، مثبتًا الشراكة ومحسنًا قدرة الحجب.
من صفائح سمك الزرد إلى مخمدات قابلة للبرمجة
لإظهار فعالية CRABs في حيوانات حية، استخدم الفريق سمك الزرد المهندس وراثيًا ليحمل طفرة في STIM1 تسبب بقاء قنوات CRAC مفتوحة وتحاكي متلازمة ستورموركن. كان لدى هذه الأسماك عدد أقل بكثير من خلايا الصفائح الدموية المشابهة (thrombocyte) الموسومة فلوريًا. عندما تم التعبير عن PM‑CRAB بالتزامن، تعافى إنتاج هذه الخلايا إلى حد كبير، مما يشير إلى أن الطعم استطاع معارضة الحمولة الضارة للكالسيوم. ثم أنشأ الباحثون عائلة من متغيرات CRAB بقوى مختلفة: أحادية، وثيرية، ورباعية تزايدت تدريجيًا في تثبيط القناة. والأهم من ذلك، بنوا أيضًا إصدارات قابلة للتشغيل بالضوء الأزرق (Opto‑CRAB) أو بجزيئات صغيرة مثل الرابامايسين أو نظير غير مثبط للمناعة (Chemo‑CRAB). في خلايا مزروعة، سمحت هذه المفاتيح بتحكم سريع وقابل للعكس في دخول الكالسيوم وتنشيط NFAT استجابةً لتوقيت الضوء أو الدواء.
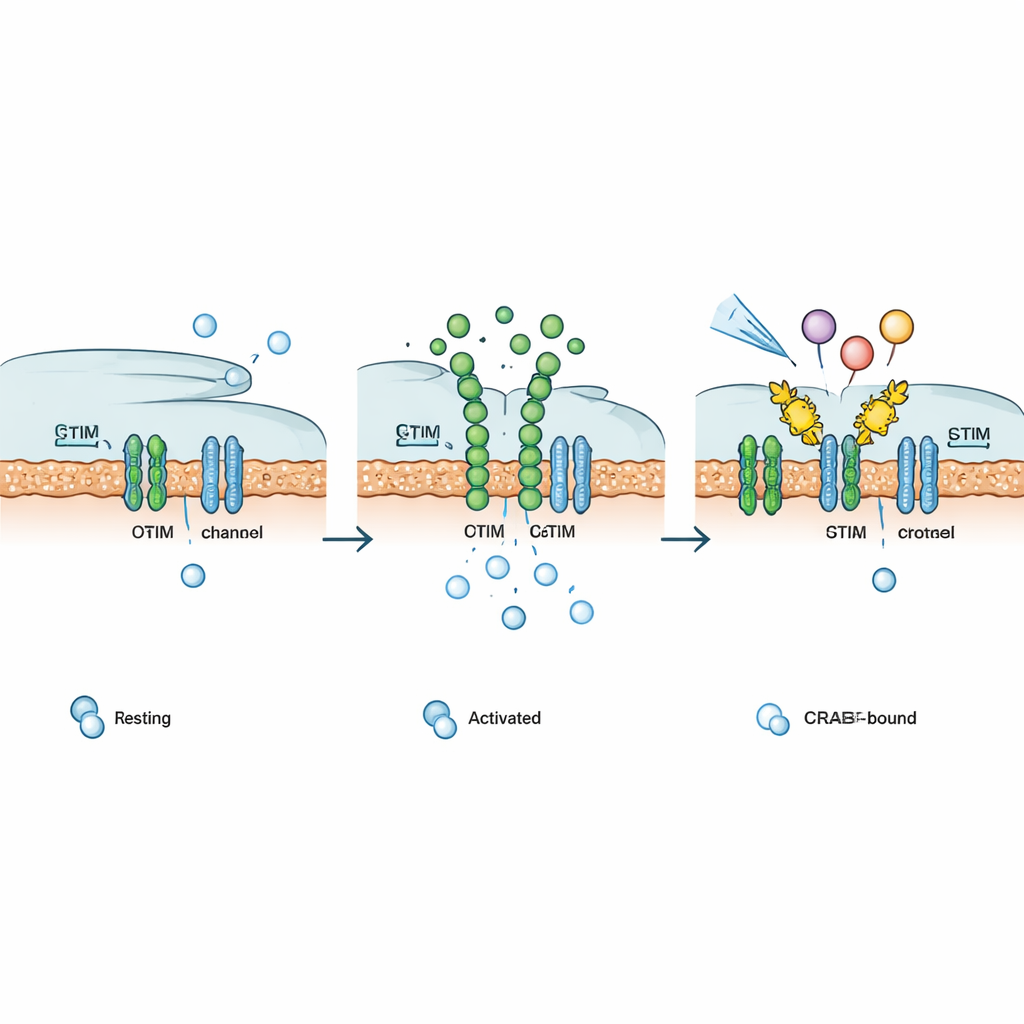
ضبط المسارات المناعية والإشارية حسب الطلب
بما أن العديد من مستقبلات السطح في الجسم—مثل بعض مستقبلات الهرمونات وعوامل النمو والمستقبلات المرتبطة بالبروتينات G—تعتمد في نهاية المطاف على قنوات CRAC للحفاظ على إشارات الكالسيوم، اختبر المؤلفون ما إذا كان Chemo‑CRAB يمكنه التدخل عبر مسارات متعددة. بعد تنشيطه بمُطلقه الكيميائي، خفّض Chemo‑CRAB استجابات الكالسيوم الناجمة عن محركات كالسيوم مُهندَسة تعمل بالضوء أو بالكافيين، ومستقبلات عوامل نمو تركيبية وطبيعية، وعدة مستقبلات مرتبطة بالبروتينات G مميزة. في خلايا T، ألغى CRAB المرسوخ على الغشاء تيارات CRAC وخفض بشكل حاد نشاط الجينات المعتمدة على NFAT. في خلايا CAR‑T البشرية المستهدفة لخلايا سرطانية موجبة لـ CD19، قلّل PM‑CRAB إفراز سيتوكينات التهابية رئيسية، بينما أتاح Chemo‑CRAB تخفيفًا معتمداً على الجرعة وقابلاً للطلب للتنشيط، مما يلمّح إلى وسيلة لتقليل الاستنزاف والسُميّة دون تعطيل الخلايا بشكل دائم.
ماذا قد يعني هذا للعلاجات المستقبلية
يمكن تشبيه CRABs لغير المتخصص على أنها مقابض ضبط مستوى متخصصة للغاية ومشفّرة جينيًا لإشارات الكالسيوم. بالعمل عند المصافحة الدقيقة بين STIM وORAI، تغلق هذه الروابط طريقًا مركزيًا لدخول الكالسيوم دون أن تتداخل بشكل واسع مع قنوات أخرى أو مستقبلات أعلى في المسار. تُظهر الدراسة أن هذه الأدوات يمكنها تصحيح خواص تشبه المرض في سمك الزرد، وتحليل شبكات إشارية معقدة في الخلايا، وتعديل خلايا الجهاز المناعي المهندَسة بطريقة قابلة للبرمجة. وبينما تظل تحديات قائمة—مثل توصيل الجينات بأمان وتجنّب الحجب الطويل المفرط في الأنسجة السليمة—تضع الدراسة أساسًا لمنصة مرنة قد تساعد في نهاية المطاف على علاج اضطرابات قنوات الكالسيوم النادرة وضبط علاجات قوية لكنها حساسة مثل خلايا CAR‑T.
الاستشهاد: Liu, X., Ali, S., Lan, TH. et al. Engineering of genetically encoded programmable calcium channel inhibitory binders. Nat Commun 17, 3472 (2026). https://doi.org/10.1038/s41467-026-71769-2
الكلمات المفتاحية: إشارة الكالسيوم, قنوات CRAC, الاستضاءة العصبية (optogenetics), الكيمياء الجينية (chemogenetics), خلايا CAR-T