Clear Sky Science · ru
Инженерия генетически запрограммированных ингибирующих соединяющих белков для кальциевых каналов
Уменьшая громкость клеточных регуляторов
Многие наши клетки полагаются на крошечные всплески кальция, чтобы решать, когда двигаться, делиться или развязать иммунную атаку. Когда эта кальциевая сигнализация выходит из-под контроля, она может приводить к редким генетическим заболеваниям, хроническому воспалению и даже ограничивать эффективность Т‑клеток, борющихся с раком. В этом исследовании представлен набор специально разработанных белковых инструментов, названных CRAB, которые действуют как программируемые демпферы на важном пути поступления кальция в клетки, открывая новые возможности для фундаментальных исследований и будущих терапий.
Как клетки используют кальций как включатель‑выключатель
В большинстве нерва‑подобных клеток основной вход для кальция обеспечивает структура, известная как CRAC‑канал, образованная двумя партнёрами: STIM, который ощущает уровень кальция в внутреннем хранилище, и ORAI — порой в наружной мембране клетки. Когда внутренние запасы снижаются, STIM меняет конформацию, перемещается в участки соприкосновения внутренней и наружной мембран и сцепляется с ORAI. Это открывает канал, позволяя кальцию вливаться и запускать реакции — от кратковременного движения до долговременных изменений активности генов. В иммунных клетках этот путь необходим для активации факторов транскрипции, таких как NFAT, которые включают гены, нужные для защиты, но при отсутствии контроля он может приводить к заболеваниям.
Когда кальциевая сигнализация даёт сбой
Наследственные изменения, которые постоянно переводят STIM или ORAI в «включённое» состояние, могут вызывать мультисистемные расстройства, такие как синдром Сторморкена, характеризующийся низким количеством тромбоцитов, проблемами со свёртываемостью, мышечной слабостью и другими симптомами. Менее выраженное, но хроническое сверхактивирование того же пути вносит вклад в развитие аутоиммунных заболеваний, прогрессирование рака и истощение модифицированных CAR‑T клеток, применяемых при лейкемии. Разработчики лекарств пытались блокировать CRAC‑каналы малыми молекулами, но многие из этих соединений взаимодействуют с другими ионными каналами и органами, вызывая побочные эффекты и тормозя клиническое продвижение. Отсутствовал более специфичный, регулируемый и генетически направляемый способ сдерживать активность CRAC.
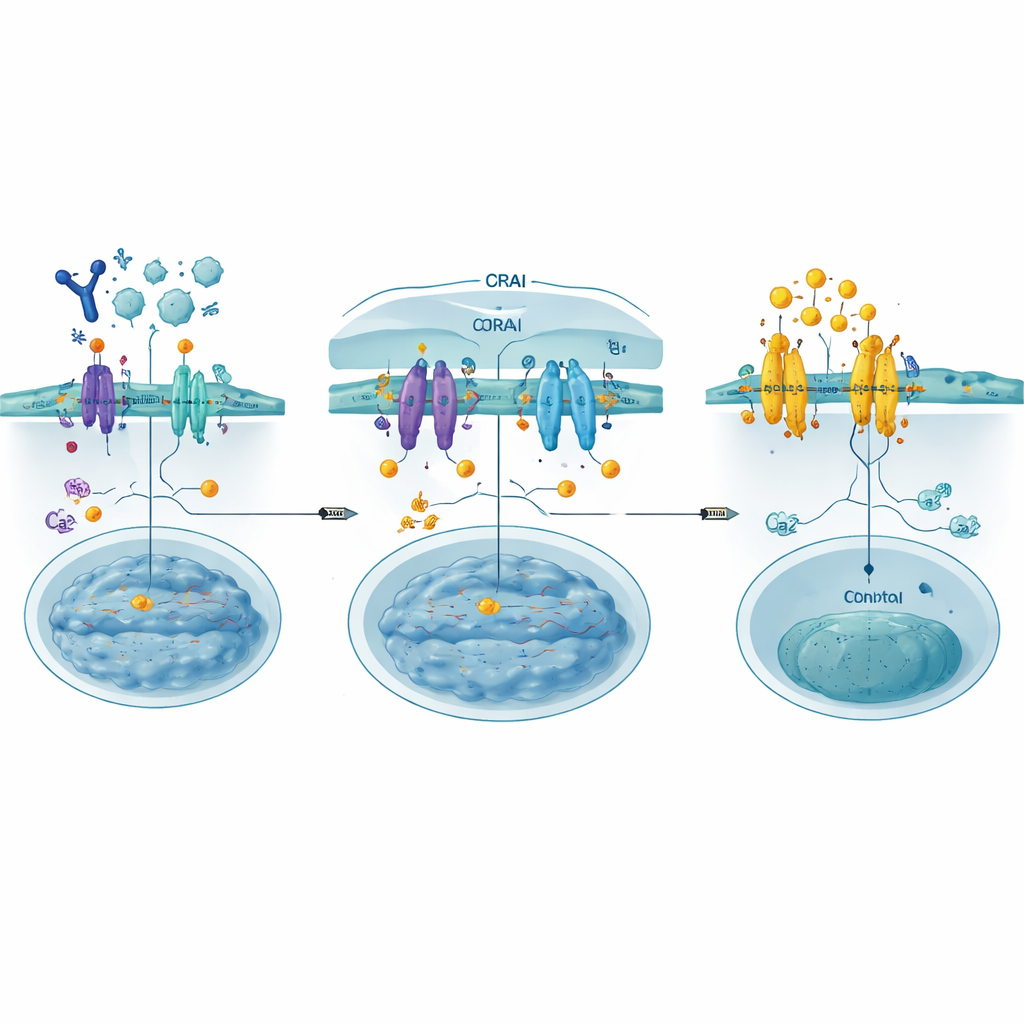
Построение «приманок», блокирующих ворота
Авторы разработали CRAB (ингибирующие связывающие белки CRAC) как короткие генетически запрограммированные фрагменты белка, имитирующие ту часть ORAI, к которой обычно прикрепляется STIM. Закреплённые на мембране клетки, эти «приманки» перехватывают активированный STIM прежде, чем он сможет сцепиться с настоящими каналами ORAI, эффективно закрывая ворота «вверх по течению» потока кальция. С помощью глубокого сканирования мутаций — систематического тестирования сотен небольших изменений последовательности — они выявили особенно сильный сродник, названный PM‑CRAB, который эффективно снижал вход кальция и перемещение NFAT в ядро в человеческих клетках. Структурное моделирование показало, что замена одной аминокислоты позволяет пептиду CRAB плотнее войти в связывающую щель STIM, стабилизируя взаимодействие и повышая блокирующую способность.
От тромбоцитов рыбы к программируемым регуляторам
Чтобы показать действие CRAB в живом организме, команда использовала рыбок‑данио с генетической модификацией, несущих мутацию STIM1, вызывающую постоянное открытие CRAC‑каналов и имитирующую синдром Сторморкена. У этих рыб значительно меньше флуоресцирующих тромбоцитоподобных клеток. Когда PM‑CRAB экспрессировался совместно, производство этих клеток во многом восстановилось, что указывает на способность приманки нейтрализовать вредную кальциевую перегрузку. Исследователи затем создали семейство вариантов CRAB с разной мощностью: мономеры, димеры и тетрамеры, которые постепенно усиливали ингибирующий эффект. Важным стало создание версий, которые можно включать синим светом (Opto‑CRAB) или малыми молекулами, такими как рапамицин или неиммунодепрессивный аналог (Chemo‑CRAB). В культуре клеток эти переключатели позволяли быстро и обратимо контролировать поступление кальция и активацию NFAT в зависимости от времени воздействия света или препарата.
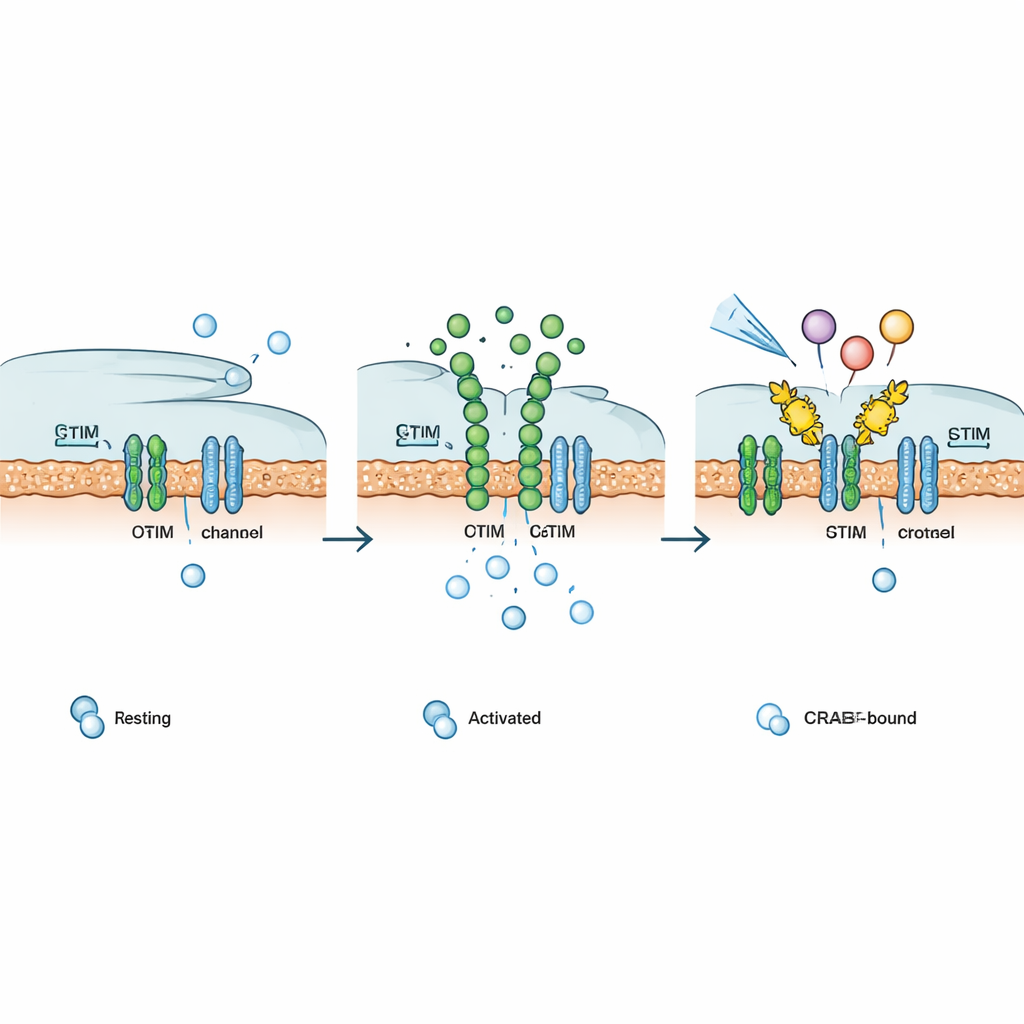
Настройка иммунных и сигнальных путей по требованию
Поскольку многие поверхностные рецепторы в организме — например, определённые гормональные, факторы роста и G‑белок‑связанные рецепторы — в конечном счёте опираются на CRAC‑каналы для поддержания кальциевых сигналов, авторы проверили, может ли Chemo‑CRAB вмешиваться в разные пути. После активации химическим триггером Chemo‑CRAB приглушал кальциевые ответы, вызванные как инженерными светозависимыми или кофеин‑чувствительными кальциевыми активаторами, так и синтетическими и естественными рецепторами факторов роста, а также несколькими различными G‑белок‑связанными рецепторами. В Т‑клетках мембраносвязываемый CRAB устранял CRAC‑токи и резко снижал активность генов, зависимых от NFAT. В человеческих CAR‑T клетках, нацеленных на CD19‑положительные раковые клетки, PM‑CRAB уменьшал выброс ключевых провоспалительных цитокинов, в то время как Chemo‑CRAB обеспечивал дозозависимое, по требованию подавление активации, что указывает на способ ограничить истощение и токсичность без постоянной инактивации клеток.
Что это может значить для будущих терапий
Для неспециалиста CRAB можно представить как высоко специфичные, генетически кодированные регуляторы «громкости» кальциевой сигнализации. Действуя на точном «рукопожатии» между STIM и ORAI, они отключают центральный путь поступления кальция, не мешая широко другим каналам или вышестоящим рецепторам. Работа демонстрирует, что эти инструменты могут корректировать похожие на заболевание признаки у рыбок‑данио, разбирать сложные сигнальные сети в клетках и программируемо модулировать модифицированные иммунные клетки. Хотя остаются задачи — такие как безопасная доставка генов и избегание чрезмерной длительной блокады в здоровых тканях — исследование закладывает универсальную платформу, которая в перспективе может помочь лечить редкие нарушения кальциевых каналов и тонко настраивать мощные, но уязвимые терапии вроде CAR‑T клеток.
Цитирование: Liu, X., Ali, S., Lan, TH. et al. Engineering of genetically encoded programmable calcium channel inhibitory binders. Nat Commun 17, 3472 (2026). https://doi.org/10.1038/s41467-026-71769-2
Ключевые слова: кальциевая сигнализация, CRAC-каналы, оптогенетика, хемогенетика, CAR‑T клетки