Clear Sky Science · zh
自噬阻断导致小鼠肌节肌病模型中严重骨骼肌破坏 6
当细胞的清理队伍失灵
我们的肌肉不断自我修复,默默清除磨损部件,让我们可以不假思索地行走、呼吸和活动。本文探讨当这种细胞清理系统因一处遗传突变而崩溃时会发生什么。结果是一种毁灭性的儿童肌肉疾病,削弱四肢和呼吸肌。通过构建详尽的小鼠模型,研究者不仅揭示了肌细胞内损伤如何展开,还测试了逆转损害的方法,为未来疗法带来一线希望。
聚焦一种罕见的肌病
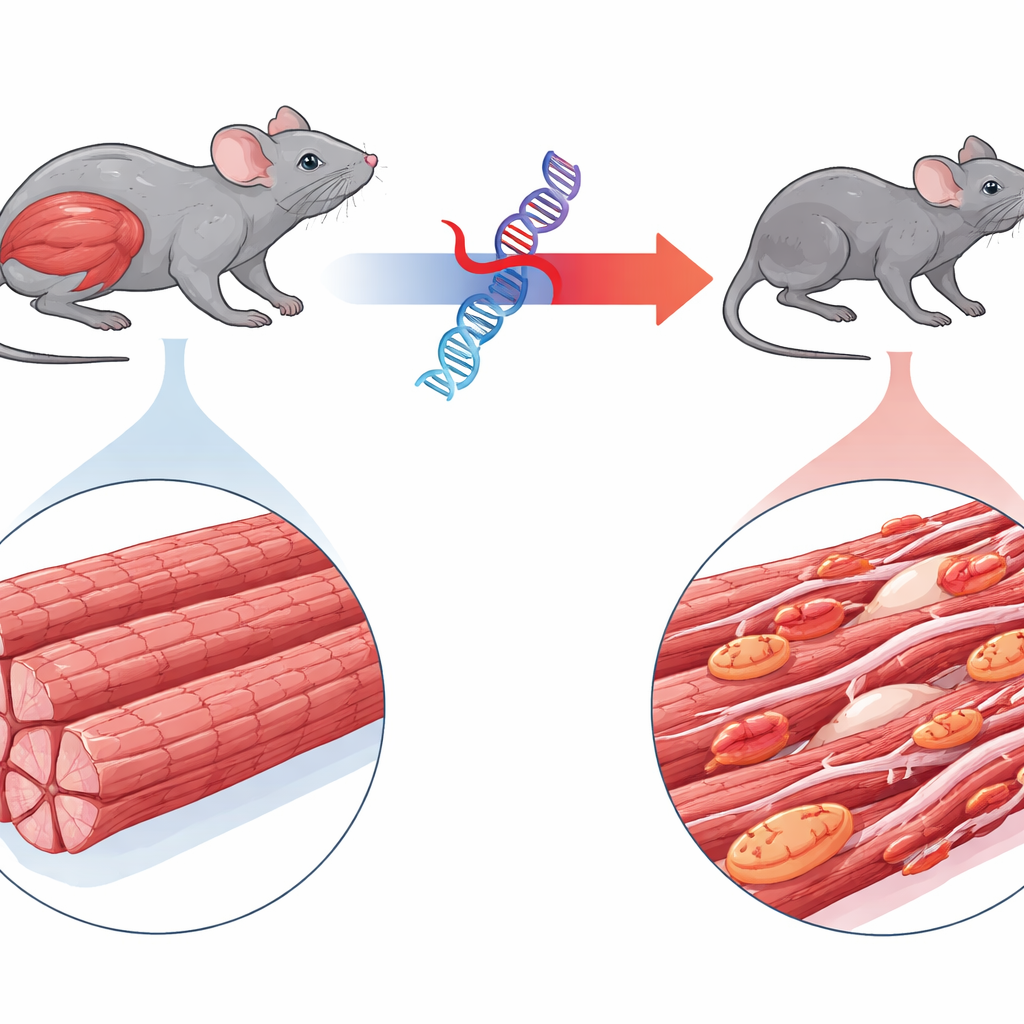
该研究以肌节肌病6型为中心,这是一种由名为 BAG3 的基因突变引起的罕见疾病。患儿会迅速出现严重肌无力,有时伴随心脏问题,并常因呼吸衰竭早逝。BAG3 通常负责监督肌纤维内微小收缩单元的质量,将受损蛋白导向细胞回收途径。作者工程化小鼠,使其表达带有荧光标记的人类突变型 BAG3,从而能够追踪其行为。与表达正常人类 BAG3 的小鼠不同,携带突变体的动物迅速变小,出现肢体和呼吸肌萎缩,并表现出摇摆步态,极为贴近人类疾病的特征。
肌纤维如何瓦解
显微和超微结构检查揭示了突变蛋白如何彻底破坏肌肉结构。在受影响的小鼠中,肌纤维变薄并布满异常蛋白团块。高度有序的收缩机械条纹——肌节——片段化且变得模糊,许多纤维显示中央核,这是试图再生的标志。免疫细胞浸润组织,纤维性瘢痕物质增加,尽管不像心脏那样剧烈。在功能上,这些小鼠分离的肌肉产力比健康动物低高达90%,即便考虑到其体积较小,这仍然证实了收缩核心机器出现了故障。
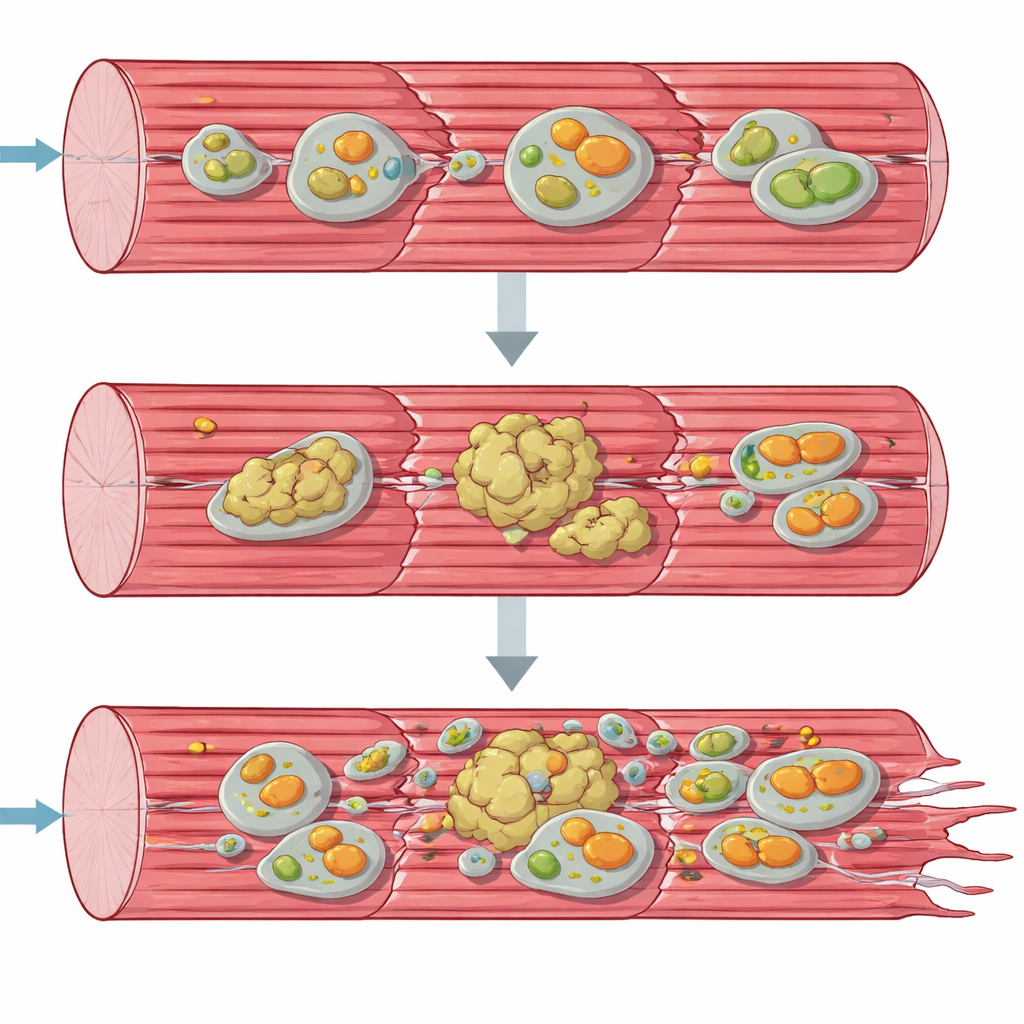
蛋白堆积与病态线粒体
为了从系统层面理解这些崩溃,团队使用了可以一次性检测数千种分子的“组学”工具。基因表达和蛋白质谱显示肌细胞正竭力应对:用于合成新蛋白和应激反应的基因被激活,许多分子伴侣和其他质量控制因子积累。然而,许多关键的收缩结构蛋白从其正常的可溶形式中减少,转而进入富含不可溶聚集体的部分。与此同时,细胞回收通路的组成成分——自噬以及专门清除损伤线粒体的线粒体自噬——像是卡在中途一样堆积。电子显微镜和线粒体功能测试证实,能量产生细胞器形态异常、聚集,并且功能远低于正常,尤其是在呼吸链的第一步。
自噬:核心罪魁
作者接着探讨主要问题是否出在通用的细胞回收(自噬)、线粒体特异的回收(线粒体自噬)或两者兼有。他们从突变小鼠培养肌细胞并实验性地增强不同通路。通过蛋白 BECN1 刺激广谱自噬可以清除关键应激标志物,减少突变 BAG3 聚集体,并改善肌节的外观与组织结构。相比之下,单独强制线粒体自噬或仅增加线粒体生物合成并未纠正缺陷。在活体小鼠中,使用激活自噬的药物雷帕霉素改善了抓握力、协调性和运动,并提高了肌肉中活跃回收的标志物。这些实验共同指向自噬的主要阻断,线粒体损伤更像是继发结果而非根本原因。
测试一种基因治疗策略
因为该疾病由有毒蛋白驱动,研究者探讨了降低突变 BAG3 是否能拯救肌肉。他们将一种特异性针对人类 BAG3 的短发夹 RNA(shRNA)装入工程化病毒,并将其注入年轻突变小鼠的血液中。数周后,肌肉中的突变 BAG3 明显减少,蛋白聚集体减少,瘢痕减少,中央核的纤维数量也大幅下降。最重要的是,接受治疗的肌肉产生了显著更多的力并部分恢复到正常大小。这一概念验证表明,沉默致病等位基因,或将此类方法与增强自噬的药物联合使用,可能成为患者的有力策略,前提是优化到等位基因特异性的疗法。
这对患者及更广泛领域的意义
通俗地说,这项工作表明,当像 BAG3 这样的关键帮助蛋白错误折叠并形成团块时,细胞的垃圾处理系统会堵塞。损坏的成分和异常线粒体累积,肌肉的内部支架崩溃,力量随之衰退。通过小心重建小鼠模型,研究显示恢复或绕过这一清理系统——无论是通过增强自噬还是减少突变 BAG3 本身——都能显著恢复肌肉健康。尽管在这些疗法进入临床前还有许多工作要做,但这些发现为应对这种罕见却致命的肌肉疾病提供了详细路线图,也为理解受损的细胞家务管理如何可能导致其他退行性疾病提供了更广泛的见解。
引用: Filippi, K., Graf-Riesen, K., Kuppusamy, M. et al. Blockage of autophagy causes severe skeletal muscle disruption in a mouse model for myofibrillar myopathy 6. Nat Commun 17, 3436 (2026). https://doi.org/10.1038/s41467-026-71749-6
关键词: 肌节肌病, BAG3 突变, 自噬, 骨骼肌退化, 基因治疗