Clear Sky Science · tr
Otofajinin Engellenmesi, Miyofibriller Miyopati 6 İçin Bir Fare Modelinde Ağır İskelet Kası Bozulmasına Neden Olur
Hücrenin Temizlik Ekibi Başarısız Olduğunda
Kaslarımız sürekli kendini onarıyor; yıpranmış bileşenleri sessizce temizleyerek yürümemizi, nefes almamızı ve düşünmeden hareket etmemizi sağlıyor. Bu makale, bu hücresel temizlik sisteminin tek bir kalıtsal mutasyon nedeniyle bozulduğunda neler olduğunu inceliyor. Sonuç, uzuvları ve solunum kaslarını zayıflatan yıkıcı bir çocukluk kas hastalığı. Araştırmacılar, ayrıntılı bir fare modeli oluşturarak hasarın kas hücreleri içinde nasıl geliştiğini ortaya koymakla kalmıyor, aynı zamanda tersine çevirmeye yönelik yolları test ederek gelecekteki tedaviler için bir umut ışığı vaat ediyor.
Odaklanmış Nadir Bir Kas Hastalığı
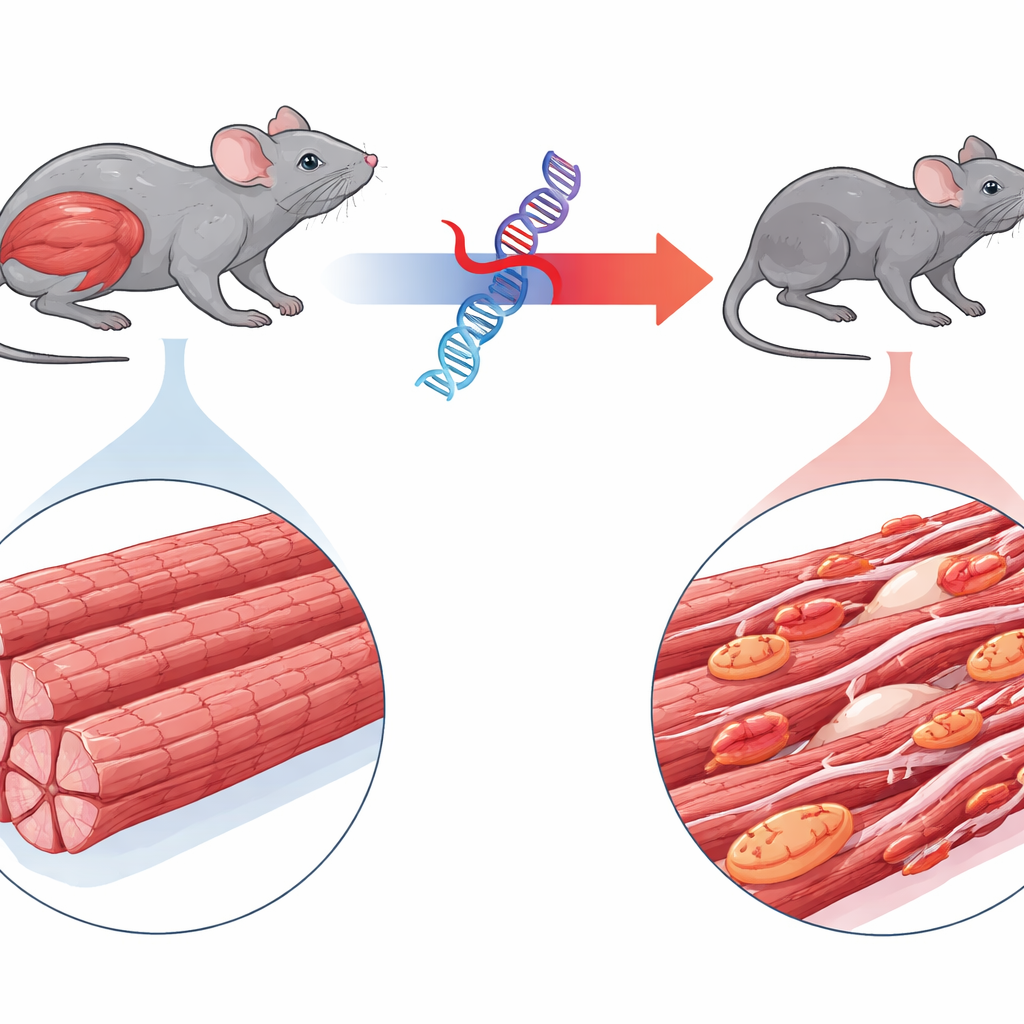
Çalışma, BAG3 adlı bir gendeki mutasyonun neden olduğu nadir bir bozukluk olan miyofibriller miyopati 6 üzerinde yoğunlaşıyor. Bu duruma sahip çocuklar hızla derin kas zayıflığı, bazen kalp sorunları geliştirir ve sık sık solunum yetmezliğinden genç yaşta hayatlarını kaybederler. BAG3 normalde kas lifleri içindeki küçük kasılma birimlerinin kalitesini denetlemeye yardım eder, hasarlı proteinleri hücresel geri dönüşüme yönlendirir. Yazarlar, insanın mutasyonlu BAG3 formunu floresan bir işaretleyici ile etikettenmiş olarak üreten fareler tasarladılar; bu sayede protein davranışını izleyebildiler. Normal insan BAG3 ekspresse eden farelerin aksine, mutasyonlu versiyona sahip hayvanlar hızla daha küçük hale geldi, uzuv ve solunum kaslarında erime gösterdi ve insan hastalığını yakından yansıtan bir yürüyüş bozukluğu sergilediler.
Kas Lifleri Nasıl Dağılır
Mikroskobik ve ultrastrüktürel incelemeler, mutasyonlu proteinin kas yapısını ne kadar kapsamlı biçimde bozduğunu ortaya koydu. Etkilenen farelerde kas lifleri daha incedi ve anormal protein kümeleriyle doluydu. Kasılma mekanizmasının son derece düzenli çizgileri — sarkomerler — parçalanmış ve bulanıktı ve birçok lif, yeniden yapılanma girişiminin işareti olan merkezi çekirdeklere sahipti. Bağışıklık hücreleri dokuya infiltre olmuş ve fibröz skar dokusu artmıştı; yine de kalpteki kadar dramatik değildi. İşlevsel olarak, bu farelerden izole edilen kaslar, daha küçük boyutları hesaba katılsa bile, sağlıklı hayvanlarınkine göre yüzde 90'a varan oranda daha az kuvvet üretti; bu da kasılmanın temel mekanizmasının başarısız olduğunu doğruladı.
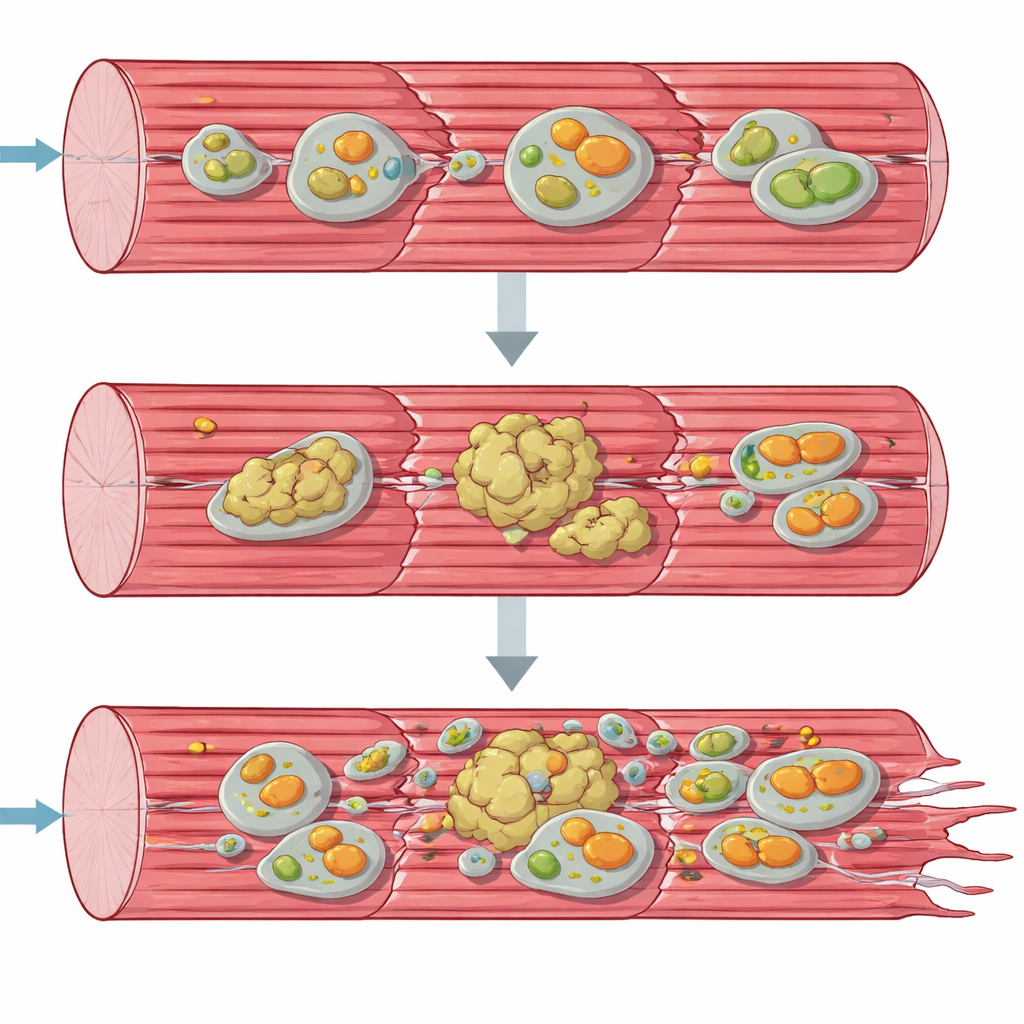
Protein Yığınları ve Hasta Mitokondriler
Bozulumayı sistemsel bir bakışla anlamak için ekip, aynı anda binlerce molekülü tarayan “omik” araçlara yöneldi. Gen aktivitesi ve protein profilleri, kas hücrelerinin çaresizce yanıt vermeye çalıştığını gösterdi: yeni protein yapımı ve stres yanıtı genleri hızlanmış, birçok şaperon ve diğer kalite kontrol faktörleri birikmişti. Yine de kontraktil aparatın birçok ana yapısal proteini normal çözünür formlarından tükenmiş ve bunun yerine çözünmez, agregat açısından zengin bir fraksiyona kaymıştı. Aynı zamanda hücrenin geri dönüşüm yollarının — otofaji ve hasarlı mitokondrilerin özel olarak uzaklaştırılması olan mitofaji — bileşenleri, işlem yarıda kalmış gibi birikmişti. Elektron mikroskobu ve mitokondriyal fonksiyon testleri, enerji üreten organellerin şekil bozukluğu gösterdiğini, kümelendiğini ve özellikle solunum zincirinin ilk adımında normal kapasitenin çok altında çalıştığını doğruladı.
Otofaji Merkezi Suçlu Olarak
Yazarlar daha sonra asıl sorunun genel hücresel geri dönüşümde (otofaji), mitokondriye özgü geri dönüşümde (mitofaji) yoksa her ikisinde mi olduğunu sordular. Mutant farelerden kas hücreleri yetiştirdiler ve farklı yolları deneysel olarak güçlendirdiler. BECN1 proteini ile geniş otofajiyi uyarmak, önemli stres belirteçlerini temizledi, mutant BAG3 agregalarını azalttı ve sarkomerlerin görünümünü ve organizasyonunu iyileştirdi. Buna karşılık, mitofajiyi zorlamak ya da sadece mitokondri üretimini artırmak kusurları düzeltmedi. Canlı farelerde otofajiyi aktive eden rapamisin ile tedavi, kavrama gücünü, koordinasyonu ve hareketi iyileştirdi ve kasta aktif geri dönüşüm belirteçlerini artırdı. Birlikte, bu deneyler otofajide birincil bir tıkanma olduğunu ve mitokondriyal hasarın kök neden değil, ikincil bir sonuç olarak ortaya çıktığını gösteriyor.
Bir Gen Terapisi Stratejisinin Testi
Hastalık toksik bir proteinden kaynaklandığı için araştırmacılar, mutant BAG3'ü azaltmanın kasları kurtarıp kurtaramayacağını araştırdılar. İnsan BAG3'ü özgül olarak hedefleyecek şekilde tasarlanmış kısa saç tokası (short hairpin) RNA'yı mühendislikli bir virüse paketlediler ve genç mutant farelerin kan dolaşımına verdiler. Haftalar sonra kaslarda çok daha az mutant BAG3, daha az protein agregası, azalmış skar dokusu ve merkezi çekirdeğe sahip liflerin sayısında belirgin düşüş görüldü. En önemlisi, tedavi edilen kaslar dramatik şekilde daha fazla kuvvet üretti ve kısmen normal boyuta kavuştu. Bu konsept kanıtı, hastalığa neden olan geni susturmanın ya da böyle bir yaklaşımı otofajiyi artıran ilaçlarla birleştirmenin, allel-spesifik bir terapi optimize edildiğinde hastalar için güçlü bir strateji olabileceğini öne sürüyor.
Hastalar ve Ötesi İçin Anlamı
Erişilebilir ifadeyle, bu çalışma BAG3 gibi önemli bir yardımcı protein yanlış katlanıp kümeleştiğinde hücrenin çöp öğütücüsünün tıkandığını gösteriyor. Kırık bileşenler ve hatalı mitokondriler birikir, kasın iç iskelesi çöker ve güç azalır. Hastalığı farede dikkatlice yeniden yaratarak çalışma, bu temizlik sistemini onarmanın veya atlamanın — ya otofajiyi güçlendirerek ya da mutant BAG3'ü azaltarak — kas sağlığını önemli ölçüde geri kazandırabileceğini gösteriyor. Bu tür tedaviler klinikte uygulanmadan önce yapılacak çok iş olsa da bulgular, bu nadir ama ölümcül kas bozukluğuna yönelik ayrıntılı bir yol haritası sunuyor ve bozulmuş hücresel temizlik mekanizmalarının diğer dejeneratif hastalıkların altında yatan nedenlerden biri olabileceğine dair daha geniş içgörüler sağlıyor.
Atıf: Filippi, K., Graf-Riesen, K., Kuppusamy, M. et al. Blockage of autophagy causes severe skeletal muscle disruption in a mouse model for myofibrillar myopathy 6. Nat Commun 17, 3436 (2026). https://doi.org/10.1038/s41467-026-71749-6
Anahtar kelimeler: miyofibriller miyopati, BAG3 mutasyonu, otofaji, iskelet kası dejenerasyonu, gen terapisi