Clear Sky Science · de
Blockade der Autophagie verursacht schwere Skelettmuskelstörungen in einem Mausmodell der myofibrillären Myopathie 6
Wenn die zelluläre Reinigungskraft versagt
Unsere Muskeln reparieren sich ständig selbst und beseitigen im Verborgenen abgenutzte Bestandteile, damit wir ohne Nachdenken gehen, atmen und uns bewegen können. Dieser Artikel untersucht, was passiert, wenn dieses zelluläre Reinigungssystem aufgrund einer einzigen vererbten Mutation zusammenbricht. Das Ergebnis ist eine verheerende kindliche Muskelerkrankung, die Gliedmaßen und Atemmuskulatur schwächt. Durch den Aufbau eines detaillierten Mausmodells decken die Forschenden nicht nur auf, wie sich der Schaden in den Muskelzellen entfaltet, sondern testen auch Wege, ihn umzukehren, und bieten damit einen Funken Hoffnung für künftige Therapien.
Eine seltene Muskelerkrankung im Fokus
Die Studie konzentriert sich auf myofibrilläre Myopathie 6, eine seltene Erkrankung, die durch eine Mutation im Gen BAG3 verursacht wird. Kinder mit dieser Erkrankung entwickeln rasch schwere Muskelschwäche, manchmal Herzprobleme, und sterben oft jung an Atemversagen. BAG3 überwacht normalerweise die Qualität der winzigen kontraktilen Einheiten in den Muskelfasern und leitet beschädigte Proteine zum zellulären Recycling. Die Autorinnen und Autoren erzeugten Mäuse, die die menschliche mutante Form von BAG3 mit einem fluoreszierenden Marker produzieren, sodass sie ihr Verhalten verfolgen konnten. Im Gegensatz zu Mäusen, die normales menschliches BAG3 exprimieren, wurden Tiere mit der mutanten Version schnell kleiner, zeigten Muskelabbau an Gliedmaßen und Atemmuskulatur und einen watschelnden Gang, was die menschliche Krankheit eindrücklich widerspiegelt.
Wie Muskelfasern auseinanderfallen
Mikroskopische und ultrastrukturelle Untersuchungen zeigten, wie gründlich das mutante Protein die Muskelstruktur stört. Bei betroffenen Mäusen waren die Muskelfasern dünner und durchsetzt mit abnormen Proteinansammlungen. Die hochgeordneten Streifen der kontraktilen Maschinerie — die Sarkomere — waren fragmentiert und unscharf, und viele Fasern wiesen zentral gelegene Zellkerne auf, ein Kennzeichen versuchter Regeneration. Immunzellen durchdrangen das Gewebe und fibröses Narbenmaterial nahm zu, wenn auch weniger dramatisch als im Herzen. Funktionell erzeugten isolierte Muskeln dieser Mäuse bis zu 90 Prozent weniger Kraft als die von gesunden Tieren, selbst unter Berücksichtigung ihrer kleineren Größe, was bestätigt, dass die Kernmaschinerie der Kontraktion versagte.
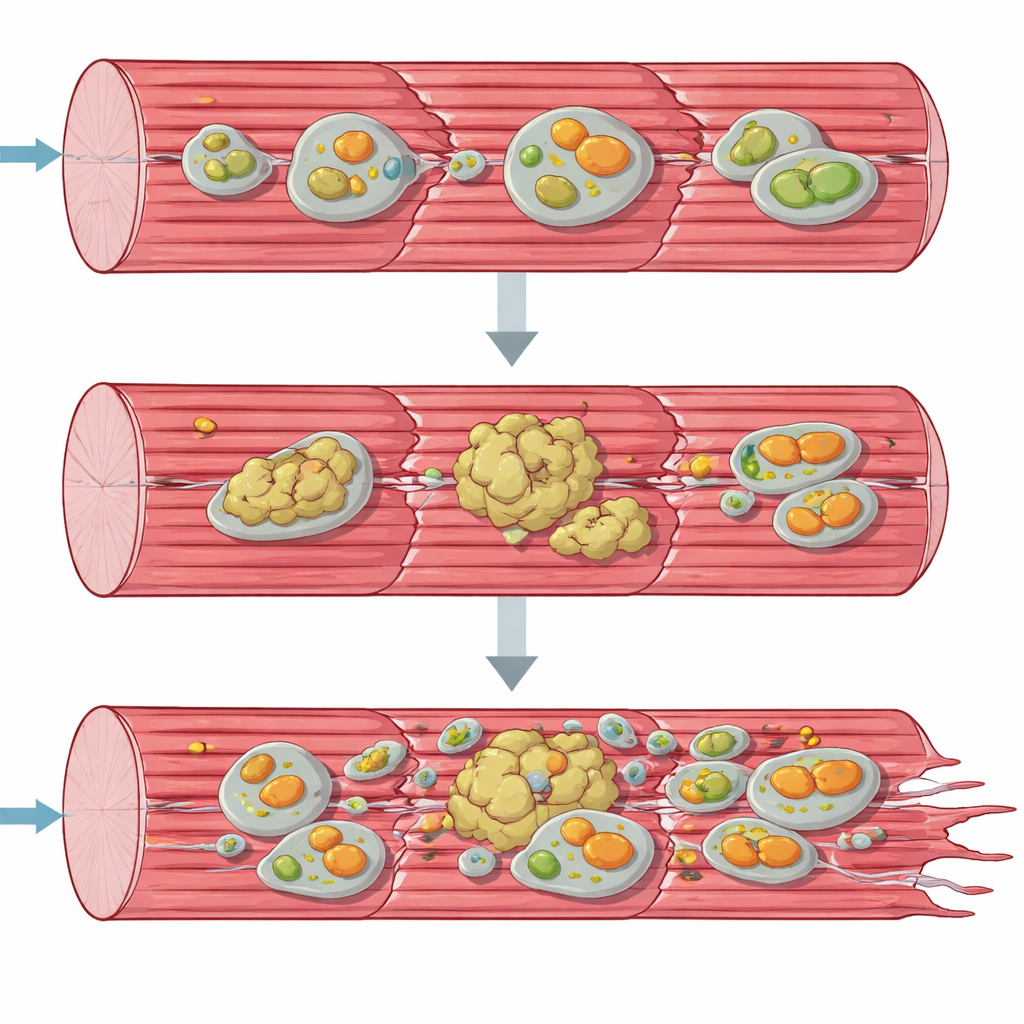
Proteinansammlungen und kranke Mitochondrien
Um den Zusammenbruch aus einer systemischen Perspektive zu verstehen, nutzte das Team „Omics“-Werkzeuge, die Tausende von Molekülen gleichzeitig erfassen. Genaktivitäts- und Proteinanalyse zeigten, dass Muskelzellen verzweifelt versuchten zu reagieren: Gene für den Aufbau neuer Proteine und Stressantworten waren hochreguliert, und viele Chaperone sowie andere Qualitätskontrollfaktoren häuften sich an. Viele wichtige Strukturproteine des kontraktilen Apparats waren jedoch aus ihren normalen löslichen Formen erschöpft und verschoben in einen unlöslichen, aggregatreichen Fraktion. Gleichzeitig stauten sich Komponenten der zellulären Recyclingwege — Autophagie und die spezialisierte Entfernung beschädigter Mitochondrien, Mitophagie — als wären sie im Prozess stecken geblieben. Elektronenmikroskopie und Tests zur mitochondrialen Funktion bestätigten, dass energieproduzierende Organellen deformiert, gehäuft und weit unterhalb der normalen Kapazität arbeiteten, insbesondere beim ersten Schritt der Atemkette.
Autophagie als zentrale Ursache
Die Autorinnen und Autoren fragten anschließend, ob das primäre Problem in der allgemeinen zellulären Recyclingfunktion (Autophagie), in der mitochondrien-spezifischen Reinigung (Mitophagie) oder in beiden liege. Sie züchteten Muskelzellen aus den mutanten Mäusen und verstärkten experimentell verschiedene Wege. Die Anregung der allgemeinen Autophagie mit dem Protein BECN1 beseitigte zentrale Stressmarker, verringerte BAG3-Aggregate der Mutante und verbesserte das Aussehen und die Organisation der Sarkomere. Im Gegensatz dazu korrigierte das forcierte Anregen der Mitophagie oder allein die Erhöhung der Mitochondrienproduktion die Defekte nicht. In lebenden Mäusen verbesserte die Behandlung mit dem Autophagie-aktivierenden Wirkstoff Rapamycin die Griffstärke, Koordination und Bewegung und erhöhte Marker aktiven Recyclings im Muskel. Zusammengenommen deuten diese Experimente auf einen primären Block in der Autophagie hin, wobei mitochondriale Schäden als sekundäre Folge und nicht als ursächlicher Auslöser erscheinen.
Prüfung einer Gentherapie-Strategie
Da die Krankheit durch ein toxisches Protein verursacht wird, untersuchten die Forschenden, ob das Herunterregulieren des mutanten BAG3 die Muskeln retten könnte. Sie verpackten eine kurze Haarpin-RNA, die gezielt menschliches BAG3 adressiert, in ein ingenieurbiologisches Virus und verabreichten es jungen mutanten Mäusen über den Blutkreislauf. Wochen später zeigten die Muskeln deutlich weniger mutantes BAG3, weniger Proteinaggregate, reduzierte Vernarbung und weit weniger Fasern mit zentralen Kernen. Am wichtigsten war, dass behandelte Muskeln dramatisch mehr Kraft erzeugten und teilweise wieder normale Größe erreichten. Dieser Proof-of-Concept legt nahe, dass das Stilllegen des krankheitsverursachenden Gens oder die Kombination einer solchen Strategie mit Wirkstoffen, die die Autophagie fördern, eine starke Therapieoption für Patienten sein könnte, sobald eine allelspezifische Behandlung optimiert ist.
Was das für Patienten und darüber hinaus bedeutet
Anschaulich gezeigt, bedeutet diese Arbeit: Wenn ein Schlüsselhelferprotein wie BAG3 fehlfaltet und verklumpt, verklemmt das zelluläre Entsorgungssystem. Zerbrochene Komponenten und defekte Mitochondrien häufen sich an, das innere Gerüst des Muskels bricht zusammen und die Kraft schwindet. Durch die sorgfältige Nachbildung der Krankheit in Mäusen zeigt die Studie, dass das Wiederherstellen oder Umgehen dieses Reinigungssystems — entweder durch die Förderung der Autophagie oder durch Reduktion des mutanten BAG3 selbst — die Muskelgesundheit erheblich wiederherstellen kann. Zwar ist noch viel zu tun, bevor solche Behandlungen die Klinik erreichen, doch die Befunde liefern eine detaillierte Roadmap zur Bekämpfung dieser seltenen, aber tödlichen Muskelerkrankung und bieten weitergehende Einblicke, wie beeinträchtigte zelluläre Hauswirtschaft anderen degenerativen Krankheiten zugrunde liegen könnte.
Zitation: Filippi, K., Graf-Riesen, K., Kuppusamy, M. et al. Blockage of autophagy causes severe skeletal muscle disruption in a mouse model for myofibrillar myopathy 6. Nat Commun 17, 3436 (2026). https://doi.org/10.1038/s41467-026-71749-6
Schlüsselwörter: myofibrilläre Myopathie, BAG3-Mutation, Autophagie, Degeneration der Skelettmuskulatur, Gentherapie