Clear Sky Science · fr
Blocage de l’autophagie entraîne une grave disruption du muscle squelettique dans un modèle murin de myopathie myofibrillaire 6
Quand l’équipe de nettoyage cellulaire fait défaut
Nos muscles se réparent constamment, éliminant silencieusement les éléments usés pour que nous puissions marcher, respirer et bouger sans y penser. Cet article examine ce qui se passe lorsque ce système de nettoyage cellulaire se dérègle à cause d’une seule mutation héréditaire. Le résultat est une maladie musculaire infantile dévastatrice qui affaiblit les membres et les muscles respiratoires. En construisant un modèle murin détaillé, les chercheurs dévoilent non seulement comment les dommages se déroulent à l’intérieur des cellules musculaires, mais testent aussi des moyens de les inverser, offrant une lueur d’espoir pour de futures thérapies.
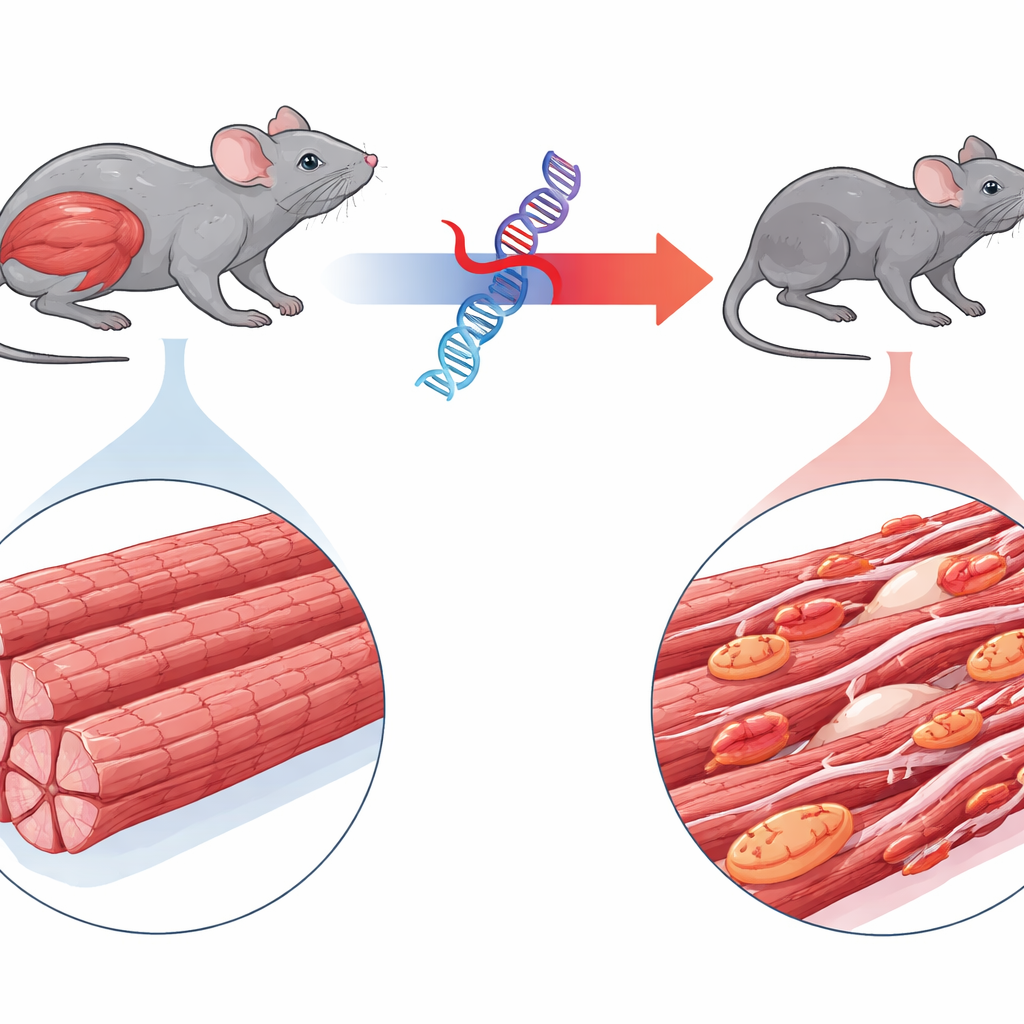
Une maladie musculaire rare sous les projecteurs
L’étude se concentre sur la myopathie myofibrillaire 6, un trouble rare causé par une mutation dans un gène nommé BAG3. Les enfants atteints de cette maladie développent rapidement une faiblesse musculaire profonde, parfois des problèmes cardiaques, et meurent souvent jeunes d’une insuffisance respiratoire. BAG3 aide normalement à superviser la qualité des minuscules unités contractiles à l’intérieur des fibres musculaires, dirigeant les protéines endommagées vers le recyclage cellulaire. Les auteurs ont généré des souris produisant la forme humaine mutante de BAG3 marquée par un marqueur fluorescent, ce qui leur a permis de suivre son comportement. Contrairement aux souris exprimant BAG3 humaine normale, les animaux portant la version mutante sont rapidement devenus plus petits, ont montré une fonte des muscles des membres et des muscles respiratoires, et une démarche chaloupée, reflétant étroitement la maladie humaine.
Comment les fibres musculaires se désagrègent
Des examens microscopiques et ultrastructuraux ont révélé à quel point la protéine mutante perturbe la structure musculaire. Chez les souris affectées, les fibres musculaires étaient plus fines et parcourues d’amas protéiques anormaux. Les bandes hautement ordonnées de la machinerie contractile — les sarcomères — étaient fragmentées et floues, et de nombreuses fibres présentaient des noyaux centraux, un signe caractéristique d’une régénération tentée. Des cellules immunitaires ont infiltré le tissu et la matière cicatricielle fibreuse a augmenté, bien que moins spectaculairement que dans le cœur. Sur le plan fonctionnel, les muscles isolés de ces souris produisaient jusqu’à 90 % de force en moins que ceux d’animaux sains, même en tenant compte de leur plus petite taille, confirmant que la machinerie centrale de la contraction était déficiente.
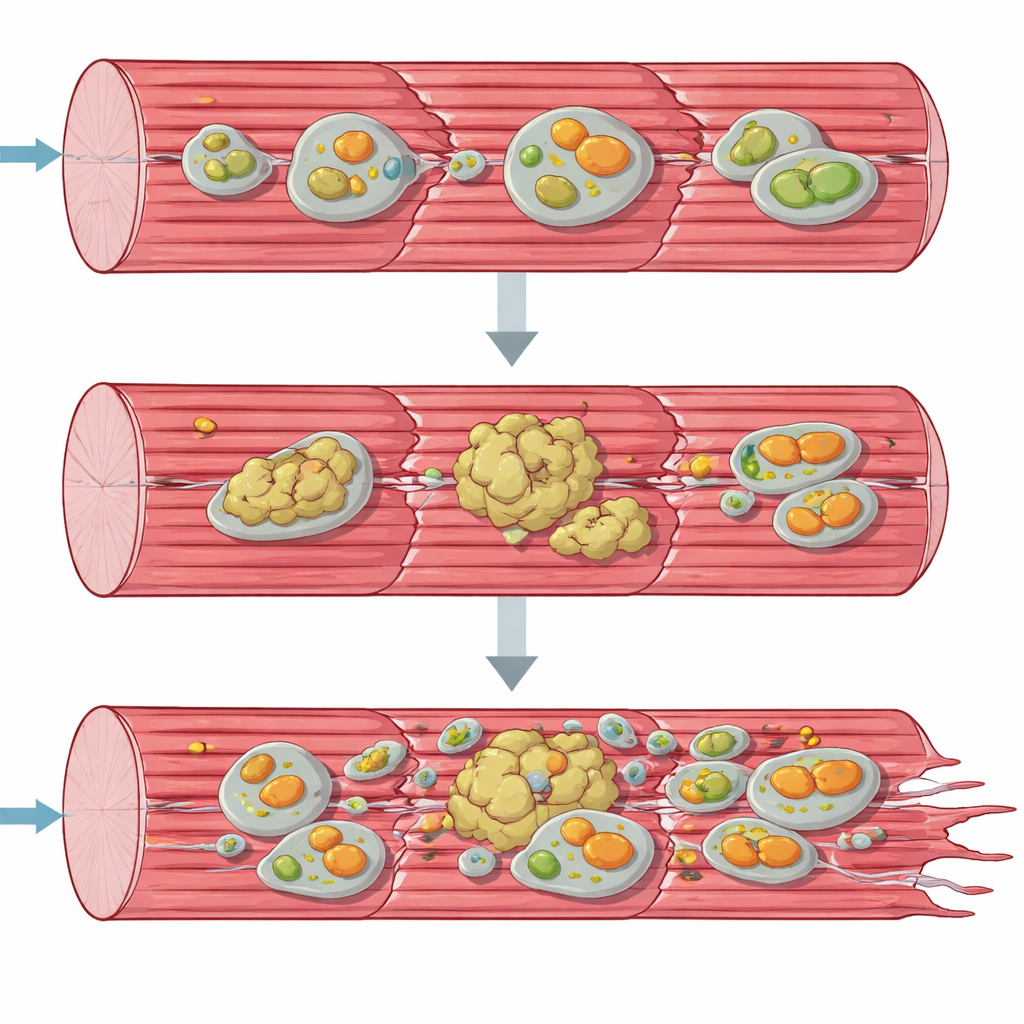
Accumulations protéiques et mitochondries malades
Pour comprendre la défaillance d’un point de vue systémique, l’équipe a eu recours à des outils « omiques » qui sondent des milliers de molécules à la fois. Les profils d’expression génique et protéique ont montré que les cellules musculaires tentaient frénétiquement de répondre : les gènes impliqués dans la fabrication de nouvelles protéines et dans les réponses au stress étaient upregulés, et de nombreuses chaperonnes et autres facteurs de contrôle qualité s’accumulaient. Pourtant, de nombreuses protéines structurelles clés de l’appareil contractile étaient appauvries dans leurs formes solubles normales et se retrouvaient plutôt dans une fraction insoluble, riche en agrégats. Parallèlement, des composants des voies de recyclage cellulaire — l’autophagie et l’élimination spécialisée des mitochondries endommagées, la mitophagie — s’accumulaient comme s’ils étaient coincés en cours de processus. La microscopie électronique et des tests de fonction mitochondriale ont confirmé que les organites producteurs d’énergie étaient déformés, regroupés et fonctionnaient bien en dessous de la capacité normale, en particulier à la première étape de la chaîne respiratoire.
L’autophagie comme coupable central
Les auteurs ont ensuite cherché à savoir si le problème principal résidait dans le recyclage cellulaire général (autophagie), dans le recyclage spécifique des mitochondries (mitophagie), ou dans les deux. Ils ont cultivé des cellules musculaires issues des souris mutantes et stimulé expérimentalement différentes voies. Stimuler l’autophagie générale avec la protéine BECN1 a effacé des marqueurs clés du stress, réduit les agrégats de BAG3 mutant et amélioré l’apparence et l’organisation des sarcomères. En revanche, forcer la mitophagie ou simplement augmenter la biogenèse mitochondriale n’a pas corrigé les défauts. Chez les souris vivantes, un traitement par la rapamycine, un activateur de l’autophagie, a amélioré la force de préhension, la coordination et la mobilité, et augmenté les marqueurs de recyclage actif dans le muscle. Ensemble, ces expériences indiquent un blocage primaire de l’autophagie, la détérioration mitochondriale apparaissant comme une conséquence secondaire plutôt que comme la cause initiale.
Tester une stratégie de thérapie génique
Parce que la maladie est provoquée par une protéine toxique, les chercheurs ont exploré si réduire le BAG3 mutant pouvait sauver les muscles. Ils ont emballé un court ARN en épingle à cheveux conçu pour cibler spécifiquement BAG3 humain dans un virus modifié et l’ont administré par voie sanguine à de jeunes souris mutantes. Quelques semaines plus tard, les muscles présentaient beaucoup moins de BAG3 mutant, moins d’agrégats protéiques, une fibrose réduite et beaucoup moins de fibres avec des noyaux centraux. Plus important encore, les muscles traités généraient sensiblement plus de force et retrouvaient partiellement une taille normale. Cette preuve de concept suggère que silencier le gène responsable de la maladie, ou combiner une telle approche avec des médicaments qui stimulent l’autophagie, pourrait constituer une stratégie puissante pour les patients, une fois qu’une thérapie alléle-spécifique sera optimisée.
Ce que cela signifie pour les patients et au-delà
En termes accessibles, ce travail montre que lorsqu’une protéine auxiliaire clé comme BAG3 se replie mal et s’agglutine, le système d’évacuation cellulaire se bloque. Les composants cassés et les mitochondries défaillantes s’accumulent, le échafaudage interne du muscle s’effondre et la force s’estompe. En recréant soigneusement la maladie chez la souris, l’étude révèle que restaurer ou contourner ce système de nettoyage — soit en renforçant l’autophagie, soit en réduisant le BAG3 mutant lui-même — peut rétablir substantiellement la santé musculaire. Bien qu’il reste beaucoup à faire avant que de tels traitements n’atteignent la clinique, ces découvertes fournissent une feuille de route détaillée pour s’attaquer à ce trouble musculaire rare mais mortel et offrent des perspectives plus larges sur la manière dont un défaut de l’entretien cellulaire pourrait sous-tendre d’autres maladies dégénératives.
Citation: Filippi, K., Graf-Riesen, K., Kuppusamy, M. et al. Blockage of autophagy causes severe skeletal muscle disruption in a mouse model for myofibrillar myopathy 6. Nat Commun 17, 3436 (2026). https://doi.org/10.1038/s41467-026-71749-6
Mots-clés: myopathie myofibrillaire, mutation BAG3, autophagie, dégénérescence du muscle squelettique, thérapie génique