Clear Sky Science · ar
انسداد البلعمة الذاتية يسبب اضطرابًا شدیدًا في العضلات الهيكلیة في نموذج فأري لاعتلال العضلات الليفي العضلي 6
عندما يتعطل طاقم التنظيف الخلوي
عضلاتنا تُصلِح نفسها باستمرار، وتُزيل بصمت الأجزاء المتهالكة حتى نتمكن من المشي والتنفس والتحرك دون تفكير. تستكشف هذه المقالة ما يحدث عندما ينهار نظام التنظيف الخلوي بسبب طفرة وراثية واحدة. النتيجة هي مرض عضلي طفولي مدمر يضعف الأطراف وعضلات التنفس. من خلال إنشاء نموذج فأري مفصل، لا يكتشف الباحثون فقط كيف يتكشف الضرر داخل خلايا العضلات، بل يختبرون أيضًا طرقًا لعكسه، مما يقدم بارقة أمل للعلاجات المستقبلية.
تركيز على مرض عضلي نادر
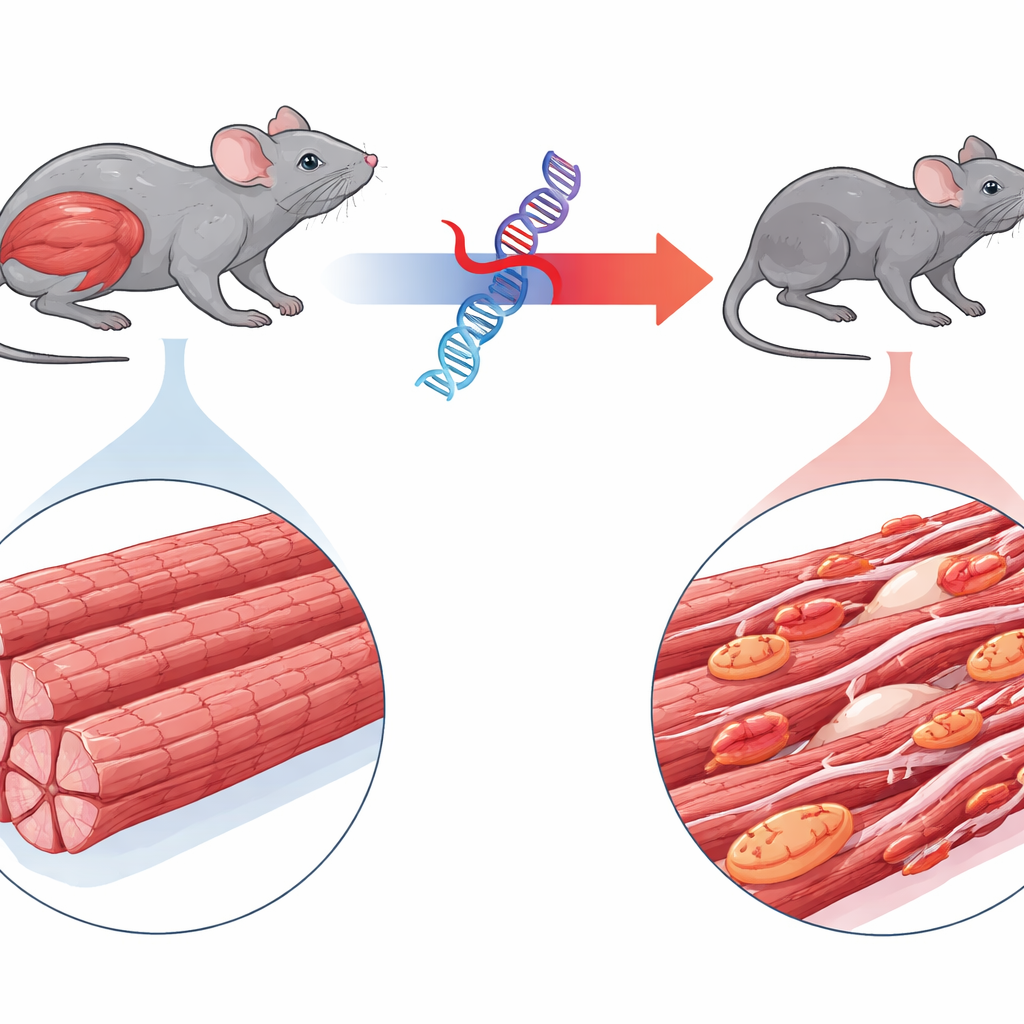
تركز الدراسة على اعتلال العضلات الليفي العضلي 6، اضطراب نادر ناتج عن طفرة في جين يُسمى BAG3. الأطفال المصابون بهذا الاضطراب يتطور لديهم ضعف عضلي عميق بسرعة، وأحيانًا مشاكل قلبية، وغالبًا يموتون في سن مبكرة نتيجة فشل التنفس. يعمل BAG3 عادةً كمشرف على جودة الوحدات الانقباضية الدقيقة داخل ألياف العضلات، موجِّهًا البروتينات التالفة نحو إعادة التدوير الخلوي. هندَس المؤلفون فئرانًا تُنتج الشكل البشري الطافر من BAG3 الموسوم بعلامة فلورية، مما أتاح لهم تتبُّع سلوكه. على عكس الفئران التي تُعبِّر عن BAG3 البشري الطبيعي، أصبحت الحيوانات الحاملة للصيغة الطافرة أصغر بسرعة، وأظهرت هزالًا في عضلات الأطراف والتنفس، ومشية متمايلة، بما يُطابق المرض البشري عن كثب.
كيف تنهار ألياف العضلات
كشفت الفحوص المجهرية وفحوص البنية الفائقة مدى تعطيل البروتين الطافر لبنية العضلة. في الفئران المتأثرة، كانت ألياف العضلات أنحف وممتلئة بتكتلات بروتينية غير طبيعية. كانت الخطوط المنظمة بدقة للآلية الانقباضية — الساركوميرات — متجزئة ومبهمة، وكثير من الألياف أظهرت نوى مركزية، وهو علامة مميزة لمحاولة التجدد. تسللت خلايا مناعية إلى النسيج وزاد نسيج الندبة الليفي، وإن كان بدرجة أقل مما حدث في القلب. وظيفيًا، أنتجت عضلات معزولة من هذه الفئران قوة أقل تصل إلى 90 بالمئة مقارنةً بتلك من حيوانات سليمة، حتى بعد احتساب صغر حجمها، مما يؤكد أن الآلية الأساسية للانقباض كانت تفشل.
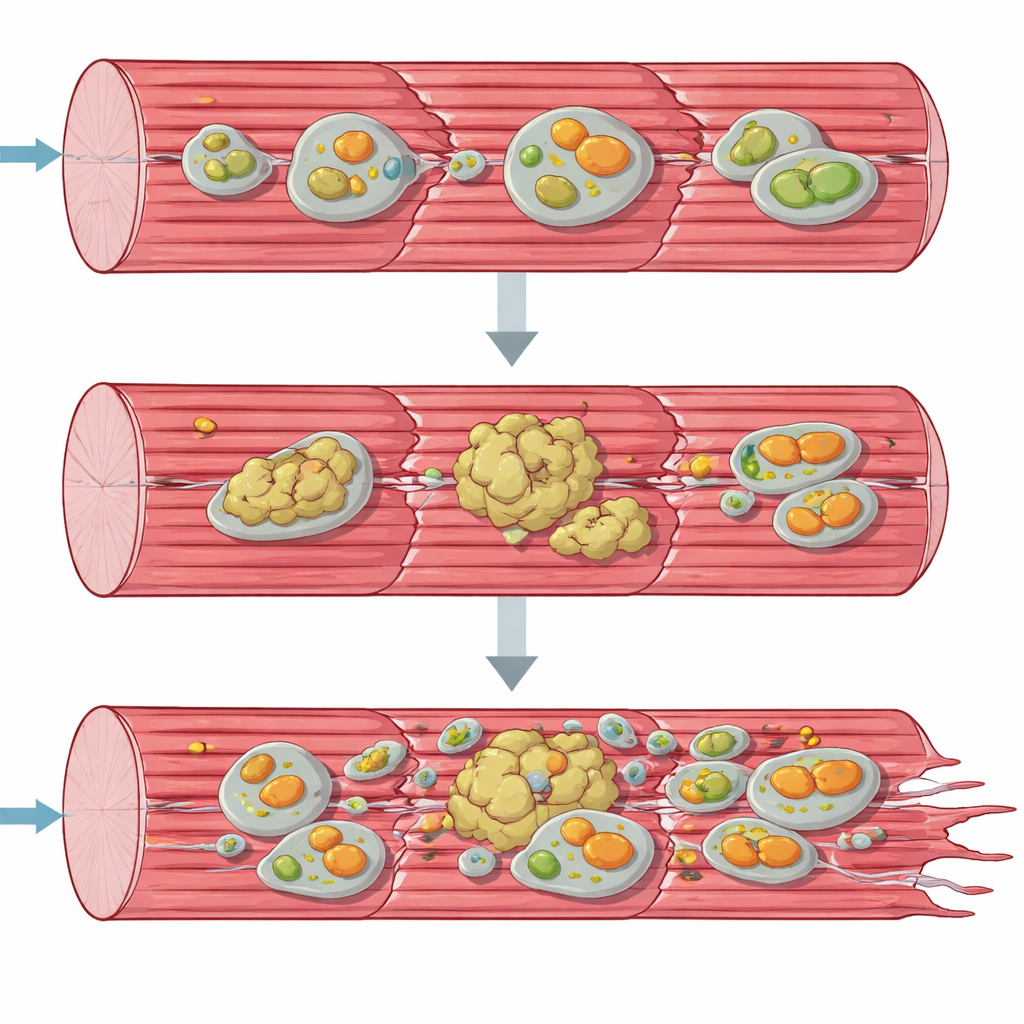
تراكم البروتينات والميتوكندريا المريضة
لفهم الانهيار من منظور أنظمة، لجأ الفريق إلى أدوات «الأوميكس» التي تفحص آلاف الجزيئات دفعة واحدة. أظهرت ملفات نشاط الجينات والبروتينات أن خلايا العضلات كانت تحاول الاستجابة بيأس: تزايدت تعبيرات جينات بناء البروتينات الجديدة والاستجابات الإجهادية، وتراكمت العديد من الشابرونات وعوامل ضبط الجودة الأخرى. ومع ذلك، نُقصت العديد من البروتينات البنائية الرئيسية للآلية الانقباضية من أشكالها المذابّة العادية وتحولت بدلًا من ذلك إلى جزء غير قابل للذوبان غني بالترسبات. في الوقت نفسه، تراكمت مكونات مسارات إعادة التدوير الخلوية — البلعمة الذاتية وإزالة الميتوكوندريا التالفة المتخصصة، الميتوفاجي — كما لو أنها توقفت في منتصف العملية. أكدت المجهر الإلكتروني واختبارات وظيفة الميتوكوندريا أن العضيات المولدة للطاقة كانت مشوهة ومجتمعة وتعمل بأداء أقل بكثير من الطبيعي، وخاصة في الخطوة الأولى من سلسلة التنفس.
البَلْعَمة الذاتية كالمتهم الرئيسي
سأل المؤلفون بعد ذلك ما إذا كانت المشكلة الأساسية تكمن في إعادة التدوير الخلوي العامة (البَلْعَمة الذاتية)، أو في إزالة الميتوكوندريا بشكل مُخصص (الميتوفاجي)، أو كلاهما. زرعوا خلايا عضلية من الفئران الطافرة وعزَّزوا تجريبيًا مسارات مختلفة. تحفيز البلعمة الذاتية العامة بالبروتين BECN1 أزال مؤشرات الإجهاد الرئيسية، وخفّض تجمعات BAG3 الطافرة، وحسّن مظهر وتنظيم الساركوميرات. في المقابل، لم تُصحِح إجبار الميتوفاجي أو زيادة إنتاج الميتوكوندريا العيوب. في الفئران الحية، حسن العلاج بالدواء المنشط للبلعمة الذاتية رابامايسين قوة القبضة والتنسيق والحركة، وزاد مؤشرات إعادة التدوير النشطة في العضلات. تشير هذه التجارب معًا إلى وجود عائق أولي في البلعمة الذاتية، مع ظهور تلف الميتوكوندريا كنتيجة ثانوية بدلًا من كونه سببًا جذريًا.
اختبار استراتيجية علاج جيني
لأن المرض يسببه بروتين سام، استكشف الباحثون ما إذا كان خفض مستوى BAG3 الطافر يمكن أن ينقذ العضلات. حزموا حمضًا نوويًا قصير التكوين على شكل دبوس شعر (short hairpin RNA) مصممًا لاستهداف BAG3 البشري بشكل محدد داخل فيروس مُعدَّل وسلموه إلى مجرى دم فئران صغيرة حاملة للطفرة. بعد أسابيع، أظهرت العضلات انخفاضًا كبيرًا في BAG3 الطافر، وتجمعات بروتينية أقل، وندوبًا أقل، وعددًا أقل بكثير من الألياف ذات النوى المركزية. والأهم من ذلك، أنتجت العضلات المعالجة قوة أكبر بكثير واستعادت جزئيًا حجمًا طبيعيًا. يشير هذا الإثبات المفاهيمي إلى أن إسكات الجين المسبب للمرض، أو الجمع بين مثل هذا النهج وأدوية تعزز البلعمة الذاتية، قد يكون استراتيجية قوية للمرضى بعد تحسين علاج محدد للحليفة (allele-specific therapy).
ماذا يعني هذا للمرضى وما بعده
بعبارات يسهل الوصول إليها، تُظهر هذه الدراسة أنه عندما يختل طي بروتين مساعد رئيسي مثل BAG3 ويتكتل، تتعطل آلة التخلص من النفايات في الخلية. تتراكم المكونات المكسورة والميتوكندريا المعيبة، ينهار السقالة الداخلية للعضلة، ويتراجع القوة. من خلال إعادة تكوين المرض بعناية في الفئران، تكشف الدراسة أنه يمكن لاستعادة هذا النظام التنظيفي أو تجاوزه — إما بتعزيز البلعمة الذاتية أو بتقليل BAG3 الطافر نفسه — أن يعيد بشكل كبير صحة العضلات. وبينما لا يزال هناك الكثير مما ينبغي عمله قبل أن تصل مثل هذه العلاجات إلى العيادات، توفر النتائج خارطة طريق مفصلة لمعالجة هذا الاضطراب العضلي النادر والقاتل وتقدم رؤى أوسع حول كيف قد تكون أعمال التنظيف الخلوي المعطلة أساسًا لأمراض تنكسية أخرى.
الاستشهاد: Filippi, K., Graf-Riesen, K., Kuppusamy, M. et al. Blockage of autophagy causes severe skeletal muscle disruption in a mouse model for myofibrillar myopathy 6. Nat Commun 17, 3436 (2026). https://doi.org/10.1038/s41467-026-71749-6
الكلمات المفتاحية: اعتلال العضلات الليفي العضلي, طفرة BAG3, البلعمة الذاتية, انحلال العضلات الهيكلية, العلاج الجيني