Clear Sky Science · nl
Blokkade van autophagie veroorzaakt ernstige verstoring van skeletspieren in een muismodel voor myofibrillaire myopathie 6
Als de opruimploeg van de cel faalt
Onze spieren herstellen zich voortdurend en ruimen ongemerkt versleten onderdelen op, zodat we kunnen lopen, ademen en bewegen zonder erbij na te denken. Dit artikel onderzoekt wat er gebeurt wanneer dat cellulaire opruimsysteem faalt door een enkele erfelijke mutatie. Het resultaat is een verwoestende spierziekte van de kindertijd die ledematen en ademhalingsspieren verzwakt. Door een gedetailleerd muismodel te bouwen, onthullen de onderzoekers niet alleen hoe de schade zich binnen spiercellen ontvouwt, maar testen ze ook manieren om die om te keren, wat een sprankje hoop biedt voor toekomstige therapieën.
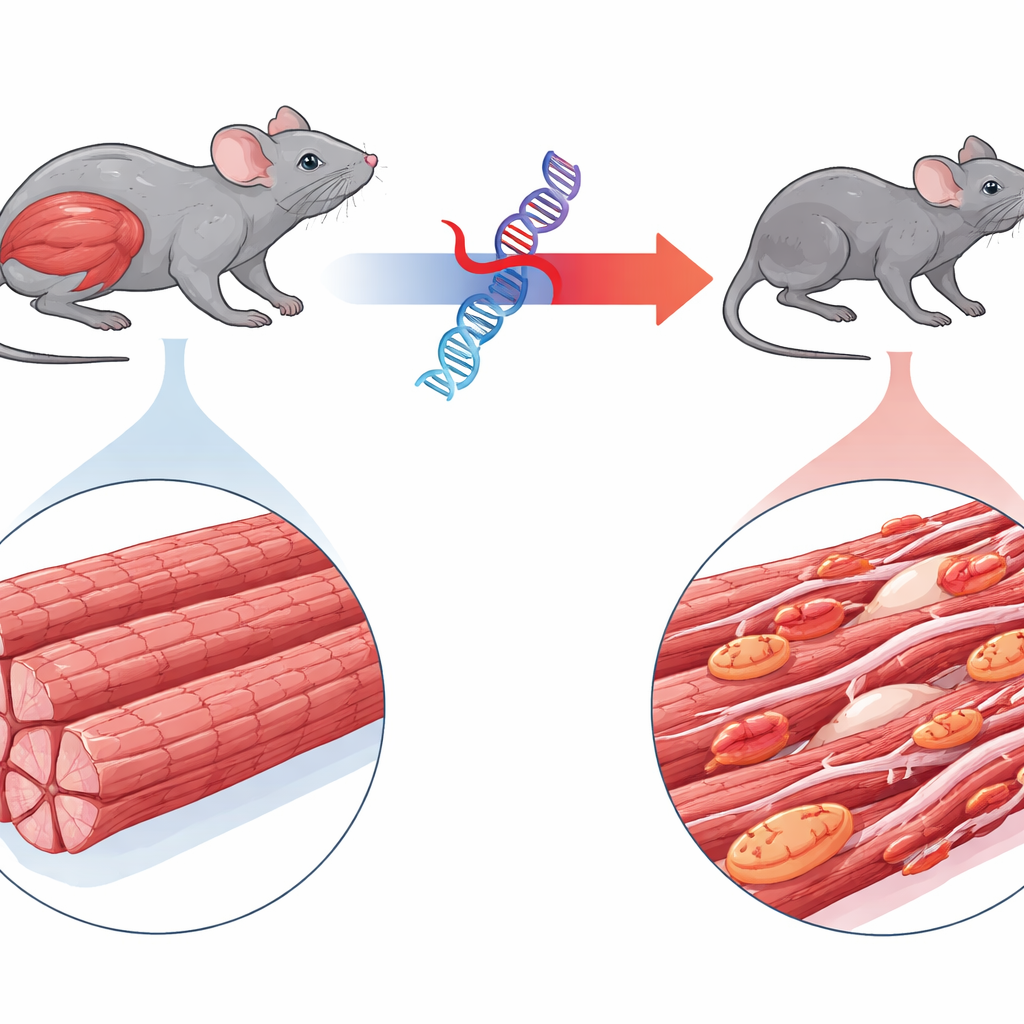
Een zeldzame spierziekte onder de loep
De studie richt zich op myofibrillaire myopathie 6, een zeldzame aandoening veroorzaakt door een mutatie in een gen genaamd BAG3. Kinderen met deze aandoening ontwikkelen snel ernstige spierzwakte, soms hartproblemen, en sterven vaak op jonge leeftijd aan ademhalingsfalen. BAG3 helpt normaal gesproken bij het bewaken van de kwaliteit van de kleine contractiele eenheden binnen spiervezels en stuurt beschadigde eiwitten naar de cellulaire recycling. De auteurs maakten muizen die de menselijke gemuteerde vorm van BAG3 produceren, uitgerust met een fluorescerende marker, zodat ze het gedrag konden volgen. In tegenstelling tot muizen die normaal menselijk BAG3 uitdrukken, werden dieren met de gemuteerde versie snel kleiner, vertoonden ze verlies van ledemaat- en ademhalingsspieren en hadden ze een wijdbeende gang, wat nauw aansluit bij de menselijke ziekte.
Hoe spiervezels uit elkaar vallen
Microscopische en ultrastructurale onderzoeken toonden aan hoe grondig het gemuteerde eiwit de spierstructuur verstoort. Bij getroffen muizen waren spiervezels dunner en vol met abnormale eiwitklonters. De sterk geordende strepen van het contractiele apparaat—de sarcomeren—waren gefragmenteerd en vervaagd, en veel vezels vertoonden gecentraliseerde kernen, een kenmerk van poging tot regeneratie. Immuuncellen drongen het weefsel binnen en het vezelige littekenweefsel nam toe, al minder dramatisch dan in het hart. Functioneel produceerden geïsoleerde spieren van deze muizen tot 90 procent minder kracht dan die van gezonde dieren, zelfs na correctie voor hun kleinere grootte, wat bevestigt dat het kernmachinerie voor samentrekking faalde.
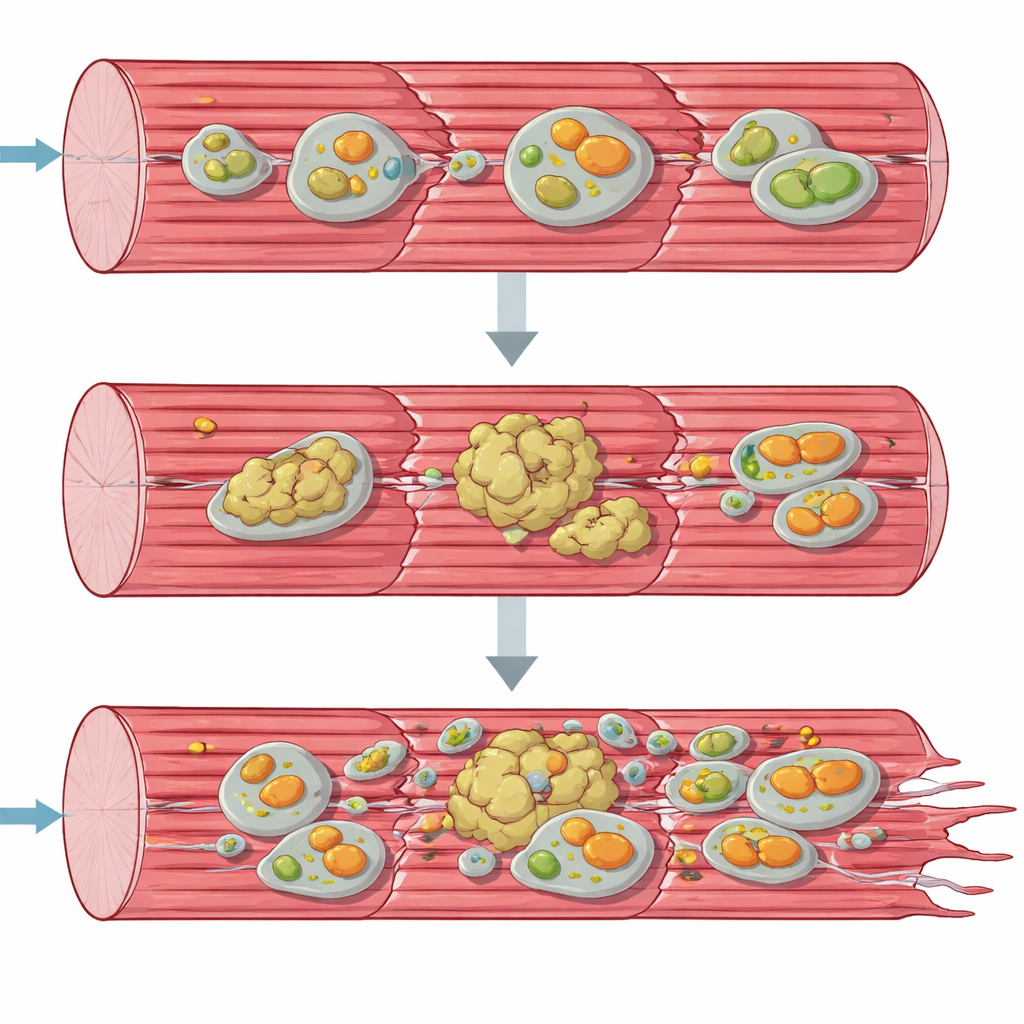
Eiwitstapels en zieke mitochondriën
Om het verval vanuit een systeemprestatie te begrijpen, gebruikte het team “omics”-tools die duizenden moleculen tegelijk onderzoeken. Genactiviteit en eiwitprofielen lieten zien dat spiercellen koortsachtig probeerden te reageren: genen voor het aanmaken van nieuwe eiwitten en voor stresreacties waren opgevoerd, en veel chaperonnes en andere kwaliteitscontrolefactoren stapelden zich op. Toch raakten veel belangrijke structurele eiwitten van het contractiele apparaat ontdaan van hun normale oplosbare vormen en verschooften ze naar een onoplosbare, aggregate-rijke fractie. Tegelijkertijd stapelden componenten van de cellulaire recyclingpaden—autofagie en de gespecialiseerde verwijdering van beschadigde mitochondriën, mitofagie—zich op alsof ze vastzaten halverwege het proces. Elektronenmicroscopie en tests van mitochondriale functie bevestigden dat energieproducerende organellen misvormd, geclusterd waren en veel minder goed functioneerden dan normaal, vooral in de eerste stap van de ademhalingsketen.
Autofagie als centrale boosdoener
De auteurs vroegen zich vervolgens af of het primaire probleem lag in algemene cellulaire recycling (autofagie), in mitochondriumspecifieke recycling (mitofagie), of in beide. Ze kweekten spiercellen van de gemuteerde muizen en versterkten experimenteel verschillende paden. Het stimuleren van brede autofagie met het eiwit BECN1 verwijderde belangrijke stressmarkers, verminderde mutant BAG3-aggregaten en verbeterde het uiterlijk en de organisatie van sarcomeren. Ter vergelijking: het forceren van mitofagie of alleen het verhogen van de mitochondriale productie corrigeerde de defecten niet. In levende muizen verbeterde behandeling met het autofagie-activerende middel rapamycine de grijpkracht, coördinatie en beweging, en verhoogde markers van actieve recycling in spier. Samen wijzen deze experimenten op een primaire blokkade in autofagie, waarbij mitochondriale schade optreedt als een secundair gevolg in plaats van de hoofdoorzaak.
Het testen van een gentherapie-strategie
Aangezien de ziekte wordt aangedreven door een toxisch eiwit, onderzochten de onderzoekers of het terugschakelen van mutant BAG3 de spieren zou kunnen redden. Ze verpakten een short hairpin RNA ontworpen om specifiek humaan BAG3 te richten in een ontworpen virus en brachten dit via de bloedbaan in bij jonge gemuteerde muizen. Weken later toonden spieren veel minder mutant BAG3, minder eiwitaggregaten, verminderde verharding en veel minder vezels met gecentraliseerde kernen. Het belangrijkst: behandelde spieren genereerden dramatisch meer kracht en herkregen gedeeltelijk hun normale grootte. Dit proof-of-concept suggereert dat het uitschakelen van het ziekteveroorzakende gen, of het combineren van zo’n benadering met geneesmiddelen die autofagie stimuleren, een krachtige strategie voor patiënten kan zijn zodra een alleelspecifieke therapie is geoptimaliseerd.
Wat dit betekent voor patiënten en daarbuiten
In toegankelijke termen laat dit werk zien dat wanneer een belangrijke helper-eiwit zoals BAG3 verkeerd vouwt en klontert, het afvalsysteem van de cel vastloopt. Gebroken componenten en defecte mitochondriën hopen zich op, het interne skelet van de spier stort in en de kracht slinkt. Door de ziekte zorgvuldig in muizen te recreëren, toont de studie aan dat het herstellen of omzeilen van dit opruimsysteem—hetzij door autofagie te versterken, hetzij door het verminderen van mutant BAG3 zelf—de spiergezondheid aanzienlijk kan herstellen. Hoewel er nog veel moet gebeuren voordat zulke behandelingen de kliniek bereiken, bieden de bevindingen een gedetailleerde routekaart voor het aanpakken van deze zeldzame maar dodelijke spierziekte en geven ze bredere inzichten in hoe verstoord cellair huishouding ten grondslag kan liggen aan andere degeneratieve aandoeningen.
Bronvermelding: Filippi, K., Graf-Riesen, K., Kuppusamy, M. et al. Blockage of autophagy causes severe skeletal muscle disruption in a mouse model for myofibrillar myopathy 6. Nat Commun 17, 3436 (2026). https://doi.org/10.1038/s41467-026-71749-6
Trefwoorden: myofibrillaire myopathie, BAG3-mutatie, autofagie, degeneratie van skeletspieren, gentherapie