Clear Sky Science · sv
Blockering av autofagi orsakar svår skelettmuskeldestruktion i en musmodell för myofibrillär myopati 6
När cellens städpatrull fallerar
Våra muskler reparerar sig ständigt, tyst rensande bort utslitna komponenter så att vi kan gå, andas och röra oss utan att tänka på det. Den här artikeln utforskar vad som händer när det cellulära städsystemet kollapsar på grund av en enda ärftlig mutation. Resultatet är en förödande barndomssjukdom i muskler som försvagar lemmar och andningsmuskulatur. Genom att bygga en detaljerad musmodell avslöjar forskarna inte bara hur skadan utvecklas inne i muskelfibrerna, utan testar också sätt att vända den — vilket ger ett strimma hopp för framtida behandlingar.
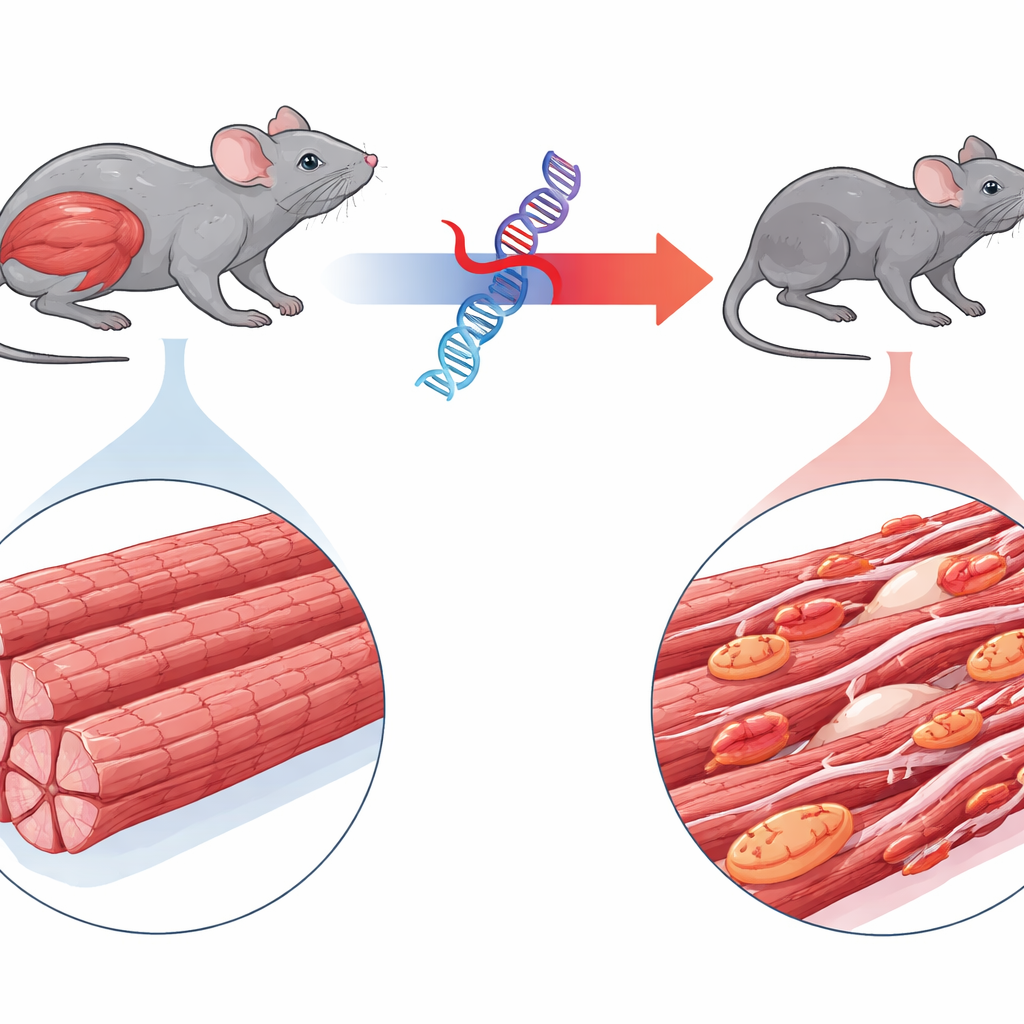
En sällsynt muskelsjukdom i fokus
Studien kretsar kring myofibrillär myopati 6, en sällsynt störning orsakad av en mutation i ett gen som kallas BAG3. Barn med detta tillstånd utvecklar snabbt djup muskelsvaghet, ibland hjärtproblem, och dör ofta unga av andningssvikt. BAG3 hjälper normalt till att övervaka kvaliteten på de små kontraktila enheterna inne i muskelfibrerna och dirigerar skadade proteiner till cellens återvinningssystem. Författarna konstruerade möss som producerar den humana mutanta formen av BAG3 märkt med en fluorescerande markör, vilket gjorde det möjligt att följa dess beteende. Till skillnad från möss som uttrycker normal human BAG3 blev djuren med den mutanta versionen snabbt mindre, visade förtvinade lemmar och andningsmuskler, och hade ett vaggande gångsätt — en bild som starkt speglar den mänskliga sjukdomen.
Hur muskelfibrer faller sönder
Mikroskopiska och ultrastrukturella undersökningar visade hur grundligt den mutanta proteinet stör muskelsstrukturen. Hos drabbade möss var muskelfibrerna tunnare och fyllda med onormala proteinansamlingar. De högordnade strimmorna i det kontraktila maskineriet — sarkomererna — var fragmenterade och suddiga, och många fibrer visade centrala kärnor, ett kännetecken för försök till regenerering. Immunceller infiltrerade vävnaden och fibröst ärrmaterial ökade, om än mindre dramatiskt än i hjärtat. Funktionsmässigt producerade isolerade muskler från dessa möss upp till 90 procent mindre kraft än de från friska djur, även efter att man tagit hänsyn till deras mindre storlek, vilket bekräftar att det centrala kontraktionsmaskineriet sviktade.
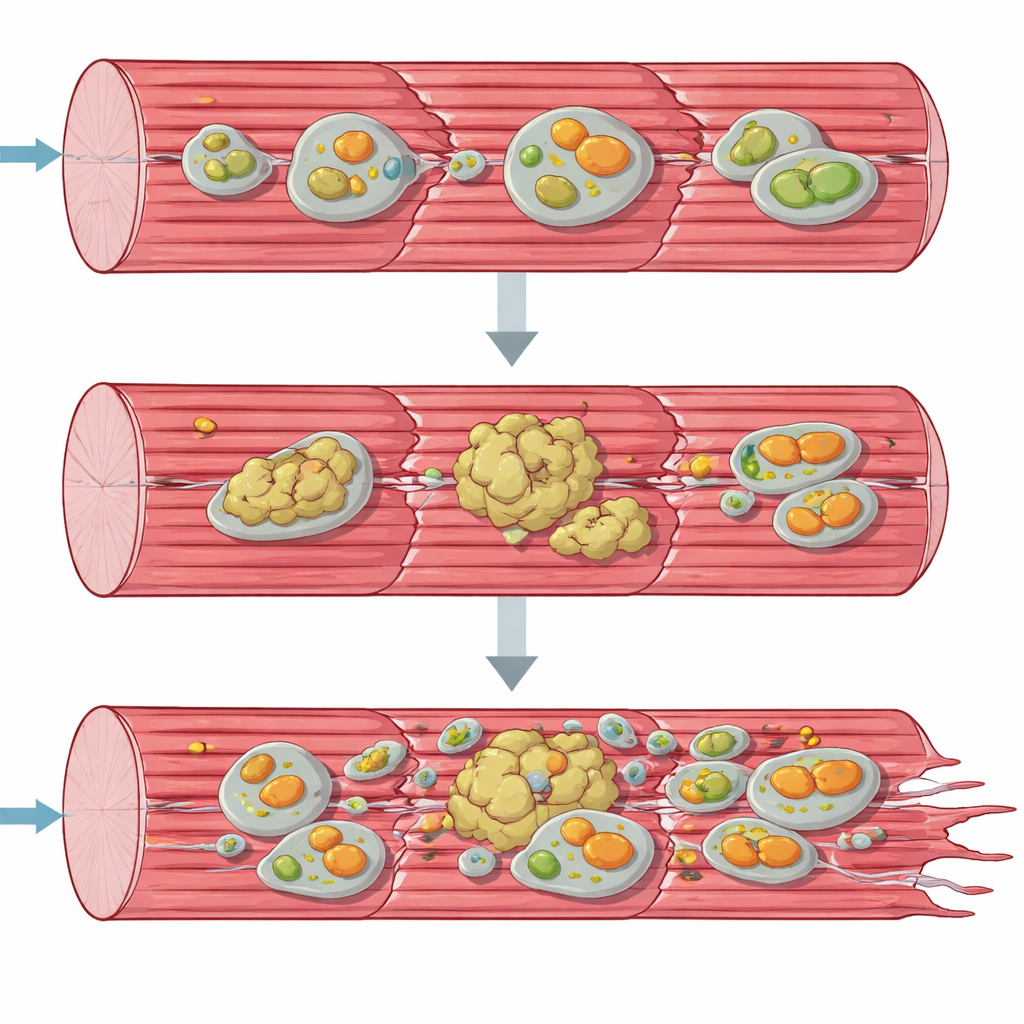
Proteinansamlingar och sjuka mitokondrier
För att förstå sammanbrottet ur ett systemperspektiv använde teamet "omik"-verktyg som kartlägger tusentals molekyler samtidigt. Genaktivitet och proteinnivåer visade att muskelfibrerna febrilt försökte svara: gener för att bygga nya proteiner och stressresponser var uppreglerade, och många chaperoner och andra kvalitetskontrollfaktorer ackumulerades. Ändå var många nyckelstrukturella proteiner i det kontraktila apparaten uttömda i sina normala lösliga former och hade istället förskjutits till en olöslig, aggregatrik fraktion. Samtidigt byggdes komponenter i cellens återvinningsvägar — autofagi och den specialiserade borttagningen av skadade mitokondrier, mitofagi — upp som om de fastnat mitt i processen. Elektronmikroskopi och tester av mitokondriell funktion bekräftade att energiproducerande organeller var missformade, klustrade och arbetade långt under normal kapacitet, särskilt vid det första steget i andningskedjan.
Autofagi som huvudorsak
Författarna frågade sedan om det primära problemet låg i det breda cellulära återvinningssystemet (autofagi), i mitokondriespecifik återvinning (mitofagi), eller båda. De odlade muskeceller från de mutanta mössen och förstärkte experimentellt olika vägar. Att stimulera bred autofagi med proteinet BECN1 rensade bort viktiga stressmarkörer, minskade aggregat av mutanta BAG3 och förbättrade sarkomernas utseende och organisation. I kontrast korrigerade inte tvingad mitofagi eller enbart ökad mitokondrieproduktion defekterna. Hos levande möss förbättrade behandling med det autofagiaktiverande läkemedlet rapamycin greppstyrka, koordination och rörelse, och ökade markörer för aktiv återvinning i muskeln. Tillsammans pekar dessa experiment mot ett primärt block i autofagi, där mitokondrieskador framträder som en sekundär följd snarare än grundorsaken.
Test av en genterapistrategi
Eftersom sjukdomen drivs av ett toxiskt protein undersökte forskarna om nedreglering av mutanta BAG3 kunde rädda musklerna. De förpackade en short hairpin-RNA utformad för att specifikt rikta in sig på human BAG3 i ett konstruerat virus och levererade det i blodomloppet hos unga mutanta möss. Veckor senare visade musklerna betydligt mindre mutant BAG3, färre proteinaggregat, minskad ärrbildning och långt färre fibrer med centrala kärnor. Viktigast av allt genererade behandlade muskler dramatiskt mer kraft och återfick delvis normal storlek. Detta proof-of-concept tyder på att tystande av den sjukdomsframkallande genen, eller att kombinera en sådan strategi med läkemedel som stimulerar autofagi, kan vara en kraftfull strategi för patienter när en allelspecifik behandling optimerats.
Vad detta betyder för patienter och vidare
På ett tillgängligt sätt visar arbetet att när ett nyckelhjälpprotein som BAG3 felveckas och klumpar sig, kärvar cellens sopmaskineri. Trasiga komponenter och defekta mitokondrier samlas, musklernas interna stomme kollapsar och styrkan avtar. Genom att noggrant återskapa sjukdomen i möss visar studien att återställande eller kringgående av detta städsystem — antingen genom att öka autofagin eller genom att reducera mutant BAG3 självt — kan återställa muskelhälsan i hög grad. Även om mycket återstår innan sådana behandlingar når kliniken, ger fynden en detaljerad färdplan för att ta itu med denna sällsynta men dödliga muskelsjukdom och ger bredare insikter i hur nedsatt cellulärt hushållsarbete kan ligga bakom andra degenerativa sjukdomar.
Citering: Filippi, K., Graf-Riesen, K., Kuppusamy, M. et al. Blockage of autophagy causes severe skeletal muscle disruption in a mouse model for myofibrillar myopathy 6. Nat Commun 17, 3436 (2026). https://doi.org/10.1038/s41467-026-71749-6
Nyckelord: myofibrillär myopati, BAG3-mutation, autofagi, degeneration av skelettmuskulatur, genteknik