Clear Sky Science · pt
Bloqueio da autofagia causa grave desorganização do músculo esquelético em um modelo murino da miofibrilar miopatia 6
Quando a equipe de limpeza da célula falha
Nossos músculos estão constantemente se reparando, eliminando silenciosamente partes desgastadas para que possamos caminhar, respirar e nos mover sem pensar. Este artigo explora o que acontece quando esse sistema celular de limpeza se rompe por causa de uma única mutação hereditária. O resultado é uma doença muscular infantil devastadora que enfraquece os membros e os músculos respiratórios. Ao construir um modelo murino detalhado, os pesquisadores não apenas revelam como o dano se desenvolve dentro das células musculares, mas também testam maneiras de revertê‑lo, oferecendo uma fagulha de esperança para terapias futuras.
Uma doença muscular rara em foco
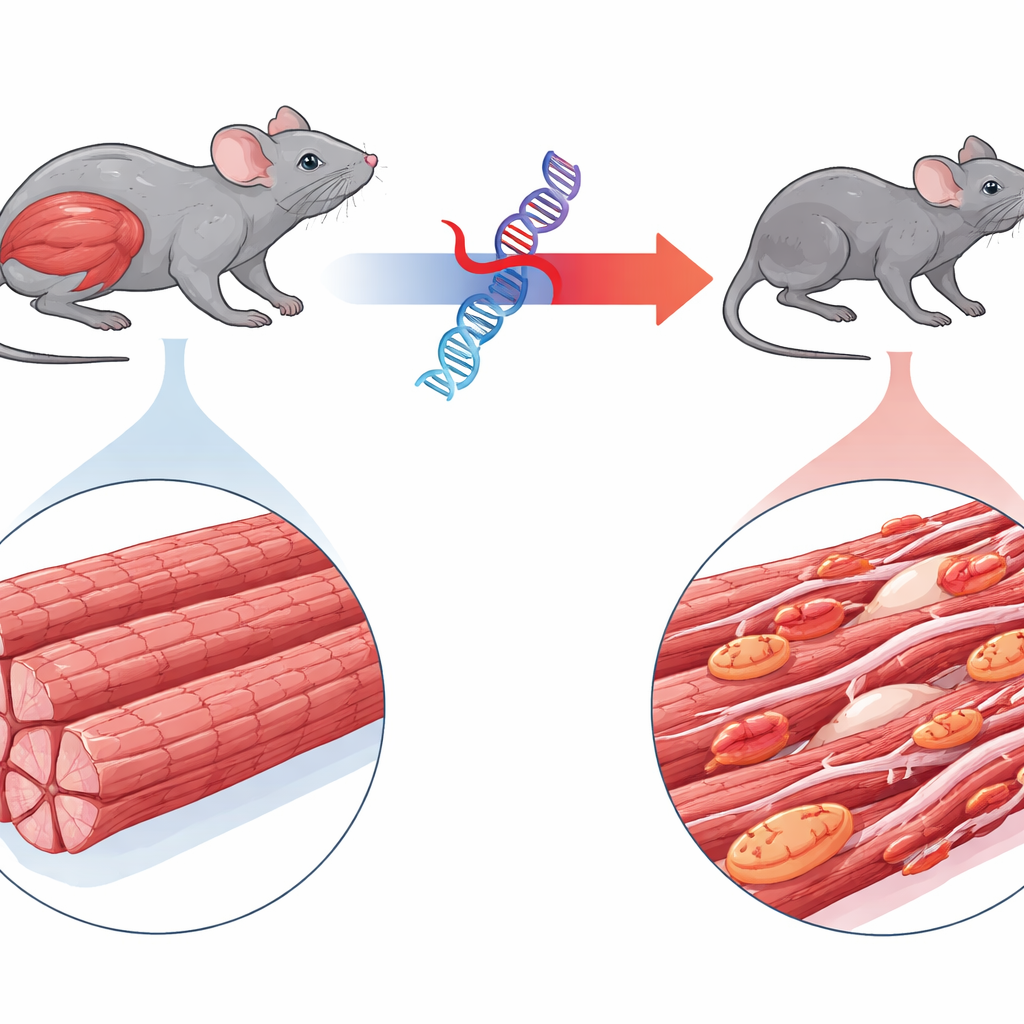
O estudo centra‑se na miofibrilar miopatia 6, um distúrbio raro causado por uma mutação em um gene chamado BAG3. Crianças com essa condição desenvolvem rapidamente fraqueza muscular profunda, às vezes problemas cardíacos, e frequentemente morrem jovens por insuficiência respiratória. O BAG3 normalmente ajuda a supervisionar a qualidade das pequenas unidades contráteis dentro das fibras musculares, direcionando proteínas danificadas para a reciclagem celular. Os autores produziram camundongos que expressam a forma humana mutante do BAG3 marcada com um marcador fluorescente, permitindo rastrear seu comportamento. Ao contrário dos camundongos que expressam o BAG3 humano normal, os animais com a versão mutante rapidamente ficaram menores, apresentaram perda de massa nos músculos dos membros e respiratórios e desenvolveram um andar bamboleante, espelhando de perto a doença humana.
Como as fibras musculares se desfazem
Exames microscópicos e ultrastruturais revelaram o quão profundamente a proteína mutante desorganiza a estrutura muscular. Nos camundongos afetados, as fibras musculares estavam mais finas e repletas de agregados proteicos anormais. As faixas altamente ordenadas da maquinaria contrátil — os sarcômeros — estavam fragmentadas e borradas, e muitas fibras apresentavam núcleos centralizados, um marco de tentativa de regeneração. Células imunes infiltraram o tecido e o material fibroso cicatricial aumentou, embora em grau menor do que no coração. Funcionalmente, músculos isolados desses camundongos produziram até 90% menos força do que os de animais saudáveis, mesmo depois de ajustar para o menor tamanho, confirmando que a máquina central de contração estava falhando.
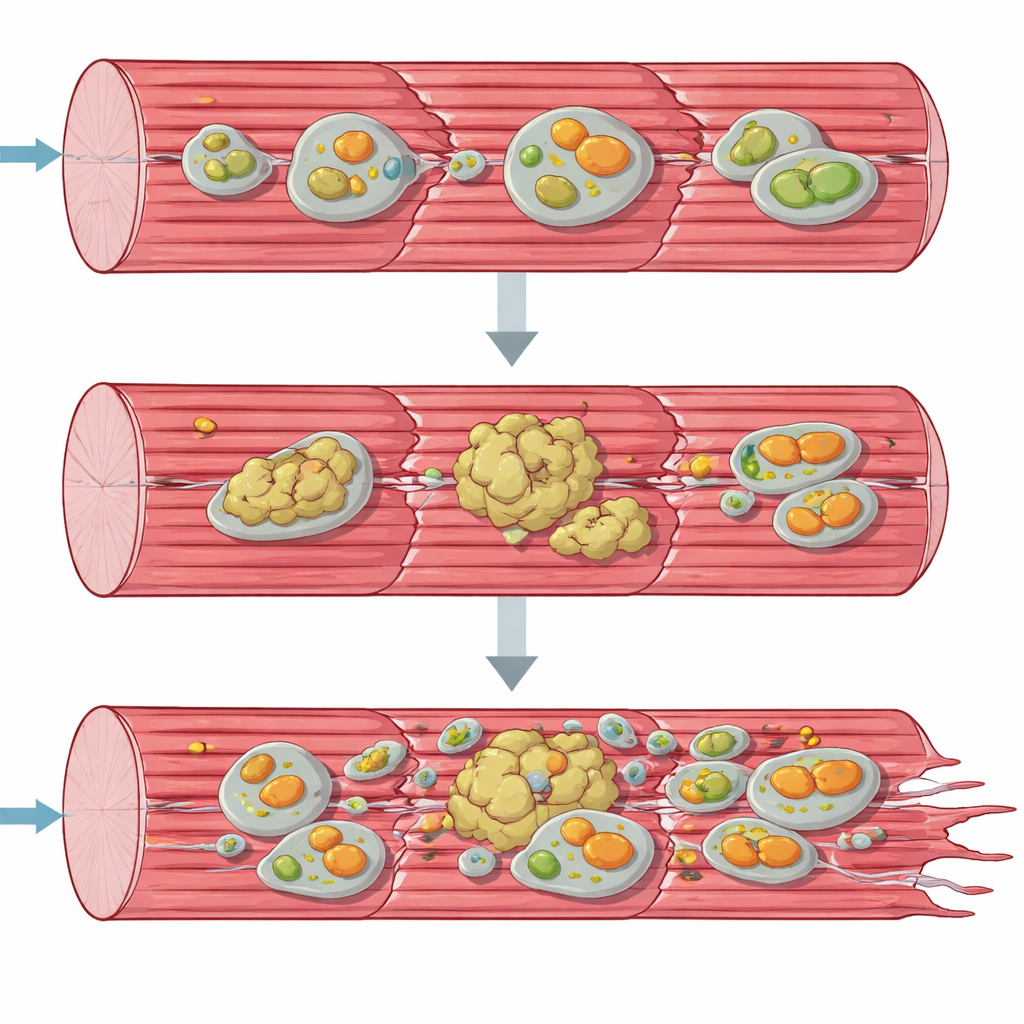
Acúmulos de proteína e mitocôndrias doentes
Para entender a quebra em uma visão de sistemas, a equipe recorreu a ferramentas “ômicas” que analisam milhares de moléculas de uma vez. A atividade gênica e os perfis proteicos mostraram que as células musculares estavam tentando responder freneticamente: genes para síntese proteica e respostas ao estresse estavam ativados, e muitas chaperonas e outros fatores de controle de qualidade se acumularam. Ainda assim, muitas proteínas estruturais-chave do aparelho contrátil estavam esgotadas em suas formas solúveis normais e deslocadas para uma fração insolúvel rica em agregados. Ao mesmo tempo, componentes das vias de reciclagem celular — autofagia e a remoção especializada de mitocôndrias danificadas, a mitofagia — acumulavam‑se como se ficassem presos a meio caminho do processo. Microscopia eletrônica e testes de função mitocondrial confirmaram que as organelas produtoras de energia estavam deformadas, agrupadas e funcionando muito abaixo da capacidade normal, especialmente no primeiro passo da cadeia respiratória.
Autofagia como o culpado central
Os autores então investigaram se o problema primário residia na reciclagem celular geral (autofagia), na reciclagem específica de mitocôndrias (mitofagia) ou em ambos. Eles cultivaram células musculares dos camundongos mutantes e ativaram experimentalmente diferentes vias. Estimular a autofagia ampla com a proteína BECN1 eliminou marcadores chave de estresse, reduziu agregados do BAG3 mutante e melhorou a aparência e a organização dos sarcômeros. Em contraste, forçar a mitofagia ou simplesmente aumentar a produção de mitocôndrias não corrigiu os defeitos. Em camundongos vivos, o tratamento com o fármaco ativador da autofagia rapamicina melhorou a força de preensão, a coordenação e o movimento, e aumentou marcadores de reciclagem ativa no músculo. Em conjunto, esses experimentos indicam um bloqueio primário na autofagia, com o dano mitocondrial emergindo como uma consequência secundária em vez da causa raiz.
Testando uma estratégia de terapia gênica
Como a doença é conduzida por uma proteína tóxica, os pesquisadores exploraram se reduzir o BAG3 mutante poderia resgatar os músculos. Eles embalaram um RNA em alça curta (short hairpin RNA) projetado para mirar especificamente o BAG3 humano em um vírus engenheirado e o administraram na corrente sanguínea de camundongos jovens mutantes. Semanas depois, os músculos apresentaram muito menos BAG3 mutante, menos agregados proteicos, cicatrização reduzida e muito menos fibras com núcleos centralizados. O mais importante, os músculos tratados geraram muito mais força e recuperaram parcialmente o tamanho normal. Esta prova de conceito sugere que silenciar o gene causador da doença, ou combinar tal abordagem com drogas que aumentem a autofagia, pode ser uma estratégia poderosa para pacientes, uma vez que uma terapia específica de alelo seja otimizada.
O que isso significa para pacientes e além
Em termos acessíveis, este trabalho mostra que quando uma proteína auxiliar chave como o BAG3 se dobra mal e forma aglomerados, o sistema de descarte da célula emperra. Componentes quebrados e mitocôndrias defeituosas se acumulam, o andaime interno do músculo colapsa e a força diminui. Ao recriar cuidadosamente a doença em camundongos, o estudo revela que restaurar ou contornar esse sistema de limpeza — seja aumentando a autofagia ou reduzindo o BAG3 mutante — pode restaurar substancialmente a saúde muscular. Embora ainda haja muito a fazer antes que tais tratamentos cheguem à clínica, as descobertas fornecem um roteiro detalhado para enfrentar esse transtorno muscular raro, porém letal, e oferecem insights mais amplos sobre como a falha na manutenção celular pode fundamentar outras doenças degenerativas.
Citação: Filippi, K., Graf-Riesen, K., Kuppusamy, M. et al. Blockage of autophagy causes severe skeletal muscle disruption in a mouse model for myofibrillar myopathy 6. Nat Commun 17, 3436 (2026). https://doi.org/10.1038/s41467-026-71749-6
Palavras-chave: miofibrilar miopatia, mutação em BAG3, autofagia, degeneração do músculo esquelético, terapia gênica