Clear Sky Science · he
חסימה של אוטופאגיה גורמת להרס חמור של שריר שלד במודל עכבר למיו-פיברילר מיאופתיה 6
כשצוות הניקיון התאי נכשל
השרירים שלנו מתחדשים באופן רציף, מנקים בשקט רכיבים בלויים כדי שנוכל ללכת, לנשום ולנוע ללא מחשבה. מאמר זה חוקר מה קורה כשהמערכת הזו של ניקוי תאי מתמוטטת בעקבות מוטציה תורשתית יחידה. התוצאה היא מחלת שרירים ילדים קשה שמחלה את הגפיים ושרירי הנשימה. על ידי בניית מודל עכבר מפורט, החוקרים לא רק חושפים איך הנזק מתפתח בתוך תאי השריר, אלא גם בודקים דרכים להפוך אותו — ומציעים ניצוץ של תקווה לטיפולים עתידיים.
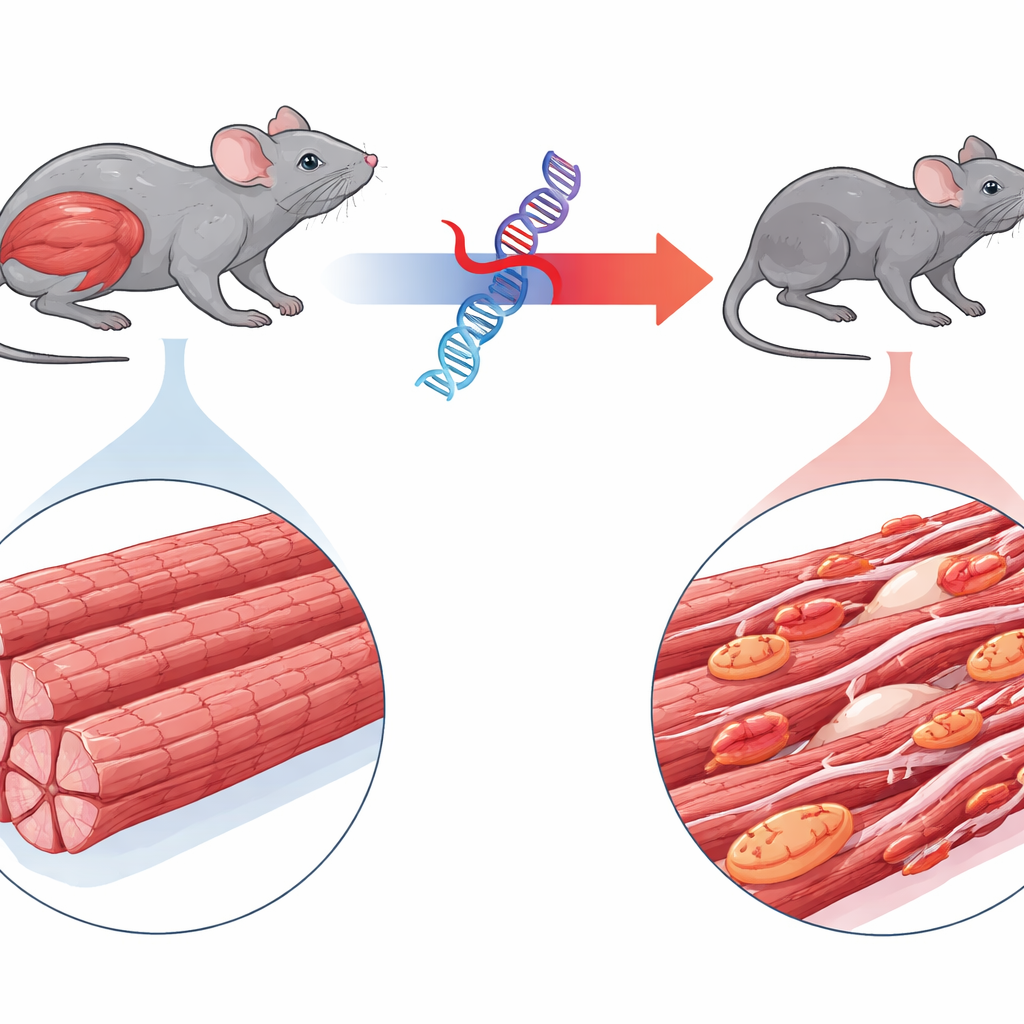
מחלת שריר נדירה במרכז התמונה
המחקר מתרכז במיו-פיברילר מיאופתיה 6, הפרעה נדירה הנגרמת על ידי מוטציה בגן בשם BAG3. ילדים עם מצב זה מפתחים במהירות חולשת שרירים עמוקה, לעתים בעיות לב, ולעיתים רבים מתים צעירים מכישלון נשימתי. BAG3 בדרך כלל מסייעת לפקח על איכות היחידות החוזרות הקטנות בתוך סיבי השריר, ומנותבת חלבונים פגומים למחזור תאית. החוקרים מהנדסים עכברים שמייצרים את הצורה האנושית המוטנטית של BAG3 מסומנת בסמן פלורסנטי, ומאפשרים להם לעקוב אחרי התנהגותה. בניגוד לעכברים המבטאים BAG3 אנושית תקינה, בעלי החיים עם הגרסה המוטנטית הפכו במהירות לקטנים יותר, הראו אטרופיה של שרירי גפיים ונשימה, והליכה מתנדנדת, מה שהדהד בקירוב את המחלה האנושית.
איך סיבי השריר מתמוטטים
בדיקות מיקרוסקופיות ואולטרה-מבניות חשפו עד כמה החלבון המוטנטי משבש את מבנה השריר. בעכברים מושפעים, סיבי השריר היו דקים יותר ומלאים בגושים חלבוניים חריגים. הפסיפסים המסודרים של המכונה הכיווצית — הסרקומרים — היו מפורקים ומטושטשים, והרבה סיבים הציגו גרעינים ממוקמים במרכז, סימן לנסותת שיקום. תאים חיסוניים חדרו ברקמה והחומר הצלקתי הסיבי גדל, אם כי בפחות דרמטיות מאשר בלב. בפן התפקודי, שרירים מבודדים מעכברים אלו ייצרו עד 90 אחוז פחות כוח בהשוואה לאלה מעכברים בריאים, אפילו בהתחשב בגודלם הקטן יותר, מה שאישר שהמכונה המרכזית לכיווץ מפסיקה לפעול כהלכה.
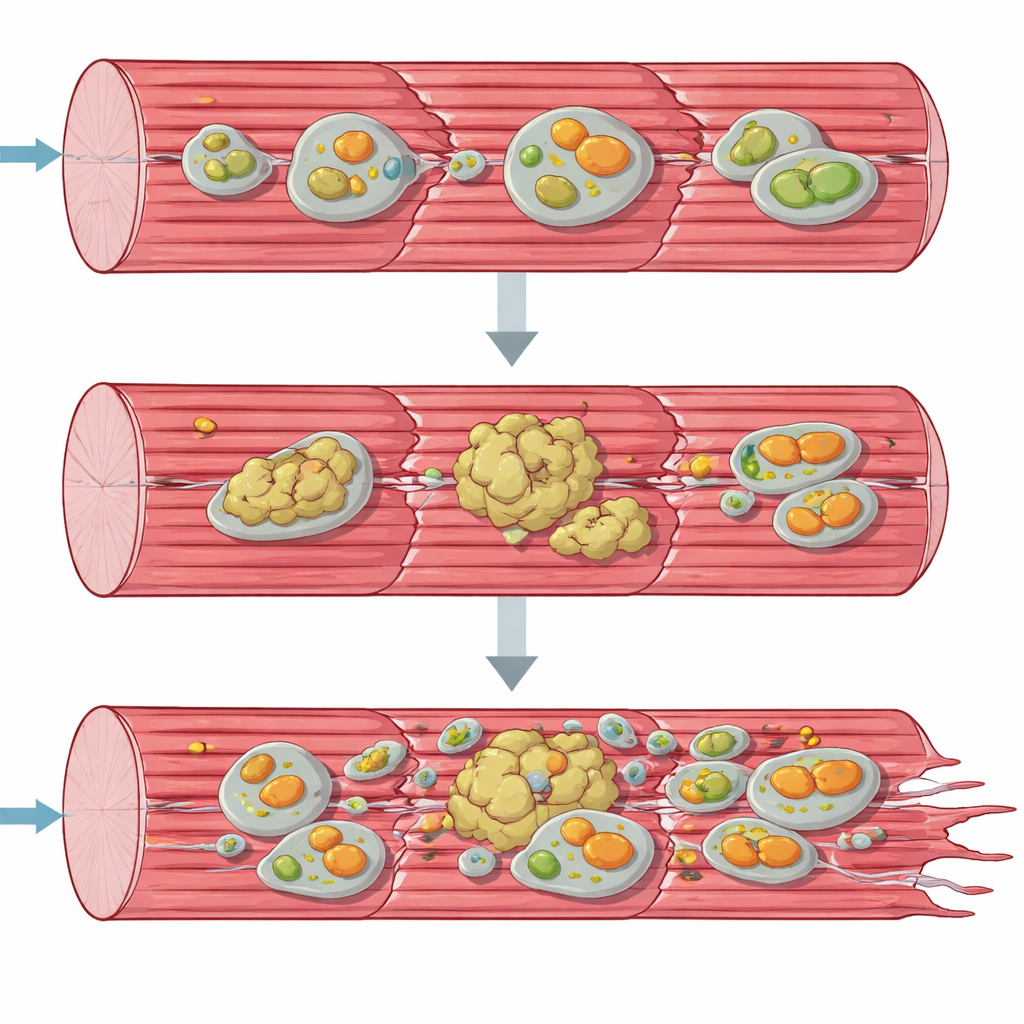
צבירות חלבונים ומיטוכונדריות חולות
כדי להבין את ההתמוטטות במבט מערכתתי, הצוות פנה לכלי “אומיקס” הסורקים אלפי מולקולות בבת אחת. פרופילי פעילות גנים וחלבונים הראו שתאי השריר נלחמו בניסיון להגיב: גנים לבניית חלבונים חדשים ולמנגנוני תגובת מתח הוגברו, והרבה צ'פרונים ופקטורי בקרת איכות הצטברו. עם זאת, הרבה חלבוני מבנה מרכזיים של המכשור הכיווצי נדדו מצורתם המומסת הנורמלית והצטברו במפלס בלתי מומס ועשיר אגגרגטים. במקביל, מרכיבים של מסלולי המחזור התאי — אוטופאגיה והסרת מיטוכונדריות פגומות ספציפית, מיטופאגיה — הצטברו כאילו תקועים באמצע התהליך. מיקרוסקופ אלקטרונים ובדיקות תפקוד מיטוכונדריאלי אישרו שאברוני ייצור האנרגיה היו מעוותים, מקובצים, ועבדו הרבה מתחת לקיבולת נורמלית, במיוחד בשלב הראשון של שרשרת הנשימה.
האוטופאגיה כעבריין המרכזי
המחברים אז בדקו האם הבעיה הראשונית נמצאת במחזור התאי הכללי (אוטופאגיה), במחזור המיועד למיטוכונדריה (מיטופאגיה), או בשניהם. הם גידלו תאי שריר מהעכברים המוטנטיים וחיזקו ניסיונית מסלולים שונים. גירוי אוטופאגיה רחבה בעזרת החלבון BECN1 ניקז סמני מתח מרכזיים, הקטין את אגגרגטי BAG3 המוטנטי, ושיפר את מראה והארגון של הסרקומרים. לעומת זאת, כפיית מיטופאגיה או הגברה פשוטה של ייצור מיטוכונדריה לא תיקנה את הפגמים. בעכברים חיים, טיפול בתרופה המפעילה אוטופאגיה, ראפאמיצין, שיפר אחיזת כוח, קואורדינציה ותנועה, והגביר סמנים של מחזור פעיל בשריר. יחד, ניסויים אלו מצביעים על חסימה ראשונית באוטופאגיה, כאשר נזק מיטוכונדריאלי צומח כתוצאה משנית ולא כגורם השורש.
בדיקת אסטרטגיית תרפיית גנים
מכיוון שהמחלה מונעת על ידי חלבון רעיל, החוקרים חקרו האם הפחתת BAG3 המוטנטי יכולה להציל את השרירים. הם ארזו RNA בגזרה קצרה (shRNA) שתוכנן במיוחד לפגוע ב-BAG3 האנושי בתוך וירוס מהונדס והזריקו אותו למחזור הדם של עכברים צעירים מוטנטיים. שבועות לאחר מכן, השרירים הראו הרבה פחות BAG3 מוטנטי, פחות אגגרגטים חלבוניים, צלקת מופחתת והרבה פחות סיבים עם גרעינים מרכזיים. החשוב מכל, השרירים המטופלים ייצרו יותר כוח באופן דרמטי ושבו חלקית לגודל נורמלי. הוכחת הרעיון הזו מרמזת ששתקת הגן הגורם למחלה, או שילוב של גישה כזו עם תרופות שמגבירות אוטופאגיה, עשויה להיות אסטרטגיה עוצמתית עבור מטופלים, לאחר שיאופטמו טיפולים ספציפיים לאילל.
מה משמעות הדבר עבור מטופלים ומעבר לכך
במונחים נגישים, עבודה זו מראה שכאשר חלבון עזר מרכזי כמו BAG3 מתקפל לא נכון ומתעקש, מערכת פינוי הפסולת של התא נסתמת. רכיבים שבורים ומיטוכונדריות פגומות מצטברים, השלד הפנימי של השריר קורס, והחוזק דועך. על ידי שיחזור זהירות של המחלה בעכברים, המחקר מגלה ששיקום או עקיפת מערכת הניקוי הזו — בין אם על ידי הגברת אוטופאגיה או על ידי הפחתת BAG3 המוטנטי עצמו — יכול לשקם במידה ניכרת את בריאות השריר. למרות שעדיין נותר הרבה לעשות לפני שטיפולים אלו יגיעו למרפאות, הממצאים מספקים מפת דרכים מפורטת להתמודדות עם הפרעה שרירית נדירה אך קטלנית זו ומציעים תובנות רחבות יותר על איך טיפול ביתי תאי פגום עשוי לעמוד בבסיס מחלות ניווניות נוספות.
ציטוט: Filippi, K., Graf-Riesen, K., Kuppusamy, M. et al. Blockage of autophagy causes severe skeletal muscle disruption in a mouse model for myofibrillar myopathy 6. Nat Commun 17, 3436 (2026). https://doi.org/10.1038/s41467-026-71749-6
מילות מפתח: מיו-פיברילר מיאופתיה, מוטציה ב-BAG3, אוטופאגיה, ניוון שריר שלד, תרפיית גנים