Clear Sky Science · ru
Блокада аутофагии вызывает тяжёлое разрушение скелетной мышцы в модели мыши миофибриллярной миопатии 6
Когда механизм уборки клетки даёт сбой
Наши мышцы постоянно восстанавливаются, тихо утилизируя изношенные элементы, чтобы мы могли ходить, дышать и двигаться автоматически. В этой статье рассматривается, что происходит, когда система внутриклеточной уборки разрушена из‑за одной наследственной мутации. Результатом является разрушительное детское мышечное заболевание, ослабляющее конечности и дыхательную мускулатуру. Создав подробную мышиную модель, исследователи не только раскрывают, как разворачивается повреждение внутри мышечных клеток, но и проверяют пути его обращения, давая проблеск надежды для будущих терапий.
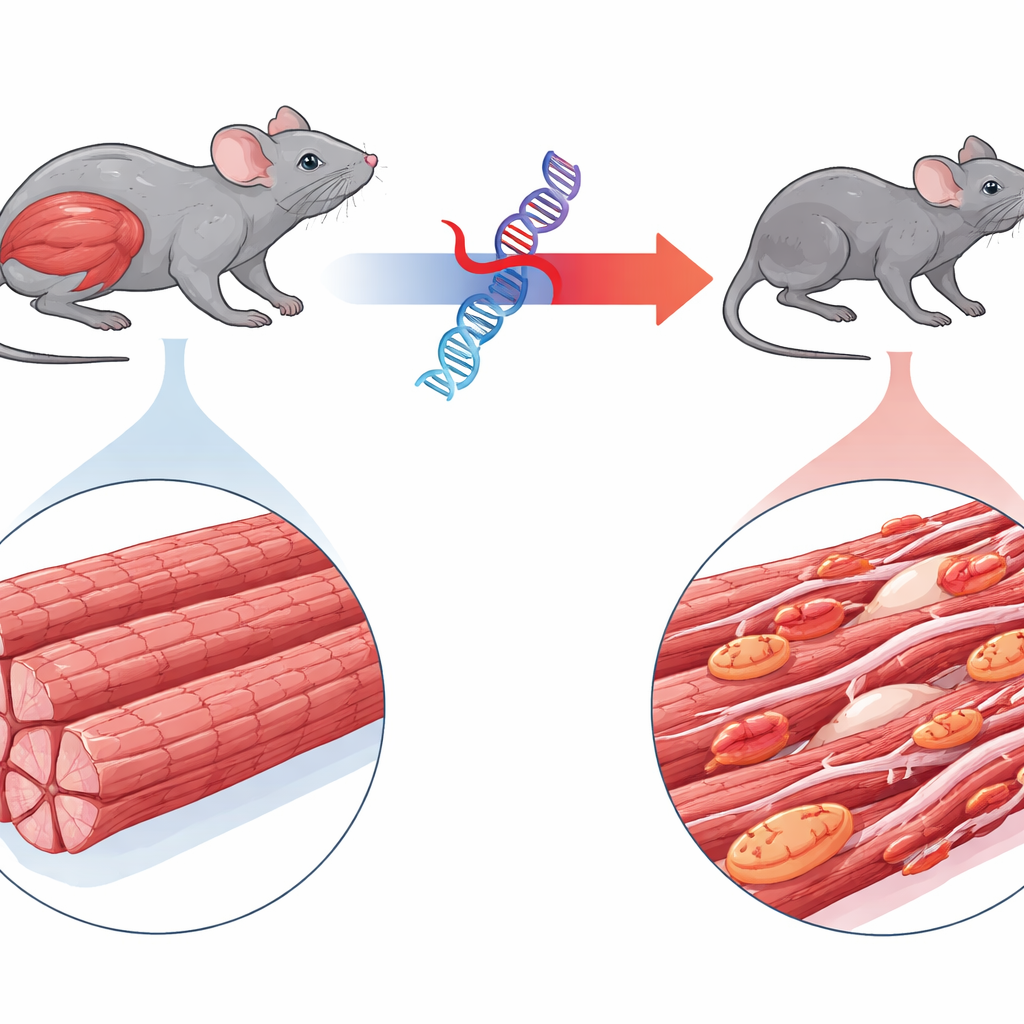
Редкое мышечное заболевание в центре внимания
Исследование сосредоточено на миофибриллярной миопатии 6 — редком заболевании, вызванном мутацией в гене BAG3. Дети с этим состоянием быстро развивают выраженную мышечную слабость, иногда наблюдаются проблемы с сердцем, и часто они умирают в юном возрасте от дыхательной недостаточности. BAG3 обычно контролирует качество крошечных сократительных единиц внутри мышечных волокон, направляя повреждённые белки на переработку. Авторы создали мышей, которые производят человеческую мутантную форму BAG3 с флуоресцентным маркером, что позволило отследить её поведение. В отличие от животных, экспрессирующих нормальный человеческий BAG3, мыши с мутантной версией быстро уменьшались в размере, демонстрировали истощение конечностей и дыхательной мускулатуры и покачивающуюся походку, что тесно повторяет клиническую картину у людей.
Как распадаются мышечные волокна
Микроскопическое и ультраструктурное исследование показало, насколько глубоко мутантный белок разрушает структуру мышцы. У поражённых мышей мышечные волокна были тоньше и пронизаны аномальными белковыми сгустками. Высокоупорядоченные полосы сократительного аппарата — саркомеры — были фрагментированы и размыты, и многие волокна имели центрально расположенные ядра, что характерно для попыток регенерации. Ткань инфильтрировалась иммунными клетками, увеличивалось количество фиброзного рубцового материала, хоть и менее выраженно, чем в сердце. Функционально изолированные мышцы этих животных вырабатывали до 90 процентов меньше силы по сравнению со здоровыми, даже с учётом их меньшего размера, что подтверждает, что ключевой сократительный механизм не справляется со своей задачей.
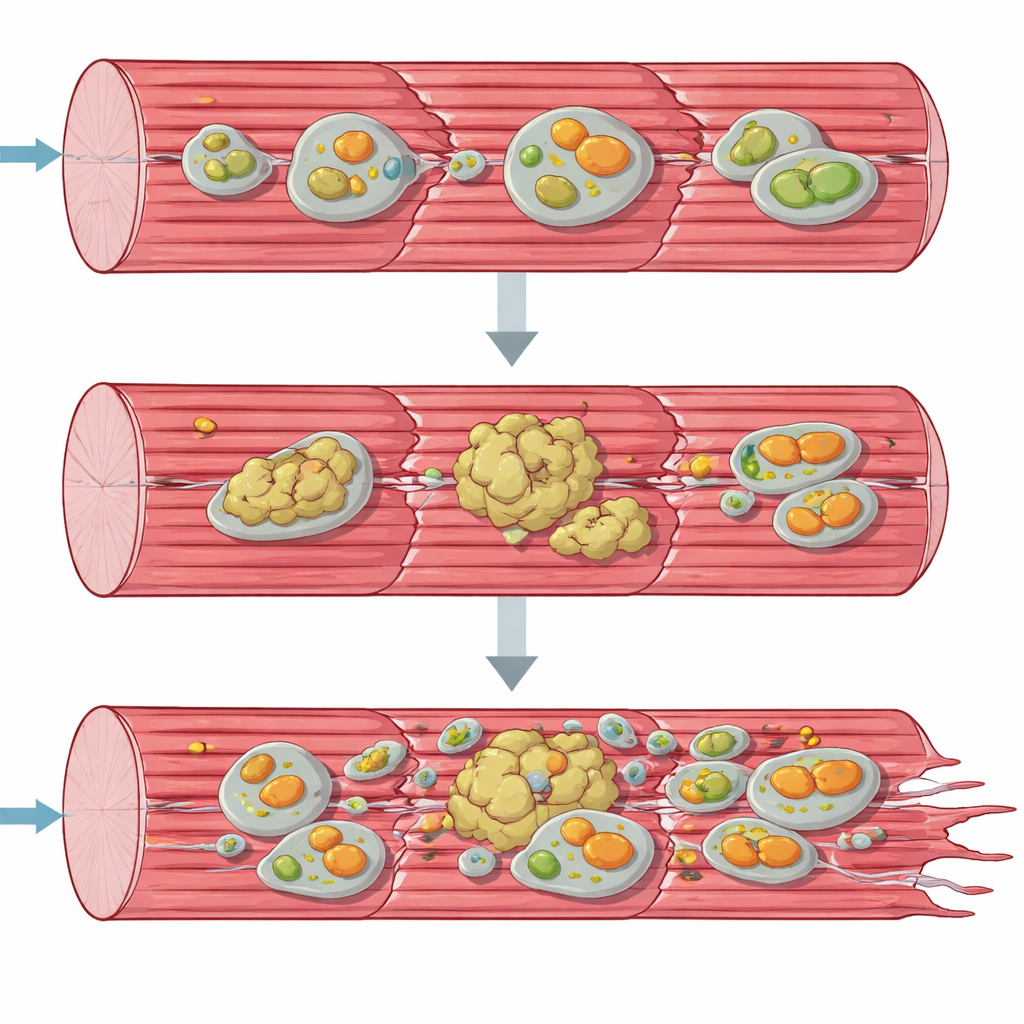
Накопление белков и больные митохондрии
Чтобы понять разрушение на системном уровне, команда применила «омикс»‑подходы, анализирующие тысячи молекул одновременно. Активность генов и профили белков показали, что мышечные клетки яростно пытаются отреагировать: включились гены синтеза белка и ответов на стресс, накопилось много шаперонов и других факторов контроля качества. Тем не менее многие ключевые структурные белки сократительного аппарата исчезли из нормальной растворимой фракции и вместо этого перешли в нерастворимую, богатую агрегатами фракцию. Одновременно компоненты путей утилизации клетки — аутофагии и специализированной утилизации повреждённых митохондрий, митофагии — накапливались, как будто застряли посередине процесса. Электронная микроскопия и тесты функции митохондрий подтвердили, что энергетические органеллы деформированы, сгруппированы и работают значительно хуже нормы, особенно на первом звене дыхательной цепи.
Аутофагия как ключевой виновник
Авторы затем поставили вопрос, состоит ли первичная проблема в общем клеточном утилизационном процессе (аутофагии), в митохондриальной утилизации (митофагии) или в обоих. Они выращивали мышечные клетки от мутантных мышей и экспериментально активировали разные пути. Стимуляция общей аутофагии с помощью белка BECN1 очищала ключевые маркеры стресса, уменьшала агрегаты мутантного BAG3 и улучшала внешний вид и организацию саркомеров. Напротив, принуждение митофагии или простое увеличение биогенеза митохондрий не устраняло дефекты. У живых мышей лечение рапамицином, активирующим аутофагию, улучшило силу захвата, координацию и подвижность, а также увеличило маркеры активной утилизации в мышцах. В совокупности эти эксперименты указывают на первичную блокаду аутофагии, а митохондриальные повреждения возникают как вторичная причина, а не как корень проблемы.
Испытание стратегии генотерапии
Поскольку заболевание вызвано токсичным белком, исследователи изучили, можно ли ослабить экспрессию мутантного BAG3 и тем самым восстановить мышцы. Они упаковали короткую шпильковую РНК, спроектированную для избирательной нацеленности на человеческий BAG3, в инженерный вирус и ввели его в кровоток молодых мутантных мышей. Через несколько недель в мышцах обнаруживалось значительно меньше мутантного BAG3, меньше белковых агрегатов, уменьшился фиброз и значительно сократилось число волокон с центральными ядрами. Что самое важное — обработанные мышцы генерировали значительно большую силу и частично вернули нормальные размеры. Этот доказательный эксперимент показывает, что заглушение болезнетворного аллеля, либо сочетание такого подхода с препаратами, усиливающими аутофагию, может стать мощной стратегией для пациентов после оптимизации аллелеспецифической терапии.
Что это значит для пациентов и в целом
Доступным языком эта работа демонстрирует: когда ключевой помогательный белок, такой как BAG3, неправильно сворачивается и образует комки, система утилизации клетки заклинивает. Сломанные компоненты и дефектные митохондрии накапливаются, внутренняя опора мышцы рушится, и сила убывает. Тщательно воссоздав заболевание в мышах, исследование показывает, что восстановление или обход этой системы уборки — либо путём усиления аутофагии, либо снижением уровня мутантного BAG3 — может существенно восстановить здоровье мышц. Хотя до их клинического применения ещё далеко, эти результаты дают подробную дорожную карту для борьбы с этим редким, но смертельным мышечным заболеванием и предлагают более широкие выводы о том, как нарушенное клеточное хозяйство может лежать в основе других дегенеративных болезней.
Цитирование: Filippi, K., Graf-Riesen, K., Kuppusamy, M. et al. Blockage of autophagy causes severe skeletal muscle disruption in a mouse model for myofibrillar myopathy 6. Nat Commun 17, 3436 (2026). https://doi.org/10.1038/s41467-026-71749-6
Ключевые слова: миофибриллярная миопатия, мутация BAG3, аутофагия, дегенерация скелетных мышц, генотерапия