Clear Sky Science · es
Bloqueo de la autofagia provoca una grave alteración del músculo esquelético en un modelo murino de miopatía miofibrilar 6
Cuando falla el equipo de limpieza de la célula
Nuestros músculos se reparan continuamente, eliminando en silencio las piezas desgastadas para que podamos caminar, respirar y movernos sin pensar. Este artículo explora qué ocurre cuando ese sistema celular de limpieza se colapsa debido a una única mutación heredada. El resultado es una devastadora enfermedad muscular infantil que debilita las extremidades y los músculos respiratorios. Al construir un modelo murino detallado, los investigadores no solo descubren cómo se despliega el daño dentro de las células musculares, sino que también prueban vías para revertirlo, ofreciendo un rayo de esperanza para futuras terapias.
Una enfermedad muscular rara en el punto de mira
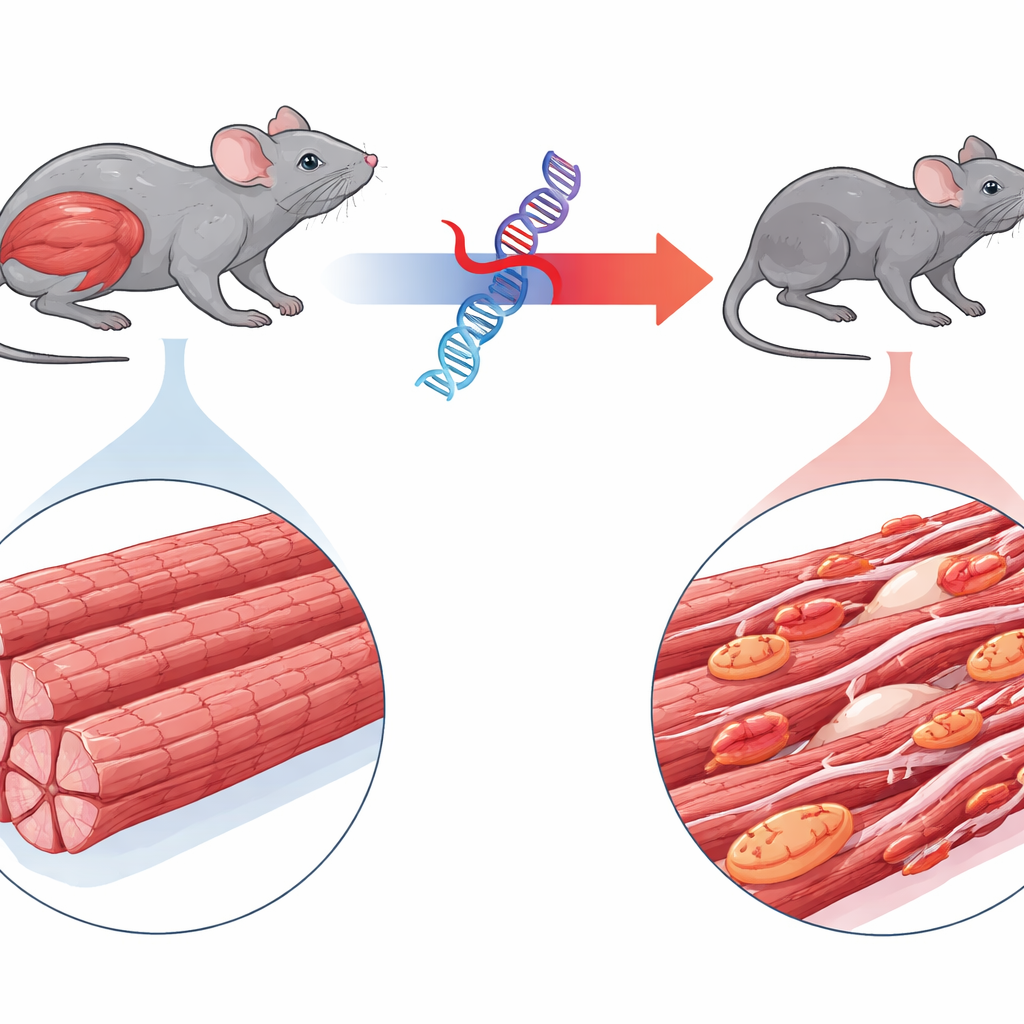
El estudio se centra en la miopatía miofibrilar 6, un trastorno raro causado por una mutación en un gen llamado BAG3. Los niños con esta condición desarrollan rápidamente una debilidad muscular profunda, en ocasiones problemas cardíacos, y con frecuencia mueren jóvenes por insuficiencia respiratoria. BAG3 normalmente supervisa la calidad de las diminutas unidades contráctiles dentro de las fibras musculares, dirigiendo las proteínas dañadas al reciclaje celular. Los autores modificaron genéticamente ratones para que produjeran la forma humana mutante de BAG3 marcada con un marcador fluorescente, lo que les permitió seguir su comportamiento. A diferencia de los ratones que expresan BAG3 humano normal, los animales con la versión mutante se encogieron rápidamente, mostraron desgaste de los músculos de las extremidades y respiratorios, y presentaron un andar oscilante, reflejando estrechamente la enfermedad humana.
Cómo se desmoronan las fibras musculares
Exámenes microscópicos y ultrastructurales revelaron hasta qué punto la proteína mutante altera la estructura muscular. En los ratones afectados, las fibras musculares eran más delgadas y estaban sembradas de cúmulos proteicos anormales. Las franjas altamente ordenadas de la maquinaria contráctil —los sarcómeros— estaban fragmentadas y difusas, y muchas fibras mostraron núcleos centralizados, una señal de regeneración en intento. Células inmunitarias infiltraron el tejido y aumentó el material cicatricial fibroso, aunque de forma menos dramática que en el corazón. Funcionalmente, los músculos aislados de estos ratones generaron hasta un 90% menos fuerza que los de animales sanos, incluso teniendo en cuenta su menor tamaño, confirmando que la maquinaria central de la contracción estaba fallando.
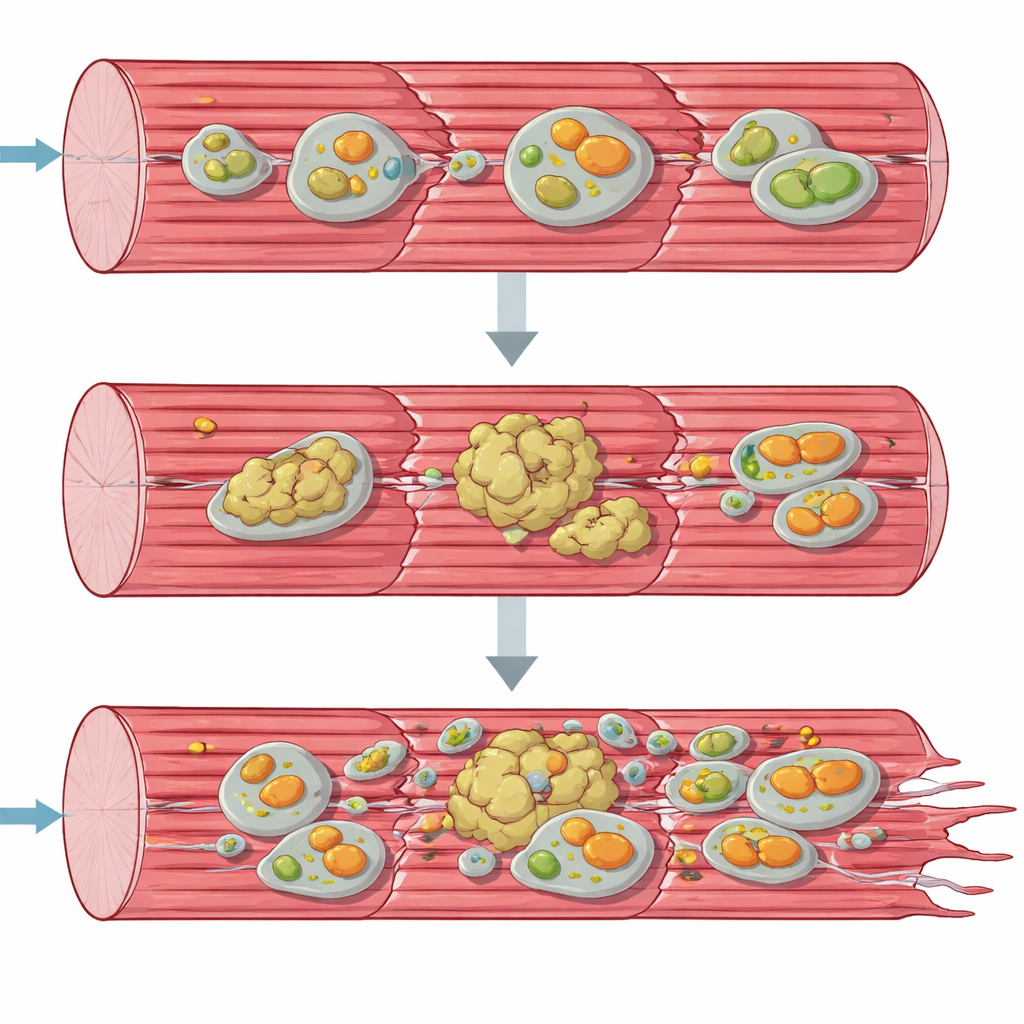
Acumulación de proteínas y mitocondrias enfermas
Para entender el colapso desde una perspectiva de sistemas, el equipo recurrió a herramientas “ómicas” que analizan miles de moléculas a la vez. La actividad génica y los perfiles proteicos mostraron que las células musculares trataban frenéticamente de responder: los genes para sintetizar nuevas proteínas y para respuestas al estrés estaban elevados, y muchas chaperonas y otros factores de control de calidad se acumulaban. Sin embargo, muchas proteínas estructurales clave del aparato contráctil se agotaron en sus formas solubles normales y en su lugar pasaron a una fracción insoluble rica en agregados. Al mismo tiempo, componentes de las vías de reciclaje celular —la autofagia y la eliminación especializada de mitocondrias dañadas, la mitofagia— se acumularon como si quedaran atascados a mitad del proceso. La microscopía electrónica y las pruebas de función mitocondrial confirmaron que los orgánulos productores de energía estaban deformados, agrupados y funcionaban muy por debajo de la capacidad normal, especialmente en el primer escalón de la cadena respiratoria.
La autofagia como culpable central
Los autores se preguntaron entonces si el problema primario residía en el reciclaje celular general (autofagia), en el reciclaje específico de mitocondrias (mitofagia), o en ambos. Cultivaron células musculares de los ratones mutantes y potenciaron experimentalmente distintas vías. Estimular la autofagia global con la proteína BECN1 eliminó marcadores clave de estrés, redujo los agregados de BAG3 mutante y mejoró la apariencia y organización de los sarcómeros. En contraste, forzar la mitofagia o simplemente aumentar la biogénesis mitocondrial no corrigió los defectos. En ratones vivos, el tratamiento con rapamicina, un fármaco activador de la autofagia, mejoró la fuerza de agarre, la coordinación y el movimiento, e incrementó marcadores de reciclaje activo en el músculo. En conjunto, estos experimentos apuntan a un bloqueo primario en la autofagia, con el daño mitocondrial emergiendo como consecuencia secundaria más que como causa raíz.
Probando una estrategia de terapia génica
Dado que la enfermedad está impulsada por una proteína tóxica, los investigadores exploraron si reducir el BAG3 mutante podría rescatar los músculos. Empaquetaron un ARN de horquilla corta diseñado para apuntar específicamente al BAG3 humano en un virus modificado y lo administraron por vía intravenosa a ratones jóvenes portadores de la mutación. Semanas después, los músculos mostraron mucho menos BAG3 mutante, menos agregados proteicos, reducción de la cicatrización y muchas menos fibras con núcleos centralizados. Lo más importante, los músculos tratados generaron mucha más fuerza y recuperaron parcialmente un tamaño más normal. Esta prueba de concepto sugiere que silenciar el gen causante de la enfermedad, o combinar dicho enfoque con fármacos que estimulen la autofagia, podría ser una estrategia potente para pacientes, una vez que se optimice una terapia específica por alelo.
Qué significa esto para los pacientes y más allá
En términos accesibles, este trabajo muestra que cuando una proteína auxiliar clave como BAG3 se pliega mal y forma cúmulos, el sistema de eliminación de desechos de la célula se atasca. Componentes rotos y mitocondrias defectuosas se acumulan, el andamiaje interno del músculo colapsa y la fuerza se diluye. Al recrear cuidadosamente la enfermedad en ratones, el estudio revela que restaurar o eludir este sistema de limpieza —ya sea potenciando la autofagia o reduciendo el BAG3 mutante— puede restaurar sustancialmente la salud muscular. Aunque queda mucho por hacer antes de que estos tratamientos lleguen a la clínica, los hallazgos proporcionan una hoja de ruta detallada para abordar este trastorno muscular raro pero letal y ofrecen ideas más amplias sobre cómo un mantenimiento celular deficiente puede subyacer a otras enfermedades degenerativas.
Cita: Filippi, K., Graf-Riesen, K., Kuppusamy, M. et al. Blockage of autophagy causes severe skeletal muscle disruption in a mouse model for myofibrillar myopathy 6. Nat Commun 17, 3436 (2026). https://doi.org/10.1038/s41467-026-71749-6
Palabras clave: miopatía miofibrilar, mutación en BAG3, autofagia, degeneración del músculo esquelético, terapia génica