Clear Sky Science · it
Il blocco dell’autofagia causa una grave distruzione del muscolo scheletrico in un modello murino della miofibrillare miopatia 6
Quando il servizio di pulizia della cellula fallisce
I nostri muscoli sono in costante riparazione, eliminando silenziosamente le parti usurate affinché possiamo camminare, respirare e muoverci senza pensarci. Questo articolo esplora cosa accade quando quel sistema cellulare di pulizia si guasta a causa di una singola mutazione ereditaria. Il risultato è una devastante malattia muscolare infantile che indebolisce gli arti e i muscoli respiratori. Ricostruendo un modello murino dettagliato, i ricercatori non solo rivelano come il danno si sviluppa all’interno delle cellule muscolari, ma mettono anche alla prova strategie per invertirlo, offrendo un barlume di speranza per terapie future.
Una malattia muscolare rara al centro dell’attenzione
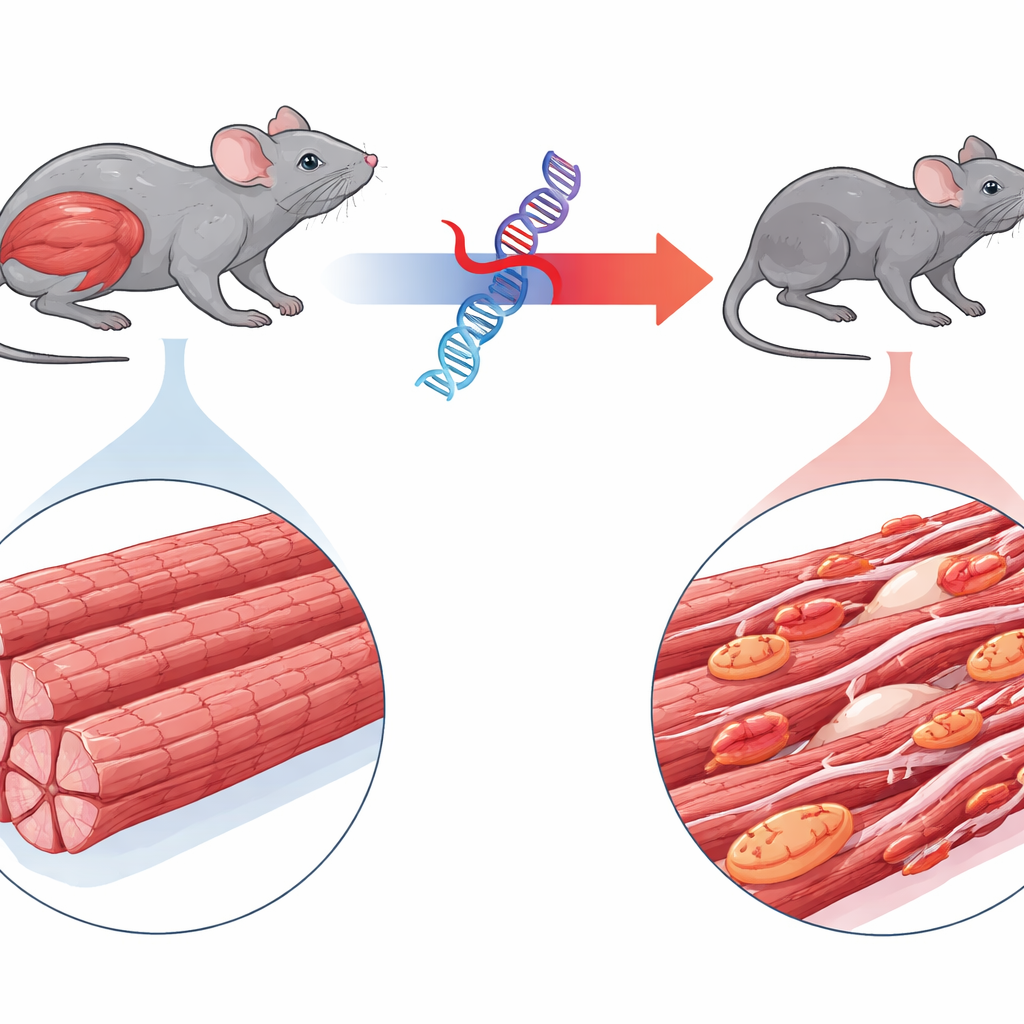
Lo studio si concentra sulla miofibrillare miopatia 6, un disturbo raro causato da una mutazione in un gene chiamato BAG3. I bambini affetti da questa condizione sviluppano rapidamente una profonda debolezza muscolare, talvolta problemi cardiaci, e spesso muoiono in giovane età per insufficienza respiratoria. BAG3 normalmente aiuta a supervisionare la qualità delle piccole unità contrattili all’interno delle fibre muscolari, indirizzando le proteine danneggiate al riciclo cellulare. Gli autori hanno ingegnerizzato topi che producono la forma mutante umana di BAG3 marcata con un indicatore fluorescente, permettendo loro di tracciarne il comportamento. Diversamente dai topi che esprimono BAG3 umano normale, gli animali con la versione mutante sono rapidamente diventati più piccoli, hanno mostrato atrofia dei muscoli degli arti e respiratori e una andatura ondeggiante, rispecchiando da vicino la malattia umana.
Come le fibre muscolari si disfano
Esami microscopici e ultrastrutturali hanno rivelato quanto profondamente la proteina mutante sconvolga la struttura muscolare. Nei topi colpiti, le fibre muscolari erano più sottili e costellate di ammassi proteici anomali. Le bande altamente ordinate della macchina contrattile — i sarcomeri — erano frammentate e sfumate, e molte fibre mostravano nuclei centralizzati, un segno di tentata rigenerazione. Cellule immunitarie hanno infiltrato il tessuto e il materiale cicatriziale fibroso è aumentato, sebbene in misura minore rispetto al cuore. A livello funzionale, i muscoli isolati da questi topi producevano fino al 90 percento in meno di forza rispetto a quelli di animali sani, anche tenendo conto delle loro dimensioni ridotte, confermando che il meccanismo centrale della contrazione stava cedendo.
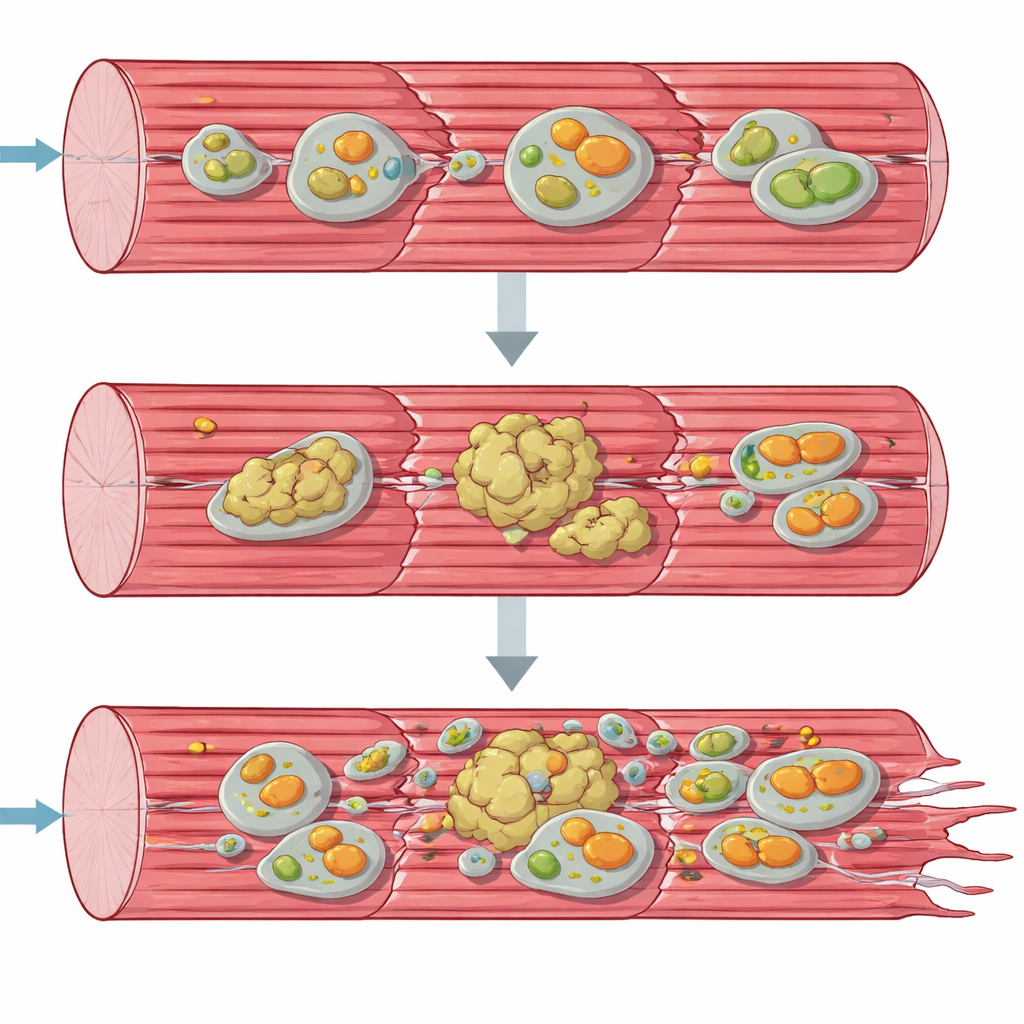
Accumuli proteici e mitocondri malati
Per comprendere il collasso da una prospettiva di sistema, il team ha impiegato strumenti “omici” che sondano migliaia di molecole contemporaneamente. L’attività genica e i profili proteici hanno mostrato che le cellule muscolari stavano cercando freneticamente di rispondere: i geni per la sintesi di nuove proteine e per le risposte allo stress erano attivati, e molti chaperoni e altri fattori di controllo qualità si accumulavano. Tuttavia, molte proteine strutturali chiave dell’apparato contrattili erano impoverite nella loro forma solubile normale e si erano invece spostate in una frazione insolubile ricca di aggregati. Allo stesso tempo, componenti delle vie di riciclo cellulare — l’autofagia e la rimozione specializzata dei mitocondri danneggiati, la mitofagia — si accumulavano come se fossero bloccati a metà processo. La microscopia elettronica e i test di funzionalità mitocondriale hanno confermato che gli organelli produttori di energia erano deformi, raggruppati e funzionavano ben al di sotto della capacità normale, specialmente al primo passaggio della catena respiratoria.
L’autofagia come colpevole principale
Gli autori si sono quindi chiesti se il problema primario risiedesse nel riciclo cellulare generale (autofagia), nella rimozione mitocondriale specifica (mitofagia), o in entrambi. Hanno coltivato cellule muscolari dai topi mutanti e stimolato sperimentalmente diverse vie. Attivare l’autofagia generale con la proteina BECN1 ha eliminato marcatori chiave di stress, ridotto gli aggregati di BAG3 mutante e migliorato l’aspetto e l’organizzazione dei sarcomeri. Al contrario, forzare la mitofagia o semplicemente aumentare la produzione mitocondriale non ha corretto i difetti. In topi vivi, il trattamento con il farmaco che attiva l’autofagia rapamicina ha migliorato la forza di presa, la coordinazione e il movimento, e ha aumentato i marker di riciclo attivo nel muscolo. Nel complesso, questi esperimenti indicano un blocco primario nell’autofagia, con il danno mitocondriale che emerge come conseguenza secondaria piuttosto che come causa principale.
Testare una strategia di terapia genica
Poiché la malattia è guidata da una proteina tossica, i ricercatori hanno esplorato se ridurre l’espressione del BAG3 mutante potesse salvare i muscoli. Hanno confezionato un short hairpin RNA progettato per colpire specificamente il BAG3 umano in un virus ingegnerizzato e lo hanno somministrato nel flusso sanguigno di giovani topi mutanti. Alcune settimane dopo, i muscoli mostravano molto meno BAG3 mutante, meno aggregati proteici, una riduzione della fibrosi e molte meno fibre con nuclei centralizzati. Soprattutto, i muscoli trattati generavano molta più forza e recuperavano parzialmente la dimensione normale. Questa prova di principio suggerisce che silenziare il gene responsabile della malattia, o combinare tale approccio con farmaci che potenziano l’autofagia, potrebbe essere una strategia efficace per i pazienti, una volta ottimizzata una terapia specifica per l’allele.
Cosa significa per i pazienti e oltre
In termini accessibili, questo lavoro mostra che quando una proteina ausiliaria chiave come BAG3 si ripiega male e si aggrega, il sistema di smaltimento della cellula si inceppa. Componenti danneggiati e mitocondri difettosi si accumulano, l’impalcatura interna del muscolo collassa e la forza viene meno. Ricreando attentamente la malattia nei topi, lo studio rivela che ripristinare o bypassare questo sistema di pulizia — sia potenziando l’autofagia sia riducendo il BAG3 mutante stesso — può ripristinare in misura significativa la salute muscolare. Sebbene rimanga molto da fare prima che tali trattamenti raggiungano la clinica, i risultati forniscono una road map dettagliata per affrontare questo raro ma mortale disturbo muscolare e offrono intuizioni più ampie su come la compromissione della manutenzione cellulare possa essere alla base di altre malattie degenerative.
Citazione: Filippi, K., Graf-Riesen, K., Kuppusamy, M. et al. Blockage of autophagy causes severe skeletal muscle disruption in a mouse model for myofibrillar myopathy 6. Nat Commun 17, 3436 (2026). https://doi.org/10.1038/s41467-026-71749-6
Parole chiave: miofibrillare miopatia, mutazione BAG3, autofagia, degenerazione del muscolo scheletrico, terapia genica