Clear Sky Science · ja
オートファジーの閉塞はミオフィブリラ筋症6のマウスモデルで重度の骨格筋破壊を引き起こす
細胞の清掃チームが機能しなくなったとき
私たちの筋肉は常に自己修復を行い、歩く・呼吸する・何気なく動くために古くなった部品を静かに除去しています。本稿は、単一の遺伝的変異によってその細胞内の清掃システムが破綻したときに何が起きるかを探ります。その結果、手足や呼吸筋を弱らせる致命的な小児期の筋疾患が生じます。詳細なマウスモデルを構築することにより、研究者たちは筋細胞内で損傷がどのように進行するかを解き明かすだけでなく、それを逆転させる手段も試験し、将来の治療への一縷の希望を示しています。
注目すべき稀な筋疾患
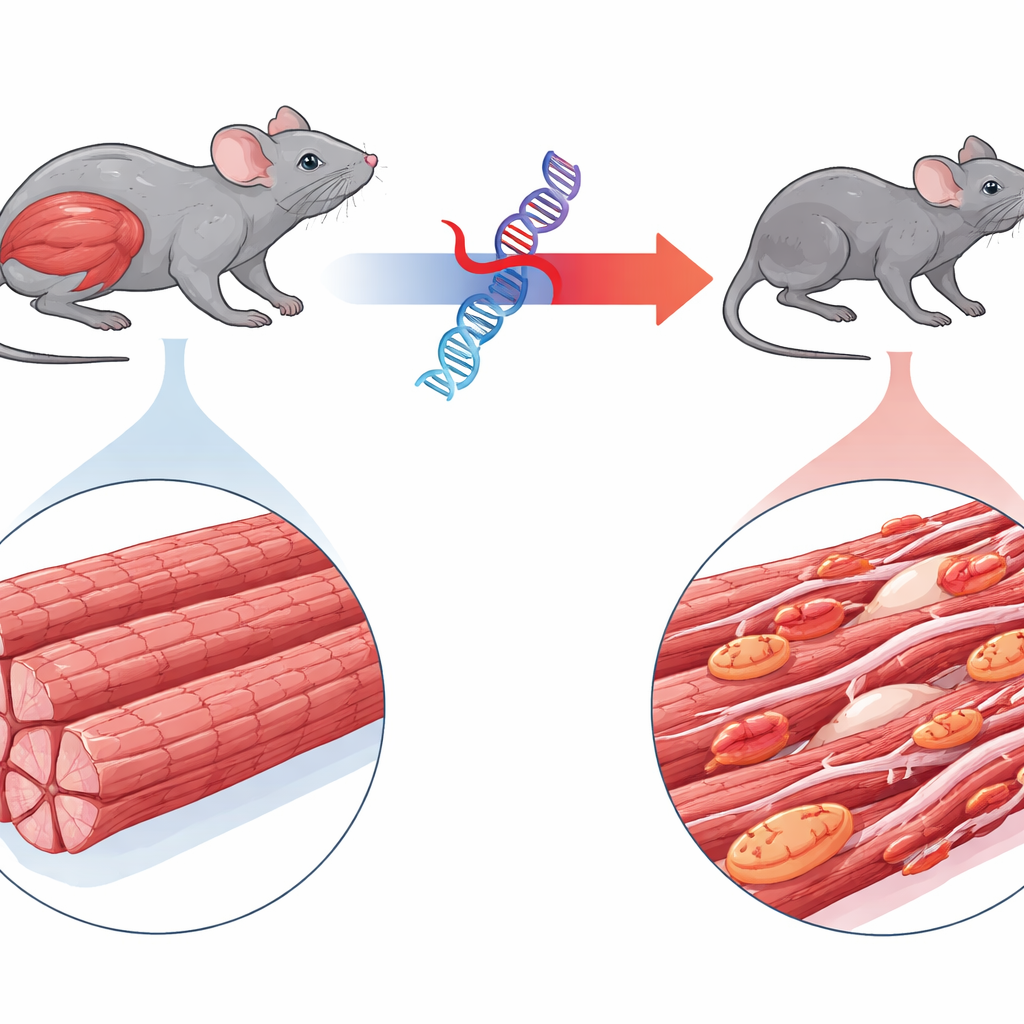
本研究は、BAG3という遺伝子の変異によって生じる稀な疾患、ミオフィブリラ筋症6に焦点を当てています。この病気の子どもたちは急速に重度の筋力低下をきたし、心臓合併症を伴うことがあり、しばしば呼吸不全で若くして亡くなります。BAG3は通常、筋線維内の微小な収縮単位の品質管理を監督し、損傷したタンパク質を細胞内のリサイクルへ導きます。著者らは、ヒトの変異型BAG3に蛍光タグを付けた形で発現させるマウスを作製し、その挙動を追跡しました。正常なヒトBAG3を発現するマウスとは異なり、変異型を有する動物は急速に小型化し、四肢や呼吸筋の萎縮を示し、よちよち歩きの歩様を呈してヒトの病態をよく反映しました。
筋線維が崩壊するしくみ
顕微鏡および超微細構造の解析により、変異タンパク質が筋構造を徹底的に乱す様子が明らかになりました。影響を受けたマウスでは筋線維は細くなり、異常なタンパク質塊が多発していました。収縮機構であるサルコメアの高度に規則的な縞模様は断片化して不明瞭になり、多くの線維で核が中央に偏位しており、再生の試みを示す指標でした。免疫細胞が組織に浸潤し、線維性の瘢痕物質も増加しましたが、心臓ほど顕著ではありませんでした。機能面では、これらのマウスから単離した筋は、サイズ差を考慮しても健康な個体の筋に比べ最大90%近く力を発揮できず、収縮の根幹となる装置が破綻していることが確認されました。
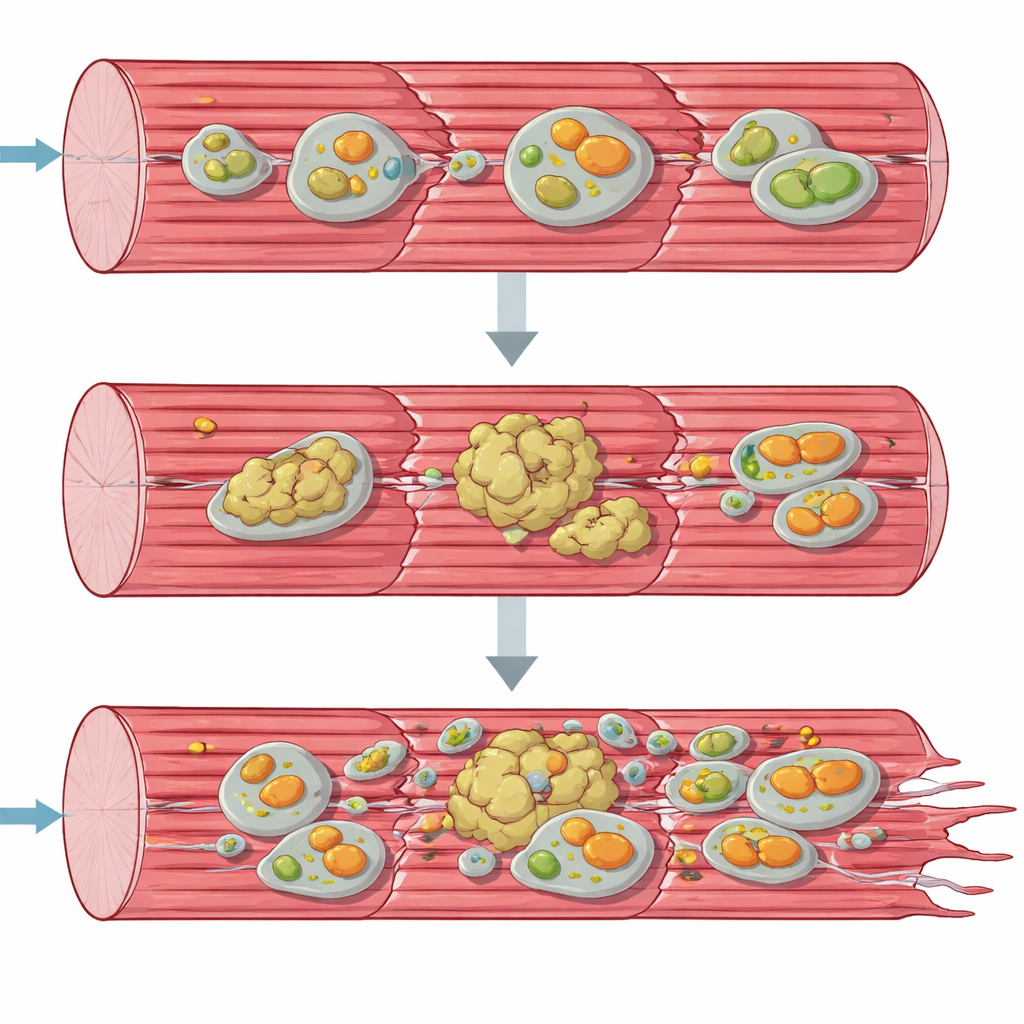
タンパク質の堆積と障害を受けたミトコンドリア
システム全体の観点から崩壊を理解するために、チームは数千の分子を同時に調べる“オミクス”手法を用いました。遺伝子発現とタンパク質プロファイルは、筋細胞が必死に応答しようとしていることを示しました:新しいタンパク質合成やストレス応答に関わる遺伝子群が活性化し、多くのシャペロンや品質管理因子が蓄積していました。それでも、収縮装置の主要な構造タンパク質の多くは通常の可溶形態から欠乏し、不溶性で凝集の多い分画へと移行していました。同時に、細胞のリサイクル経路であるオートファジーや損傷ミトコンドリアの選択的除去であるミトファジーの構成要素が途中で詰まったかのように蓄積していました。電子顕微鏡とミトコンドリア機能検査は、エネルギー産生小器官が形態異常を起こし、集合し、特に呼吸鎖の最初の段階で著しく低下した機能しか持たないことを確認しました。
中心的な犯人はオートファジー
著者らは、主要な問題が一般的な細胞内リサイクル(オートファジー)にあるのか、ミトコンドリア特異的なリサイクル(ミトファジー)にあるのか、あるいはその両方にあるのかを問い直しました。変異マウス由来の筋細胞を培養し、さまざまな経路を実験的に活性化しました。BECN1タンパク質で広範なオートファジーを刺激すると、主要なストレスマーカーが除去され、変異BAG3の凝集体が減少し、サルコメアの外観と配列が改善しました。対照的に、ミトファジーを強制的に誘導するか単にミトコンドリア生産を増やしても欠陥は是正されませんでした。生体マウスでは、オートファジー活性化薬ラパマイシンの投与が握力、協調運動、移動を改善し、筋内の活性化されたリサイクルマーカーを増加させました。これらの実験は、一次的なブロックがオートファジーにあり、ミトコンドリア障害は根本原因というよりは二次的な結果として生じることを示唆しています。
遺伝子治療戦略の試験
この病気が毒性タンパク質によって駆動されるため、研究者たちは変異BAG3の発現を下げることで筋を救えるかどうかを検討しました。ヒトBAG3を特異的に標的とするショートヘアピンRNAを組み込んだ改変ウイルスを作製し、若い変異マウスの血流に投与しました。数週間後、筋では変異BAG3の量が大幅に減少し、タンパク質凝集体が減り、瘢痕化が抑えられ、中央核を持つ線維も著しく減少していました。最も重要なことに、治療された筋は著しく大きな力を発生し、部分的に正常な大きさを回復しました。この概念実証は、病因の遺伝子をサイレンシングすること、あるいはオートファジーを高める薬剤と併用することが、アレル特異的治療が最適化されれば患者にとって強力な戦略になり得ることを示唆しています。
患者とそれ以外への意味
平易に言えば、本研究はBAG3のような主要な補助タンパク質が誤って折り畳まれ凝集すると、細胞のゴミ処理システムが詰まることを示しています。壊れた構成要素や障害ミトコンドリアが蓄積し、筋の内部骨格が崩壊し、筋力が失われていきます。マウスで病態を慎重に再現することで、この研究はこの清掃システムを回復または迂回すること―オートファジーを強化するか変異BAG3自体を減らすことで―筋の健康を大幅に回復できることを示しました。こうした治療が臨床に到達するまでには多くの課題が残りますが、知見はこの稀で致命的な筋疾患に取り組むための詳細なロードマップを提供し、障害された細胞の“家事”が他の変性疾患の基盤になり得るというより広い示唆を与えます。
引用: Filippi, K., Graf-Riesen, K., Kuppusamy, M. et al. Blockage of autophagy causes severe skeletal muscle disruption in a mouse model for myofibrillar myopathy 6. Nat Commun 17, 3436 (2026). https://doi.org/10.1038/s41467-026-71749-6
キーワード: ミオフィブリラ筋症, BAG3変異, オートファジー, 骨格筋変性, 遺伝子治療