Clear Sky Science · zh
通过脑类器官中的深度学习筛选加速利氏综合征药物发现
为毁灭性儿童脑病寻找新的希望
利氏综合征是一种罕见且常致命的疾病,侵袭婴幼儿,剥夺其大脑生长和正常功能所需的能量。家庭目前没有经证实的治疗方法,只有支持性护理。本研究将前沿生物学与人工智能结合,寻找可能有助的现有药物。通过将计算机引导的预测与试管中生长的微型脑模型相结合,研究人员在利氏综合征模型中识别出两种能部分恢复脑样活动的药物,指向一种更快速发现罕见儿童疾病治疗方法的途径。
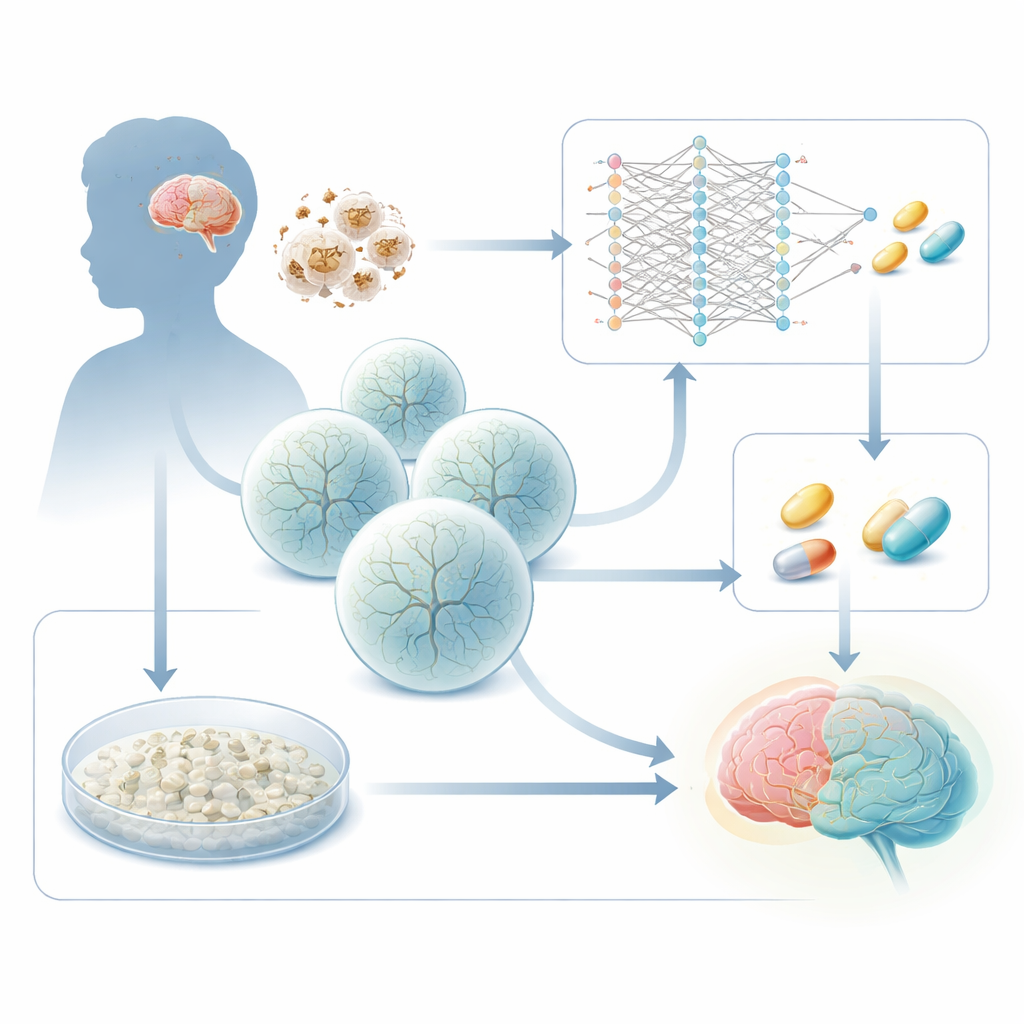
能量失衡如何损害发育中的大脑
利氏综合征由供能线粒体的基因遗传缺陷引起。一种常见的元凶是名为 SURF1 的基因,该基因参与细胞能量产生机制的关键步骤。当 SURF1 出现缺陷时,对能量需求高的脑区——尤其是中脑深部结构和基底节——开始衰竭。该团队早期的工作使用患者来源的干细胞培养出三维脑类器官,显示利氏类器官神经元形成不良,分支和连线异常。本研究提出一个务实问题:能否将这些疾病特异性的变化作为读出指标,以发现能将病变细胞推回正常发育轨迹的药物?
教会计算机提出有用的药物建议
项目的一条路线使用了为非癌细胞专门构建的深度学习框架。算法不是简单地将疾病基因表达签名与药物反应目录匹配,而是学习年轻脑细胞从类干的放射状胶质细胞,转变为中间祖细胞,再到成熟神经元时基因调控网络如何变化。利用来自利氏和健康大脑类器官的单细胞 RNA 测序数据,模型推断出应当调整哪些转录因子以将病变细胞沿正常发育路径推进。然后它在大型药物数据库中搜索,并预测哪些化合物应能“引导”该网络从利氏样状态走向更健康的神经元状态。从成千上万的候选药物中,它将名单缩小到数十种在细胞代谢上显示出有希望效应的药物。
让酵母和微型大脑为最佳候选者投票
同时,团队在酵母中进行一种非常不同的筛选。酿酒酵母有其对应的 SURF1 基因,删除该基因会使细胞在营养匮乏时变得脆弱——这是利氏综合征中能量应激的一个呼应。研究人员将缺失 SURF1 的酵母暴露于2250种已获批准的药物中,测量哪些化学物质最能拯救其存活。耐人寻味的是,人工智能筛选和酵母存活测试都指向同一化学家族:唑类,一组更为人所知的是抗真菌和皮肤科用药。从中,团队聚焦于两种化合物:talarozole(他拉唑或类)和 sertaconazole(赛他康唑),这些药物在人类细胞模型中长期暴露下似乎足够安全,并且在培养皿中的利氏来源神经元早期形成方面有显著改善。
在人体中脑类器官中测试这些药物
为更接近患者受影响的脑区,研究人员从患者来源的神经祖细胞产生中脑类器官。这些三维结构包含产多巴胺的神经元、支持细胞和发育中的回路。与健康细胞来源的类器官相比,利氏类器官体积更大但神经元结构更差,向培养基释放更多乳酸,并在遭受急性能量应激时表现异常。用低剂量 talarozole 或 sertaconazole 处理利氏中脑类器官数周,可减缓其过度生长,减少约五分之一的乳酸释放,并改善部分神经元功能指标。特别是 talarozole 增加了类似多巴胺神经元的数量,并在类器官面临突发能量匮乏时恢复更强的钙信号,表明网络反应性得到部分恢复。
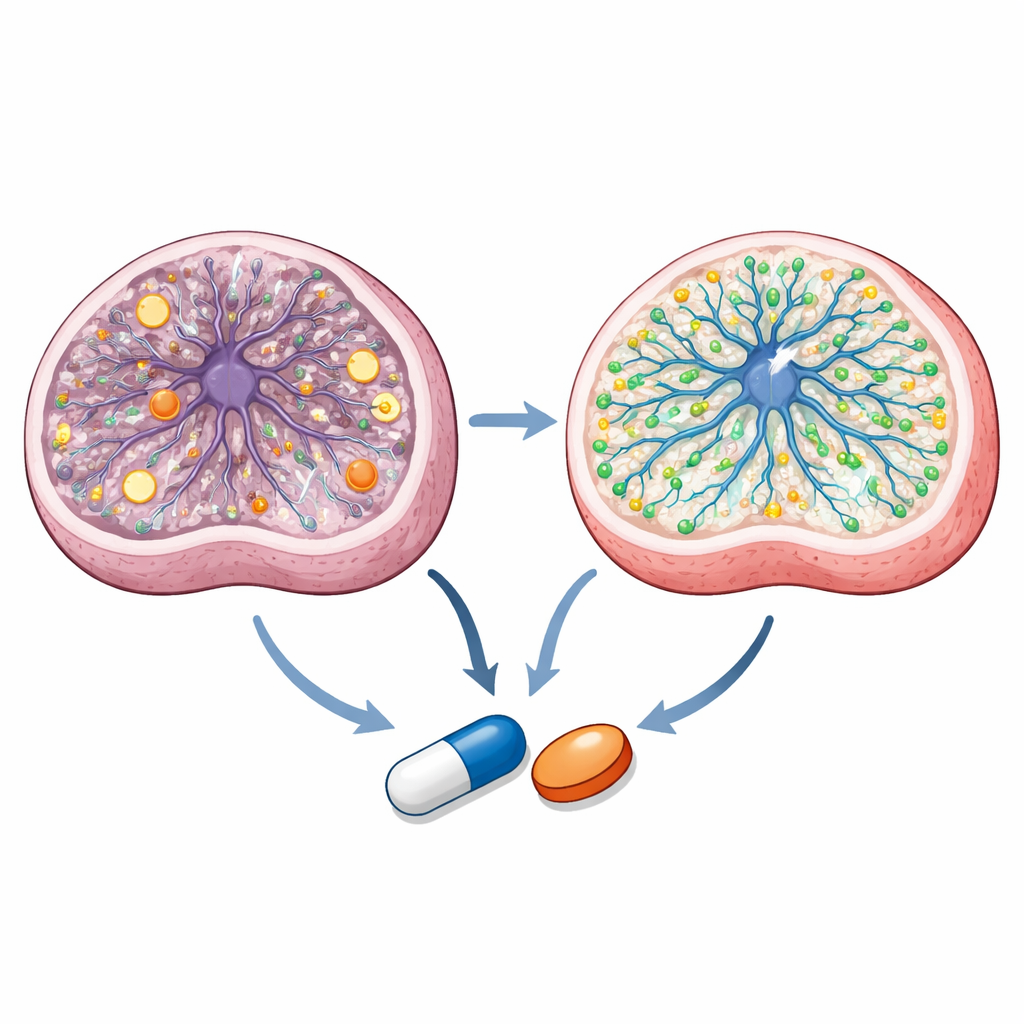
揭示这些化合物在细胞内的作用机制
深入研究发现,这两种唑类药物通过重叠但不同的途径发挥作用。详细的代谢物测定表明,利氏神经祖细胞存在能量状态失衡和线粒体化学改变。talarozole 使关键能量比率和细胞中心代谢循环的若干中间产物恢复正常,而两种药物都修正了特定的代谢瓶颈。脂质分析与成像显示,sertaconazole 对膜相关脂类和胆固醇有强烈影响,恢复了某些鞘脂并增加了在利氏细胞中减少的膜结合胆固醇。单细胞 RNA 测序的处理类器官表明,两种药物都促进与神经元生成和脂质代谢相关的基因程序,同时抑制过度活跃的线粒体基因表达。计算对接和活细胞报告试验进一步提示,talarozole 作用于分解视黄酸(一种对大脑发育至关重要的维生素 A 衍生物)的酶,并激活名为 PPARγ 的核受体,而该受体已被认为是在治疗线粒体疾病中的潜在干预点。
这对利氏综合征患儿可能意味着什么
尽管 talarozole 和 sertaconazole 并未在这些模型中完全逆转所有疾病特征,但它们在酵母、二维神经元和三维人类中脑类器官中一致缓解了利氏综合征的若干标志性病变。该工作表明,将深度学习与人类类器官和简单的酵母筛选相结合,能够快速锁定可重新定位用于一种当前缺乏治疗的罕见儿科疾病的药物。对家庭而言,这尚未转化为获批的治疗方案,但它提供了两种具体的药物候选者,更重要的是,提供了一种通用策略:使用先进计算筛选庞大的药物库,然后在逼真的人类微型大脑模型中测试最有希望的命中项。该方法可能缩短从基础生物学到对利氏综合征及其他源于线粒体功能障碍的神经发育疾病的有意义治疗选择之间的路程。
引用: Menacho, C., Okawa, S., Álvarez-Merz, I. et al. Accelerating Leigh syndrome drug discovery through deep learning screening in brain organoids. Nat Commun 17, 3570 (2026). https://doi.org/10.1038/s41467-026-71391-2
关键词: 利氏综合征, 脑类器官, 深度学习, 药物重新定位, 线粒体疾病