Clear Sky Science · ru
Ускорение поиска лекарств от синдрома Лея с помощью глубинного обучения в мозговых органоидах
Новая надежда при разрушительной детской болезни мозга
Синдром Лея — редкое, часто смертельное заболевание, поражающее младенцев и маленьких детей и лишающее их мозг энергии, необходимой для роста и функционирования. У семей сейчас нет проверенных методов лечения, есть лишь поддерживающая помощь. В этом исследовании объединены передовые методы биологии и искусственного интеллекта для поиска уже существующих лекарств, которые могли бы помочь. Сочетая компьютерные прогнозы с крошечными лабораторно выращенными моделями мозга, ученые выявляют два препарата, частично восстанавливающих мозго-подобную активность в моделях синдрома Лея, что указывает на более быстрый путь к открытию терапий для редких детских заболеваний.
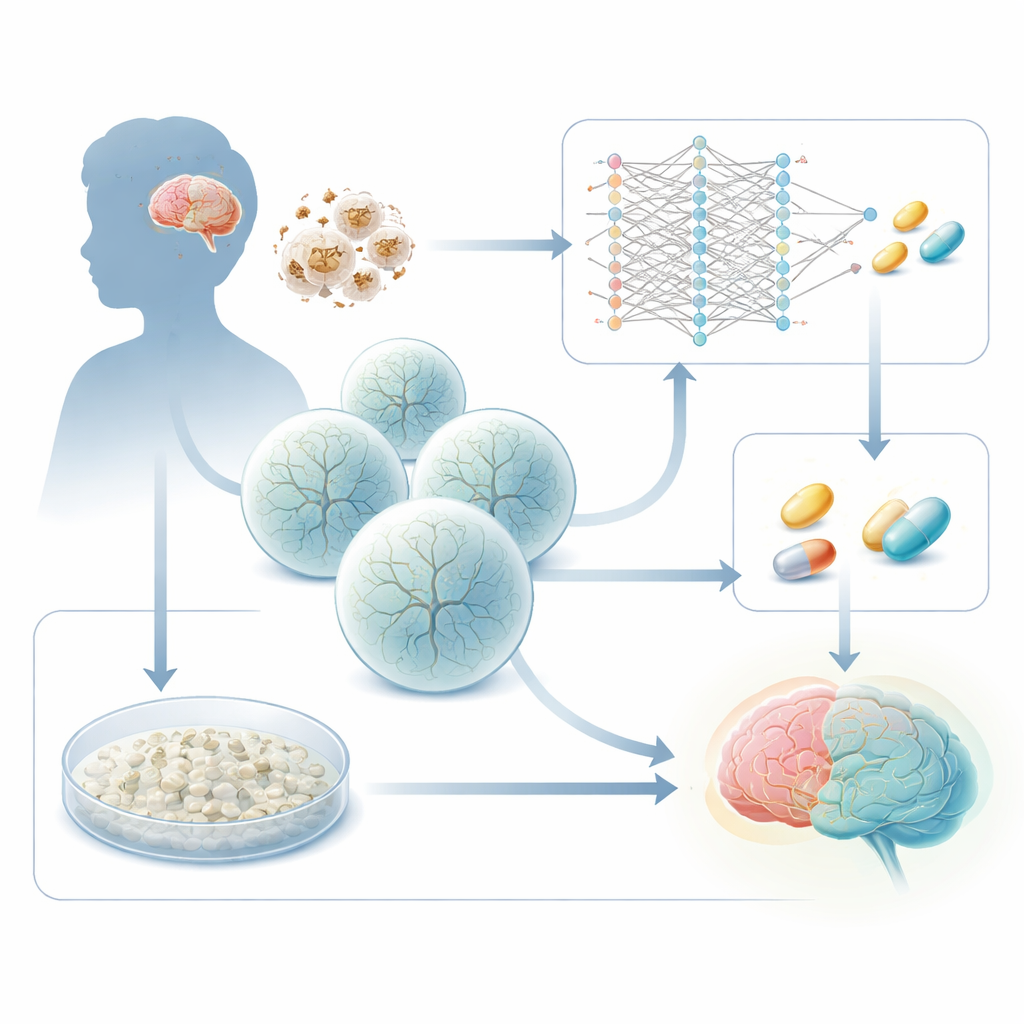
Как энергетический сбой вредит развивающемуся мозгу
Синдром Лея вызван наследственными дефектами в генах, отвечающих за работу митохондрий — «батареек» клетки. Одним из распространенных виновников является ген SURF1, необходимый для ключевого шага в энергетическом аппарате клетки. Когда SURF1 дефектен, области мозга с высоким энергопотреблением — особенно глубокие структуры среднего мозга и базальных ганглиев — начинают давать сбой. Ранние работы этой группы, использовавшие стволовые клетки пациентов для выращивания трехмерных органоидов мозга, показали, что органоиды с синдромом Лея плохо формируют нейроны, с аномальной ветвистостью и проводкой. Новое исследование задает практический вопрос: можно ли использовать эти характерные изменения как маркер, чтобы найти препараты, возвращающие больные клетки к нормальному развитию?
Обучение компьютеров предлагать полезные лекарства
Одна часть проекта использует фреймворк глубинного обучения, созданный специально для нераковых клеток. Вместо простого сопоставления сигнатур генов болезни с каталогом реакций на препараты, алгоритм изучает, как сети регуляции генов меняются по мере перехода молодых клеток мозга от стволоподобных радиальных глии к промежуточным прогениторам и затем к зрелым нейронам. Используя данные одноклеточного РНК‑seq из органоидов Лея и контролей, модель выводит, какие транскрипционные факторы следует скорректировать, чтобы сдвинуть больные клетки на нормальную траекторию развития. Затем она ищет в большой базе данных препаратов и предсказывает, какие соединения должны «направить» сеть из состояния, похожего на Лея, в более здоровое нейронное состояние. Из тысяч кандидатов список сокращается до нескольких десятков препаратов с многообещающим воздействием на клеточный метаболизм.
Дать голос дрожжам и мини‑мозгам: тестирование кандидатов
Параллельно команда проводит совершенно другой скрининг на дрожжах. Пекарские дрожжи имеют собственную версию гена SURF1, а его удаление делает клетки уязвимыми при дефиците питательных веществ — отголосок энергетического стресса при синдроме Лея. Исследователи экспонируют дрожжи с дефицитом SURF1 2 250 уже одобренными препаратами и измеряют, какие химические вещества лучше всего восстанавливают выживаемость. Любопытно, что и ИИ‑скрининг, и тест выживаемости дрожжей указывают на одно и то же семейство соединений: азолы — группу, более известную как противогрибковые и дерматологические препараты. Из них команда сосредоточивается на двух соединениях, таларозоле и сертаконазоле, которые кажутся достаточно безопасными для длительного воздействия в моделях человеческих клеток и существенно улучшают раннее формирование нейронов в нейронах, полученных от пациентов с Лей в культуре.
Проверка препаратов в человеческих органоидах среднего мозга
Чтобы приблизиться к пораженным у пациентов участкам мозга, исследователи получают органоиды среднего мозга из нейральных прогениторных клеток, выделенных у пациентов. Эти 3D‑структуры содержат дофаминергические нейроны, поддерживающие клетки и развивающиеся цепи. По сравнению с органоидами из здоровых клеток, органоиды Лея растут больше, но имеют худшую нейронную структуру, выделяют в среду больше молочной кислоты и аномально реагируют на острый энергетический стресс. Лечение органоидов среднего мозга Лея в течение нескольких недель низкими дозами таларозола или сертаконазола замедляет их чрезмерный рост, снижает выброс лактата примерно на одну пятую и улучшает некоторые показатели нейронной функции. В частности, таларозол увеличивает число дофаминоподобных нейронов и восстанавливает более выраженный кальциевый сигнал при резкой энергетической депривации, что указывает на частичное восстановление реактивности сети.
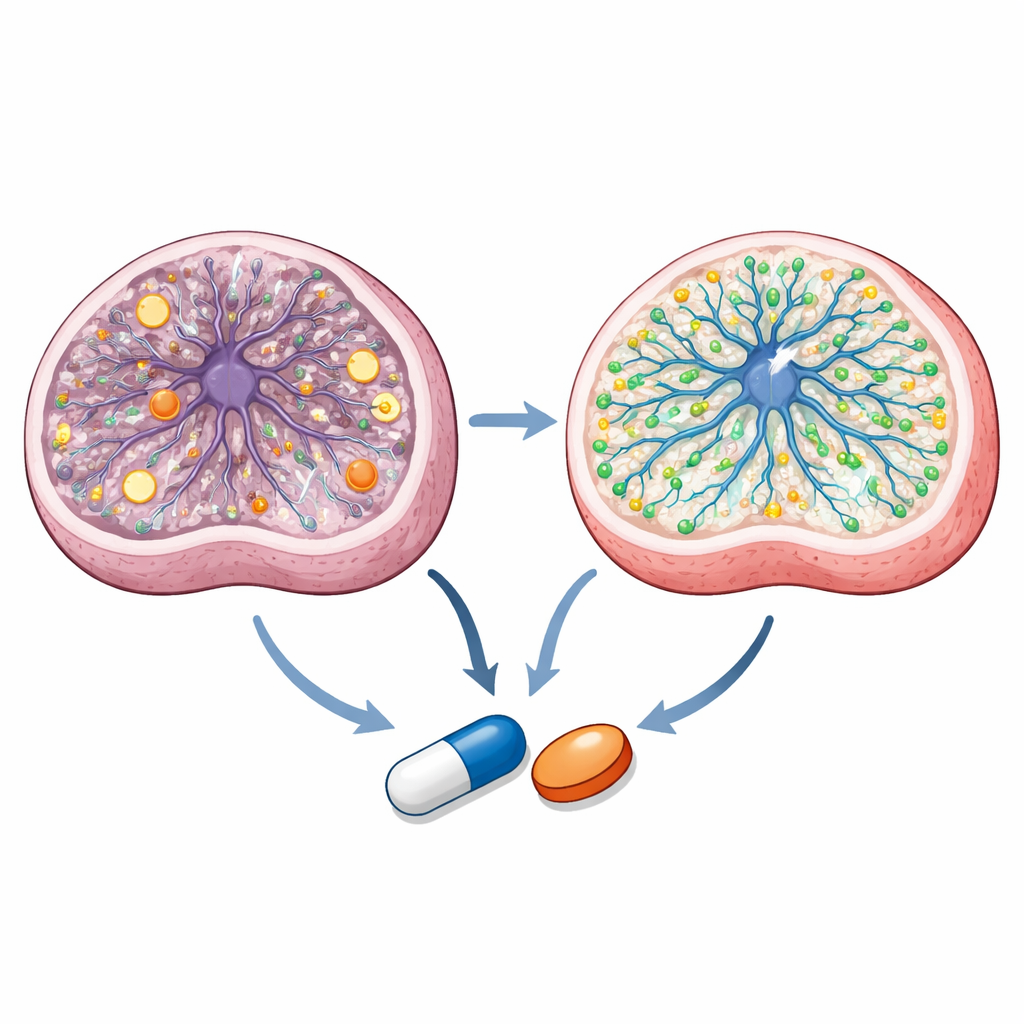
Как эти соединения работают внутри клеток
Углубленный анализ показывает, что оба азольных препарата действуют через пересекающиеся, но отличающиеся пути. Детальные измерения метаболитов показывают, что нейральные прогениторы Лея имеют нарушенный энергетический баланс и измененную митохондриальную химию. Таларозол нормализует ключевые энергетические соотношения и несколько промежуточных метаболитов в центральном метаболическом цикле клетки, в то время как оба препарата корректируют специфические метаболические узкие места. Липидный профиль и визуализация показывают, что сертаконазол сильно влияет на мембранно‑ассоциированные липиды и холестерин, восстанавливая определенные сфинголипиды и увеличивая содержание мембраноассоциированного холестерина, которое снижено при Лее. Одноклеточное РНК‑seq обработанных органоидов указывает, что оба препарата активируют генетические программы, связанные с генерацией нейронов и липидным обменом, при этом подавляя чрезмерно активную экспрессию митохондриальных генов. Молекулярное докирование и живые клеточные репортерные тесты дополнительно предполагают, что таларозол взаимодействует с ферментами, расщепляющими ретиноевую кислоту — производное витамина A, важное для развития мозга — и активирует ядерный рецептор PPARγ, рассматриваемый как потенциальная терапевтическая мишень при митохондриальных болезнях.
Что это может означать для детей с синдромом Лея
Хотя таларозол и сертаконазол не устраняют полностью все признаки болезни в этих моделях, они стабильно смягчают несколько ключевых проявлений синдрома Лея в дрожжах, 2D‑нейронах и 3D‑органоидах человеческого среднего мозга. Работа демонстрирует, что сочетание глубинного обучения с человеческими органоидами и простыми дрожжевыми скринингами может быстро выявлять препараты для репозиционирования при редком педиатрическом расстройстве, для которого сейчас нет лечения. Для семей это еще не означает одобренную терапию, но дает два конкретных кандидатных препарата и, возможно, что важнее, общую стратегию: использовать продвинутые вычисления для фильтрации огромных библиотек лекарств, а затем тестировать наиболее перспективные хиты в реалистичных моделях человеческих мини‑мозгов. Такой подход может сократить путь от фундаментальной биологии к значимым вариантам лечения синдрома Лея и других нейроразвитийных заболеваний, связанных с митохондриальной дисфункцией.
Цитирование: Menacho, C., Okawa, S., Álvarez-Merz, I. et al. Accelerating Leigh syndrome drug discovery through deep learning screening in brain organoids. Nat Commun 17, 3570 (2026). https://doi.org/10.1038/s41467-026-71391-2
Ключевые слова: синдром Лея, мозговые органоиды, глубинное обучение, репозиционирование лекарств, митохондриальная болезнь