Clear Sky Science · pl
Przyspieszanie odkrywania leków na zespół Leigha przez przesiew głębokiego uczenia w organoidach mózgowych
Nowa nadzieja dla wyniszczającej choroby mózgu u dzieci
Zespół Leigha to rzadka, często śmiertelna choroba, która dotyka niemowlęta i małe dzieci, pozbawiając ich mózgu energii potrzebnej do wzrostu i funkcjonowania. Rodziny obecnie nie mają sprawdzonych terapii, jedynie opiekę wspomagającą. To badanie łączy najnowocześniejszą biologię i sztuczną inteligencję, by przeszukiwać istniejące leki, które mogłyby pomóc. Poprzez połączenie komputerowych prognoz z miniaturowymi modelami mózgu hodowanymi w laboratorium, badacze identyfikują dwa leki, które częściowo przywracają aktywność przypominającą mózgową w modelach zespołu Leigha, wskazując szybszą drogę do odkrywania terapii dla rzadkich chorób dziecięcych.
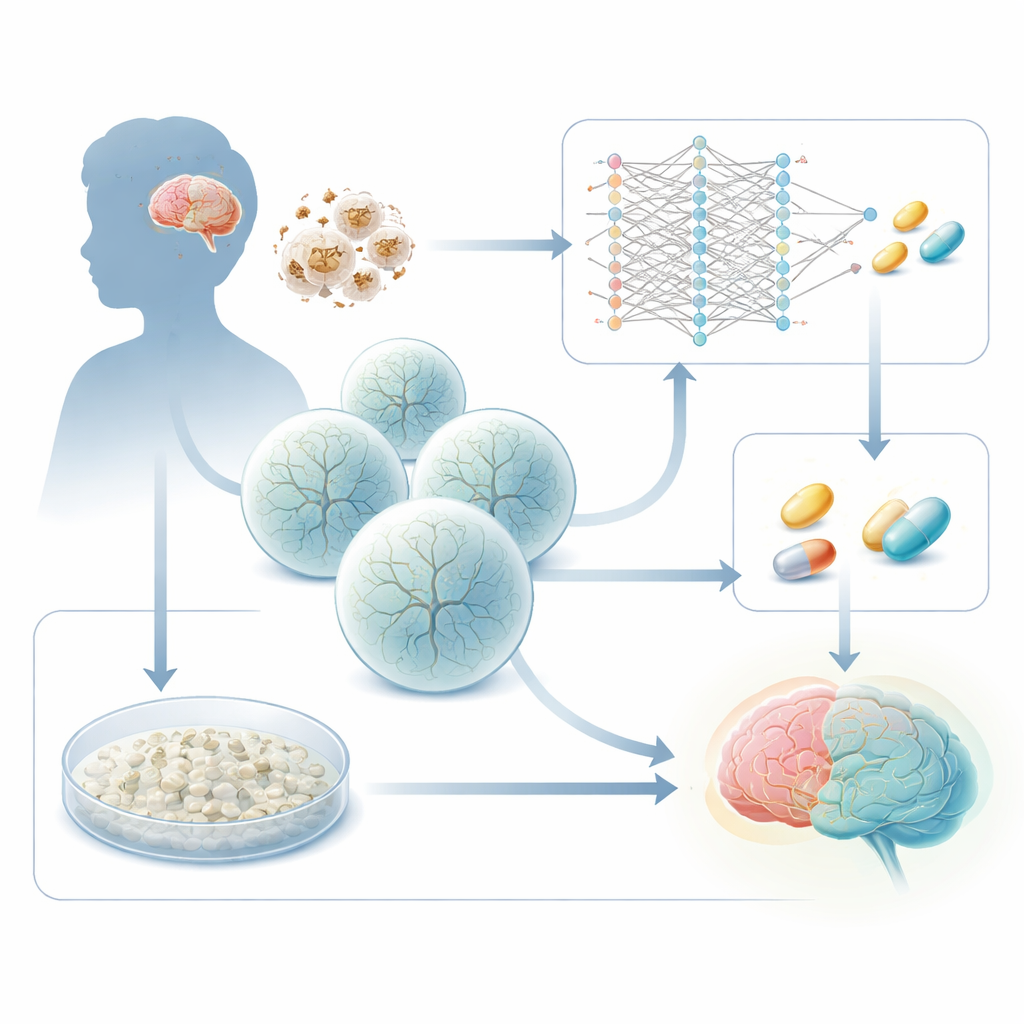
Jak niewydolność energetyczna szkodzi rozwijającemu się mózgowi
Zespół Leigha jest spowodowany dziedzicznymi wadami genów, które zasilają mitochondria, „baterie” komórki. Jednym z częstych winowajców jest gen o nazwie SURF1, niezbędny do kluczowego etapu w komórkowym mechanizmie wytwarzania energii. Gdy SURF1 jest uszkodzony, obszary mózgu o dużym zapotrzebowaniu na energię — szczególnie głębokie struktury śródmózgowia i jądra podstawy — zaczynają zawodzić. Wcześniejsze prace tej grupy wykorzystały komórki macierzyste pochodzące od pacjentów do hodowli trójwymiarowych organoidów mózgowych i wykazały, że organoidy z zespołem Leigha słabo tworzą neurony, z nieprawidłowym rozgałęzieniem i okablowaniem. Nowe badanie stawia praktyczne pytanie: czy te chorobowe zmiany można wykorzystać jako odczyt do znalezienia leków, które popchną chore komórki z powrotem na ścieżkę prawidłowego rozwoju?
Nauczanie komputerów proponowania pomocnych leków
Jednym z filarów projektu jest ramie głębokiego uczenia zbudowane specjalnie dla komórek niezwiązanych z nowotworami. Zamiast jedynie dopasowywać sygnatury genów chorobowych do katalogu odpowiedzi na leki, algorytm uczy się, jak sieci kontroli genów zmieniają się, gdy młode komórki mózgowe przechodzą od glejowych komórek promienistych przypominających komórki macierzyste, przez pośrednie progenitory, do dojrzałych neuronów. Wykorzystując sekwencjonowanie RNA pojedynczych komórek z organoidów mózgowych pochodzących od pacjentów z zespołem Leigha i od zdrowych kontroli, model wyznacza, które czynniki transkrypcyjne należy „popchnąć”, aby chore komórki podążyły normalną ścieżką rozwojową. Następnie przeszukuje dużą bazę danych leków i przewiduje, które związki powinny „kierować” siecią ze stanu przypominającego Leigha w stronę zdrowszego stanu neuronalnego. Z tysięcy kandydatów zawęża listę do kilku tuzinów leków o obiecującym wpływie na metabolizm komórkowy.
Pozwalanie drożdżom i mini‑mózgom głosować na najlepsze kandydaty
Równolegle zespół przeprowadza zupełnie inny przesiew w drożdżach. Drożdże piekarskie mają swoją wersję genu SURF1, a jego usunięcie sprawia, że komórki stają się wrażliwe przy niedoborze składników odżywczych — echo stresu energetycznego w zespole Leigha. Badacze wystawiają drożdże pozbawione SURF1 na 2250 już zatwierdzonych leków i mierzą, które chemikalia najlepiej ratują przeżywalność. Co ciekawe, zarówno ekran sztucznej inteligencji, jak i test przeżycia w drożdżach wskazują na tę samą rodzinę związków: azole, grupę znaną głównie jako leki przeciwgrzybicze i dermatologiczne. Z tej grupy zespół koncentruje się na dwóch związkach, talarozolu i sertakonazolu, które wydają się wystarczająco bezpieczne do długotrwałego narażenia w modelach komórkowych człowieka i które wyraźnie poprawiają wczesne formowanie neuronów w neuronach pochodzących od pacjentów z zespołem Leigha w hodowli.
Testowanie leków w ludzkich organoidach śródmózgowia
Aby przybliżyć się do obszarów mózgu dotkniętych chorobą u pacjentów, badacze generują organoidy śródmózgowia z progenitorów nerwowych pochodzących od pacjentów. Te 3D struktury zawierają neurony produkujące dopaminę, komórki wspierające i rozwijające się obwody. W porównaniu z organoidami z komórek zdrowych, organoidy Leigha rosną większe, ale mają gorszą strukturę neuronalną, wydzielają więcej kwasu mlekowego do pożywki i reagują nieprawidłowo przy ostrym stresie energetycznym. Leczenie organoidów śródmózgowia Leigha przez kilka tygodni niskimi dawkami talarozolu lub sertakonazolu spowalnia ich nadmierny wzrost, zmniejsza uwalnianie mleczanu o około jedną piątą i poprawia pewne miary funkcji neuronalnej. W szczególności talarozol zwiększa liczbę neuronów przypominających dopaminergiczne i przywraca silniejszy sygnał wapniowy, kiedy organoidy są wystawione na nagłe pozbawienie energii, co sugeruje częściowe odzyskanie responsywności sieciowej.
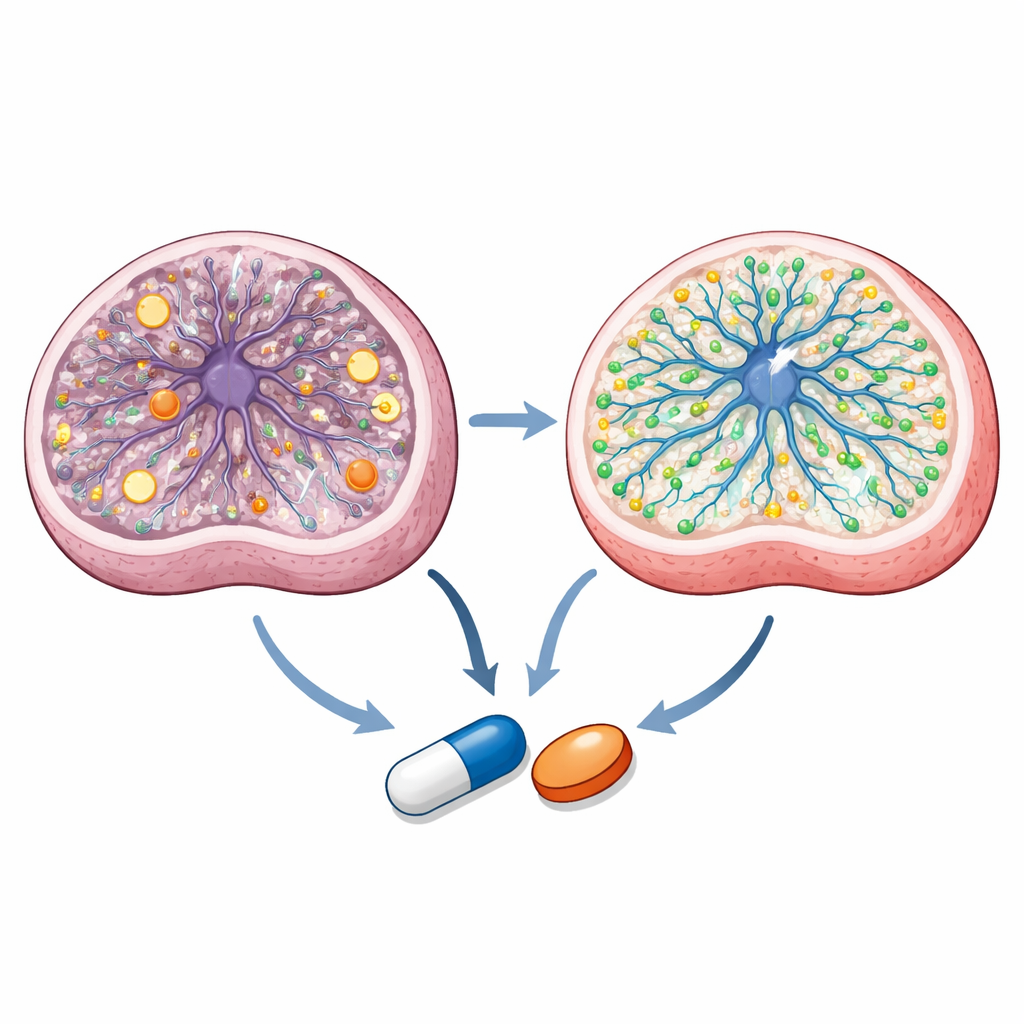
Odkrywanie, jak związki działają wewnątrz komórek
Bliższe badania wykazują, że oba azole działają przez częściowo nakładające się, lecz odrębne mechanizmy. Szczegółowe pomiary metabolitów pokazują, że progenitory nerwowe Leigha mają niezrównoważony stan energetyczny i zaburzoną chemię mitochondrialną. Talarozol normalizuje kluczowe stosunki energetyczne i kilka pośredników w centralnym cyklu metabolicznym komórki, podczas gdy oba leki korygują specyficzne wąskie gardła metaboliczne. Profilowanie lipidów i obrazowanie ujawniają, że sertakonazol wywiera silny wpływ na tłuszcze związane z błonami i cholesterol, przywracając niektóre sfingolipidy i zwiększając cholesterol związany z błoną, który jest obniżony w komórkach Leigha. Sekwencjonowanie RNA pojedynczych komórek leczonych organoidów wskazuje, że oba leki promują programy genowe powiązane z tworzeniem neuronów i metabolizmem lipidów, jednocześnie tłumiąc nadmiernie aktywną ekspresję genów mitochondrialnych. Obliczeniowe dokowanie i testy z reporterami w żywych komórkach sugerują ponadto, że talarozol oddziałuje z enzymami rozkładającymi kwas retinowy — pochodną witaminy A kluczową dla rozwoju mózgu — oraz aktywuje receptor jądrowy PPARγ, który był wskazywany jako potencjalny cel terapeutyczny w chorobach mitochondrialnych.
Co to może znaczyć dla dzieci z zespołem Leigha
Chociaż talarozol i sertakonazol nie odwracają całkowicie wszystkich cech choroby w tych modelach, konsekwentnie łagodzą kilka znamion zespołu Leigha w drożdżach, neuronach 2D i trójwymiarowych ludzkich organoidach śródmózgowia. Praca ta pokazuje, że połączenie głębokiego uczenia, ludzkich organoidów i prostych przesiewów w drożdżach może szybko wyłowić leki nadające się do ponownego zastosowania przy rzadkim schorzeniu pediatrycznym, dla którego brak jest obecnie terapii. Dla rodzin nie przekłada się to jeszcze na zatwierdzoną terapię, ale dostarcza dwóch konkretnych kandydatów oraz, być może ważniejsze, ogólnej strategii: użyj zaawansowanych obliczeń, aby przesiać ogromne biblioteki leków, a następnie przetestuj najbardziej obiecujące trafienia w realistycznych ludzkich modelach mini‑mózgu. To podejście może skrócić drogę od podstawowej biologii do istotnych opcji terapeutycznych dla zespołu Leigha i innych chorób rozwojowych układu nerwowego związanych z dysfunkcją mitochondrialną.
Cytowanie: Menacho, C., Okawa, S., Álvarez-Merz, I. et al. Accelerating Leigh syndrome drug discovery through deep learning screening in brain organoids. Nat Commun 17, 3570 (2026). https://doi.org/10.1038/s41467-026-71391-2
Słowa kluczowe: zespół Leigha, organoidy mózgowe, głębokie uczenie, ponowne zastosowanie leków, choroba mitochondrialna