Clear Sky Science · de
Beschleunigte Wirkstoffforschung bei Leigh‑Syndrom durch Deep‑Learning‑Screening in Gehirn‑Organoiden
Neue Hoffnung für eine verheerende kindliche Hirnerkrankung
Das Leigh‑Syndrom ist eine seltene, häufig tödliche Erkrankung, die Säuglinge und Kleinkinder trifft und ihrem Gehirn die Energie raubt, die es zum Wachsen und Funktionieren braucht. Familien stehen derzeit keine nachgewiesenen Therapien zur Verfügung, nur unterstützende Maßnahmen. Diese Studie verbindet modernste Biologie mit künstlicher Intelligenz, um existierende Medikamente zu durchsuchen, die helfen könnten. Durch die Kombination von computergeleiteten Vorhersagen mit winzigen, im Labor gezüchteten Gehirnmodellen identifizieren die Forschenden zwei Wirkstoffe, die die gehirnähnliche Aktivität in Modellen des Leigh‑Syndroms teilweise wiederherstellen und damit auf einen schnelleren Weg zur Entdeckung von Therapien für seltene Kinderkrankheiten hinweisen.
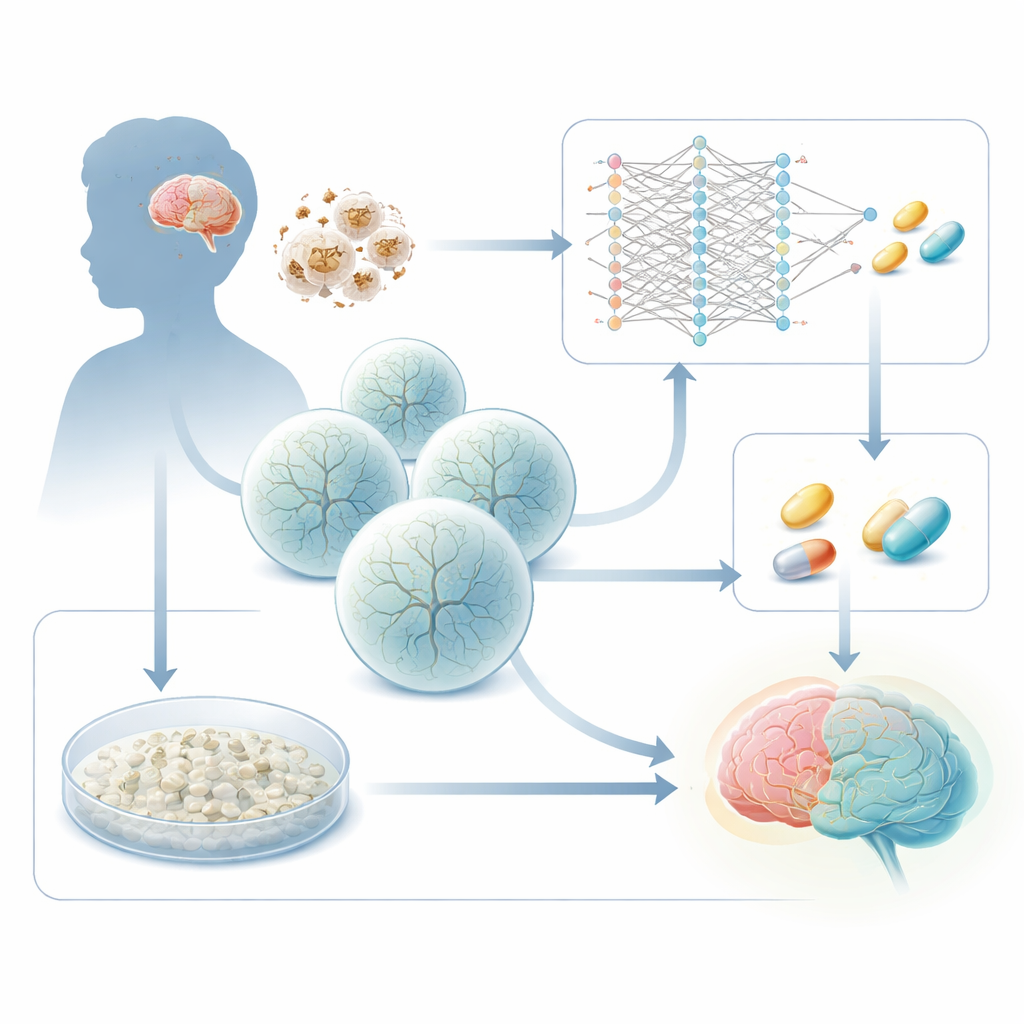
Wie Energiemangel das sich entwickelnde Gehirn schädigt
Das Leigh‑Syndrom wird durch vererbte Defekte in Genen verursacht, die die Mitochondrien — die „Batterien“ der Zelle — antreiben. Ein häufiger Übeltäter ist ein Gen namens SURF1, das für einen wichtigen Schritt in der energieproduzierenden Maschinerie der Zelle benötigt wird. Wenn SURF1 defekt ist, versagen besonders energieintensive Hirnregionen — vor allem tief gelegene Strukturen im Mittelhirn und den Basalganglien. Frühere Arbeiten dieser Gruppe verwendeten patientenabgeleitete Stammzellen zur Züchtung dreidimensionaler Organoide und zeigten, dass Leigh‑Organoide Neuronen schlecht bilden, mit ungewöhnlicher Verzweigung und Vernetzung. Die neue Studie stellt eine praktische Frage: Lassen sich diese krankheitsspezifischen Veränderungen als Ausleseparameter nutzen, um Medikamente zu finden, die erkrankte Zellen wieder in Richtung normaler Entwicklung treiben?
Computern beibringen, hilfreiche Medikamente vorzuschlagen
Ein Zweig des Projekts nutzt ein Deep‑Learning‑Framework, das speziell für nicht‑tumorale Zellen entwickelt wurde. Anstatt lediglich Krankheitsgen‑Signaturen mit einem Katalog von Arzneimittelantworten abzugleichen, lernt der Algorithmus, wie sich Gensteuerungsnetzwerke verschieben, wenn junge Gehirnzellen vom stammeshigen radialen Glia‑Status über intermediäre Vorläufer bis zu reifen Neuronen fortschreiten. Anhand von Einzelzell‑RNA‑Sequenzdaten aus Leigh‑ und gesunden zerebralen Organoiden schließt das Modell, welche Transkriptionsfaktoren moduliert werden müssen, um kranke Zellen auf den normalen Entwicklungsweg zu schieben. Anschließend durchsucht es eine große Arzneimitteldatenbank und sagt voraus, welche Verbindungen das Netzwerk aus einem Leigh‑ähnlichen Zustand in einen gesünderen neuronalen Zustand „steuern“ sollten. Aus Tausenden von Kandidaten reduziert es die Liste auf einige Dutzend Wirkstoffe mit vielversprechenden Effekten auf den zellulären Stoffwechsel.
Hefe und Mini‑Gehirne über die besten Kandidaten abstimmen lassen
Parallel dazu führt das Team ein ganz anderes Screen in Hefe durch. Backhefe besitzt eine eigene Version des SURF1‑Gens, und dessen Löschung macht die Zellen bei Nährstoffmangel verwundbar — ein Echo des Energiestresses beim Leigh‑Syndrom. Die Forschenden setzen SURF1‑defiziente Hefezellen 2.250 bereits zugelassenen Arzneimitteln aus und messen, welche Chemikalien das Überleben am besten retten. Interessanterweise deuten sowohl der KI‑Screen als auch der Hefe‑Überlebens‑Test auf dieselbe Wirkstofffamilie hin: Azole, eine Gruppe, die eher als Antimykotika und Dermatologika bekannt ist. Aus diesen konzentriert sich das Team auf zwei Verbindungen, Talarozol und Sertaconazol, die in menschlichen Zellmodellen offenbar ausreichend sicher für eine Langzeitexposition sind und die die frühe Neuronenbildung in Leigh‑abgeleiteten Neuronen in der Kultur deutlich verbessern.
Prüfung der Medikamente in menschlichen Mittelhirn‑Organoiden
Um den vom Patienten betroffenen Hirnregionen näherzukommen, erzeugen die Forschenden Mittelhirn‑Organoide aus patientenabgeleiteten neuralen Vorläuferzellen. Diese 3D‑Strukturen enthalten dopaminproduzierende Neuronen, Stütz‑/Gliazellen und sich entwickelnde Schaltkreise. Im Vergleich zu Organoiden aus gesunden Zellen wachsen Leigh‑Organoide größer, weisen jedoch eine schlechtere neuronale Struktur auf, geben mehr Milchsäure in das Kulturmedium ab und reagieren bei akutem Energiemangel abnormal. Eine mehrwöchige Behandlung der Leigh‑Mittelhirn‑Organoide mit niedrigen Dosen von Talarozol oder Sertaconazol bremst ihr übermäßiges Wachstum, reduziert die Laktatausschüttung um etwa ein Fünftel und verbessert einige Messgrößen der neuronalen Funktion. Insbesondere Talarozol erhöht die Zahl dopaminartiger Neuronen und stellt ein stärkeres Calciumsignal wieder her, wenn die Organoide einer plötzlichen Energieentziehung ausgesetzt werden, was auf eine teilweise Wiederherstellung der Netzwerkreaktivität hindeutet.
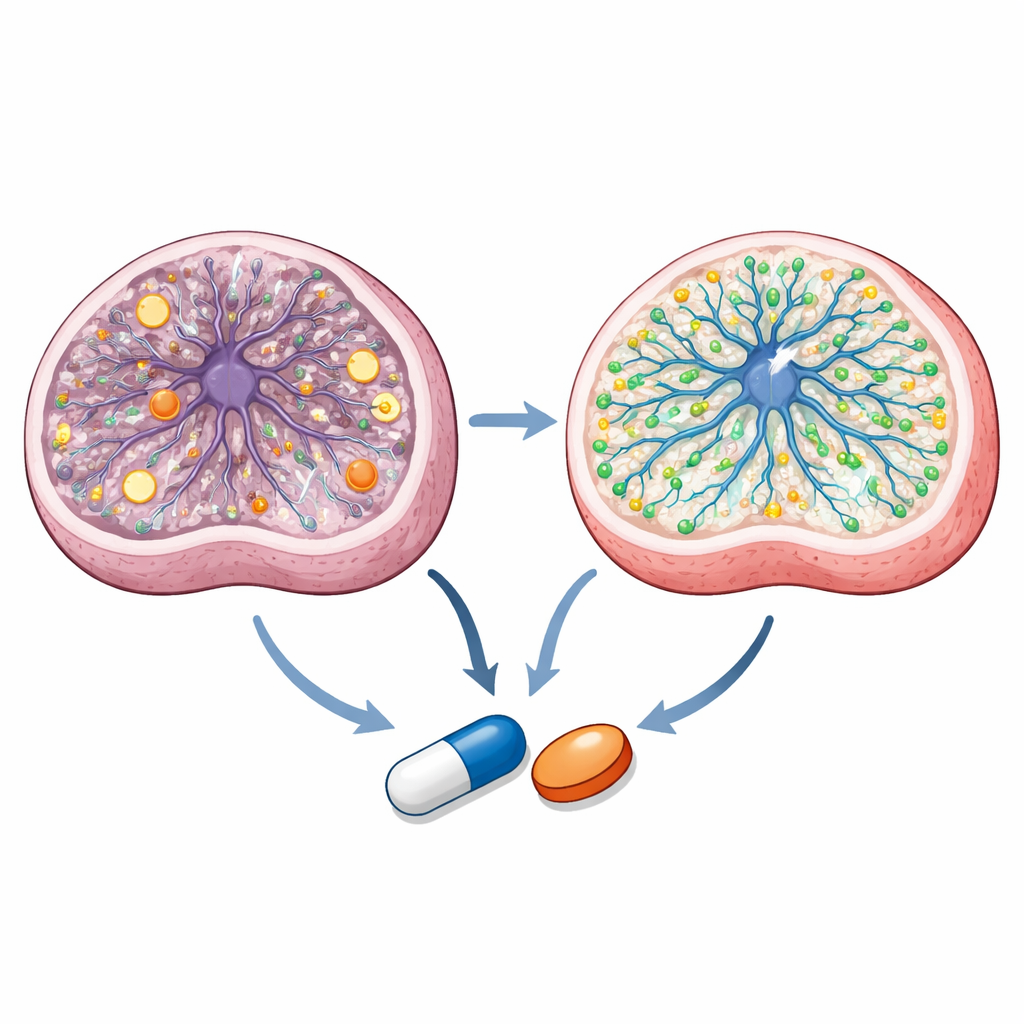
Aufdecken, wie die Verbindungen in Zellen wirken
Bei tiefer gehenden Untersuchungen stellt das Team fest, dass die beiden Azol‑Wirkstoffe über überlappende, aber unterschiedliche Wege wirken. Detaillierte Metabolitmessungen zeigen, dass neurale Vorläuferzellen aus Leigh‑Proben einen unausgewogenen Energiestatus und gestörte mitochondriale Chemie aufweisen. Talarozol normalisiert entscheidende Energieverhältnisse und mehrere Zwischenprodukte im zentralen Stoffwechselkreis der Zelle, während beide Medikamente spezifische metabolische Engpässe korrigieren. Lipidprofile und Bildgebung zeigen, dass Sertaconazol starken Einfluss auf membranassoziierte Fette und Cholesterin hat, bestimmte Sphingolipide wiederherstellt und membrangebundenes Cholesterin erhöht, das in Leigh‑Zellen reduziert ist. Einzelzell‑RNA‑Sequenzierung behandelter Organoide weist darauf hin, dass beide Medikamente Genprogramme fördern, die mit Neurongenese und Lipidstoffwechsel verbunden sind, während sie überaktive mitochondriale Genexpression dämpfen. Computergestütztes Docking und Live‑Cell‑Reporter‑Assays deuten ferner darauf hin, dass Talarozol Enzyme angreift, die Retinsäure abbauen — ein Vitamin‑A‑Derivat, das für die Gehirnentwicklung entscheidend ist — und einen nukleären Rezeptor namens PPARγ aktiviert, der als therapeutischer Ansatzpunkt bei mitochondrialen Erkrankungen diskutiert wird.
Was das für Kinder mit Leigh‑Syndrom bedeuten könnte
Obwohl Talarozol und Sertaconazol in diesen Modellen nicht alle Krankheitsmerkmale vollständig rückgängig machen, mildern sie konsistent mehrere Kennzeichen des Leigh‑Syndroms in Hefe, 2D‑Neuronen und 3D‑menschlichen Mittelhirn‑Organoiden. Die Arbeit zeigt, dass die Kombination von Deep Learning mit menschlichen Organoiden und einfachen Hefescreens schnell auf repositionierbare Medikamente für eine seltene pädiatrische Erkrankung zielen kann, für die es derzeit keine Therapien gibt. Für betroffene Familien ergibt sich daraus noch keine zugelassene Behandlung, wohl aber zwei konkrete Arzneimittelkandidaten und, vielleicht noch wichtiger, eine allgemeine Strategie: fortschrittliche Rechenmethoden nutzen, um riesige Wirkstoffbibliotheken zu filtern, und die vielversprechendsten Treffer anschließend in realistischen menschlichen Mini‑Gehirn‑Modellen testen. Dieser Ansatz könnte den Weg von der Grundlagenbiologie zu sinnvollen Behandlungsoptionen für das Leigh‑Syndrom und andere neuroentwicklungsbedingte Erkrankungen mit mitochondrialer Dysfunktion verkürzen.
Zitation: Menacho, C., Okawa, S., Álvarez-Merz, I. et al. Accelerating Leigh syndrome drug discovery through deep learning screening in brain organoids. Nat Commun 17, 3570 (2026). https://doi.org/10.1038/s41467-026-71391-2
Schlüsselwörter: Leigh‑Syndrom, Gehirn‑Organoide, Deep Learning, Wirkstoff‑Repositionierung, mitochondriale Erkrankung