Clear Sky Science · ja
脳オルガノイドでの深層学習スクリーニングにより加速するリー症候群の創薬
壊滅的な小児脳疾患に新たな希望を見いだす
リー症候群はまれでしばしば致命的な疾患で、生後まもない乳児や幼児の脳から成長と機能に必要なエネルギーを奪います。現在、家族に提供できるのは症状を和らげる対症療法のみで、確立された治療法はありません。本研究は最先端の生物学と人工知能を結び付け、既存の薬剤の中から効果が期待できるものを探索します。計算に基づく予測と実験室で育てた小さな脳モデルを組み合わせることで、研究者らはリー症候群モデルで脳様活動を部分的に回復させる二つの薬剤を特定し、希少な小児疾患に対する治療薬発見を迅速化する道筋を示しました。
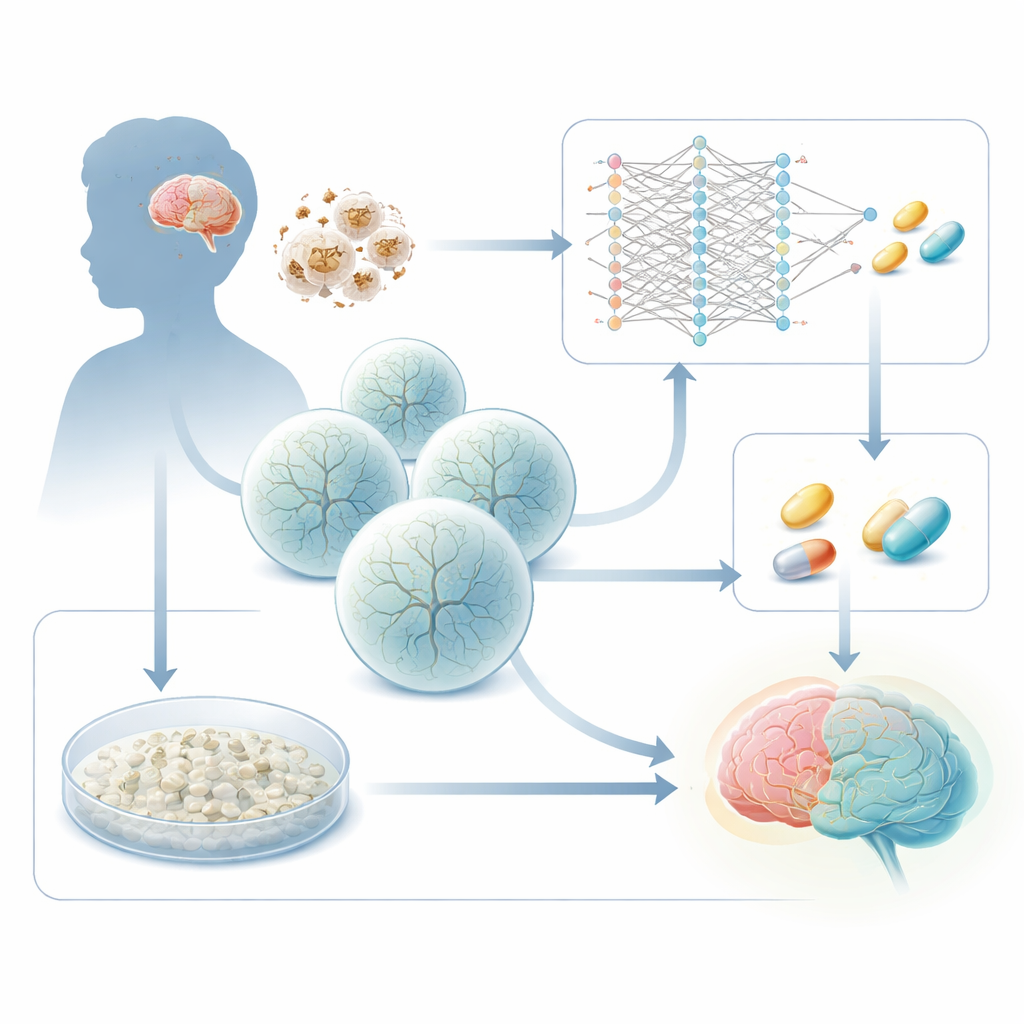
発達中の脳がエネルギー欠乏で損なわれる仕組み
リー症候群は細胞の“バッテリー”であるミトコンドリアを駆動する遺伝子の遺伝的欠陥により引き起こされます。よく知られた原因の一つがSURF1という遺伝子で、細胞のエネルギー産生機構の重要な段階に必要です。SURF1が機能不全になると、エネルギー需要の高い脳領域、特に中脳や基底核の深部が障害を受け始めます。本グループの先行研究では、患者由来の幹細胞から3次元の脳オルガノイドを作製し、リー由来オルガノイドではニューロンの形成が不十分で、樹状突起や配線が異常であることを示しました。本研究は実践的な問いを投げかけます:こうした疾患特異的変化をリードアウトとして利用し、病的な細胞を正常な発達軌道へ戻す薬剤を見つけられるか?
コンピュータに有効な薬を示唆させる
研究の一端は、非がん細胞向けに特化して構築された深層学習フレームワークを用いています。単に疾患の遺伝子シグネチャを薬剤反応のカタログと突き合わせるのではなく、アルゴリズムは若い脳細胞が放射状グリアのような幹様状態から中間前駆細胞、成熟ニューロンへと進む過程で遺伝子制御ネットワークがどのように変化するかを学習します。リーと健常の脳オルガノイドから得られた単一細胞RNAシーケンスを用いて、モデルは病的な細胞を正常な発達経路へ押し戻すためにどの転写因子を調節すべきかを推定します。次に大規模な薬剤データベースを探索し、リー様状態からより健康なニューロン状態へ「舵を取る」ことが期待される化合物を予測します。何千もの候補から、細胞代謝に有望な影響を持つ数十の薬剤へと絞り込みます。
酵母とミニ脳により最良候補を選別する
並行して、チームはまったく異なる酵母スクリーニングも実施します。パン酵母にはSURF1に相当する遺伝子があり、それを欠失させると栄養が乏しい条件下で細胞が脆弱になります—これはリー症候群におけるエネルギー欠乏の類推です。研究者らはSURF1欠損酵母を2,250種の既承認薬で処理し、生存を最もよく回復させる化学物質を測定しました。興味深いことに、人工知能スクリーニングと酵母生存テストの両方が同じ化学族を指し示しました:アゾール系薬剤で、通常は抗真菌や皮膚科薬として知られる一群です。そこから研究者らは、長期曝露に対してヒト細胞モデルで十分に安全に見え、リー由来ニューロンの初期形成を強く改善するタラロザールとセルタコナゾールの二つに注目しました。
ヒト中脳オルガノイドでの薬剤試験
患者由来の神経前駆細胞から中脳オルガノイドを作成し、患者の影響を受けやすい脳領域により近づける試みを行いました。これらの3次元構造にはドーパミン産生ニューロン、支持細胞、および形成中の回路が含まれます。健常由来オルガノイドと比較して、リー由来オルガノイドはより大きく成長する一方でニューロン構造は劣り、培養培地への乳酸放出が増加し、急性のエネルギーストレスにさらされると異常な反応を示します。低用量のタラロザールまたはセルタコナゾールで数週間処理すると、リー中脳オルガノイドの過剰成長が緩和され、乳酸放出は約5分の1低下し、いくつかのニューロン機能の指標が改善しました。特にタラロザールはドーパミン様ニューロンの数を増やし、エネルギー欠乏の急性刺激に対してカルシウム信号の応答性を回復させ、ネットワークの応答性が部分的に回復したことを示唆しました。
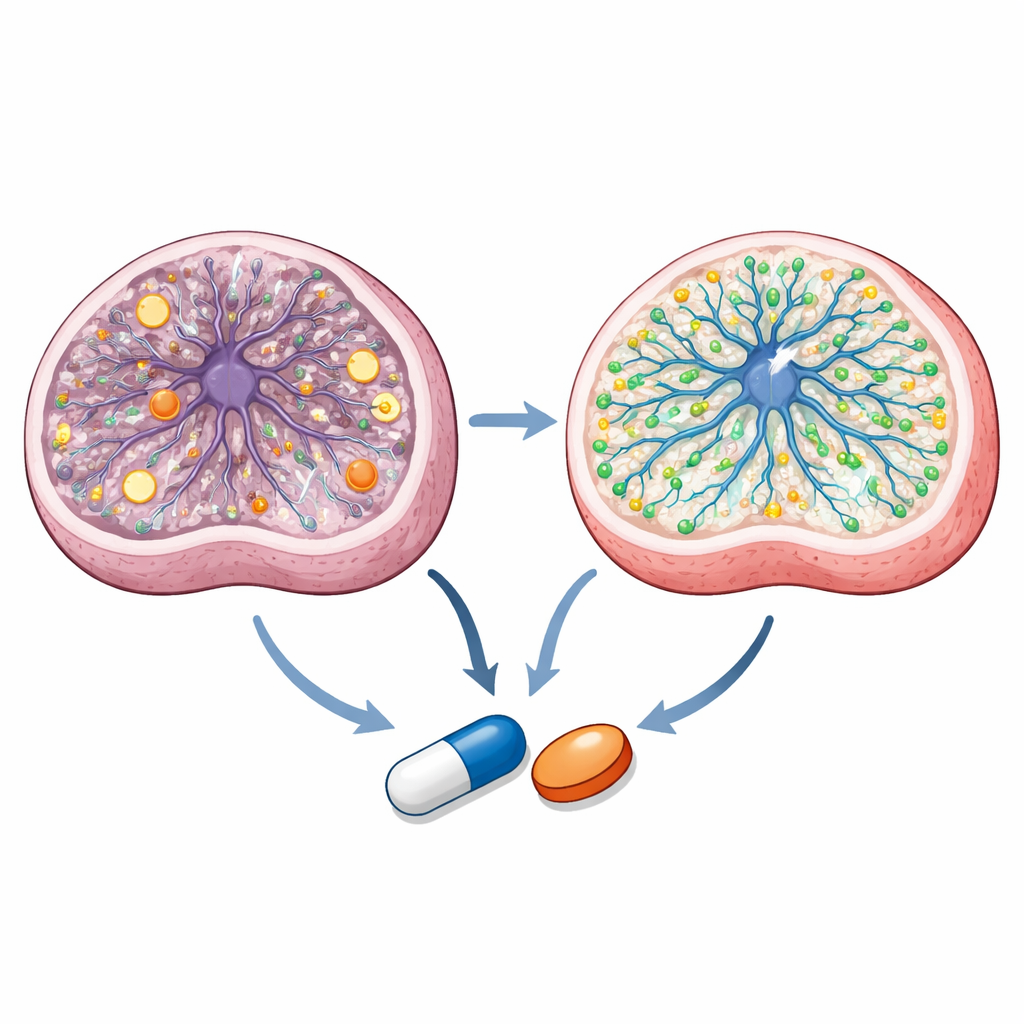
細胞内で化合物がどのように作用するかを解明する
さらに詳しく調べると、二つのアゾール薬は重なりつつも異なる経路で作用することがわかりました。詳細な代謝物測定は、リー由来の神経前駆細胞がエネルギー状態の不均衡とミトコンドリア化学の撹乱を抱えていることを示します。タラロザールは重要なエネルギー比や細胞の中心的代謝サイクルのいくつかの中間体を正常化し、両薬剤はいくつかの特定の代謝ボトルネックを是正します。脂質プロファイル解析とイメージングは、セルタコナゾールが膜関連脂質とコレステロールに強い影響を与え、特定のスフィンゴ脂質を回復させ、リー細胞で低下していた膜結合コレステロールを増加させることを明らかにしました。処理したオルガノイドの単一細胞RNAシーケンスは、両薬剤がニューロン生成や脂質代謝に関連する遺伝子プログラムを促進し、一方で過剰なミトコンドリア遺伝子発現を抑えることを示します。計算ドッキングと生細胞レポーターアッセイはさらに、タラロザールが脳発達に重要なビタミンA誘導体であるレチノイン酸を分解する酵素に作用し、ミトコンドリア疾患の治療標的として示唆されてきた核内受容体PPARγを活性化する可能性を示唆しました。
リー症候群の子どもたちにとっての意味
タラロザールとセルタコナゾールはこれらのモデルの全ての疾患特徴を完全に逆転させるわけではありませんが、酵母、2Dニューロン、3Dヒト中脳オルガノイドにまたがってリー症候群のいくつかの特徴を一貫して緩和しました。この研究は、深層学習とヒトオルガノイド、そして単純な酵母スクリーニングを組み合わせることで、治療法のない希少小児疾患に対して再利用可能な薬剤を迅速に特定できることを示しています。家族にとって、これは直ちに承認された治療法が得られるという意味ではありませんが、二つの具体的な薬剤候補を提供するとともに、より重要な点として一般的な戦略を示しています:高度な計算で巨大な薬剤ライブラリを絞り込み、有望なヒットを現実的なヒトのミニ脳モデルで検証する。こうしたアプローチは、基礎生物学からリー症候群やミトコンドリア機能障害に根ざす他の神経発達疾患に対する有意義な治療選択肢へ至る道を短縮する可能性があります。
引用: Menacho, C., Okawa, S., Álvarez-Merz, I. et al. Accelerating Leigh syndrome drug discovery through deep learning screening in brain organoids. Nat Commun 17, 3570 (2026). https://doi.org/10.1038/s41467-026-71391-2
キーワード: リー症候群, 脳オルガノイド, 深層学習, 薬剤再利用, ミトコンドリア病