Clear Sky Science · fr
Accélérer la découverte de traitements pour le syndrome de Leigh grâce au criblage par apprentissage profond dans des organoïdes cérébraux
Trouver un nouvel espoir pour une maladie cérébrale infantile dévastatrice
Le syndrome de Leigh est une maladie rare, souvent mortelle, qui touche les nourrissons et les jeunes enfants, privant leur cerveau de l’énergie nécessaire à sa croissance et à son fonctionnement. Les familles n’ont aujourd’hui aucun traitement éprouvé, seulement des soins de soutien. Cette étude réunit des approches biologiques de pointe et l’intelligence artificielle pour rechercher des médicaments existants susceptibles d’être utiles. En combinant des prédictions guidées par ordinateur avec de petits modèles cérébraux cultivés en laboratoire, les chercheurs identifient deux médicaments qui restaurent partiellement l’activité de type cérébral dans des modèles du syndrome de Leigh, ouvrant la voie à une méthode plus rapide pour découvrir des thérapies pour les maladies infantiles rares.
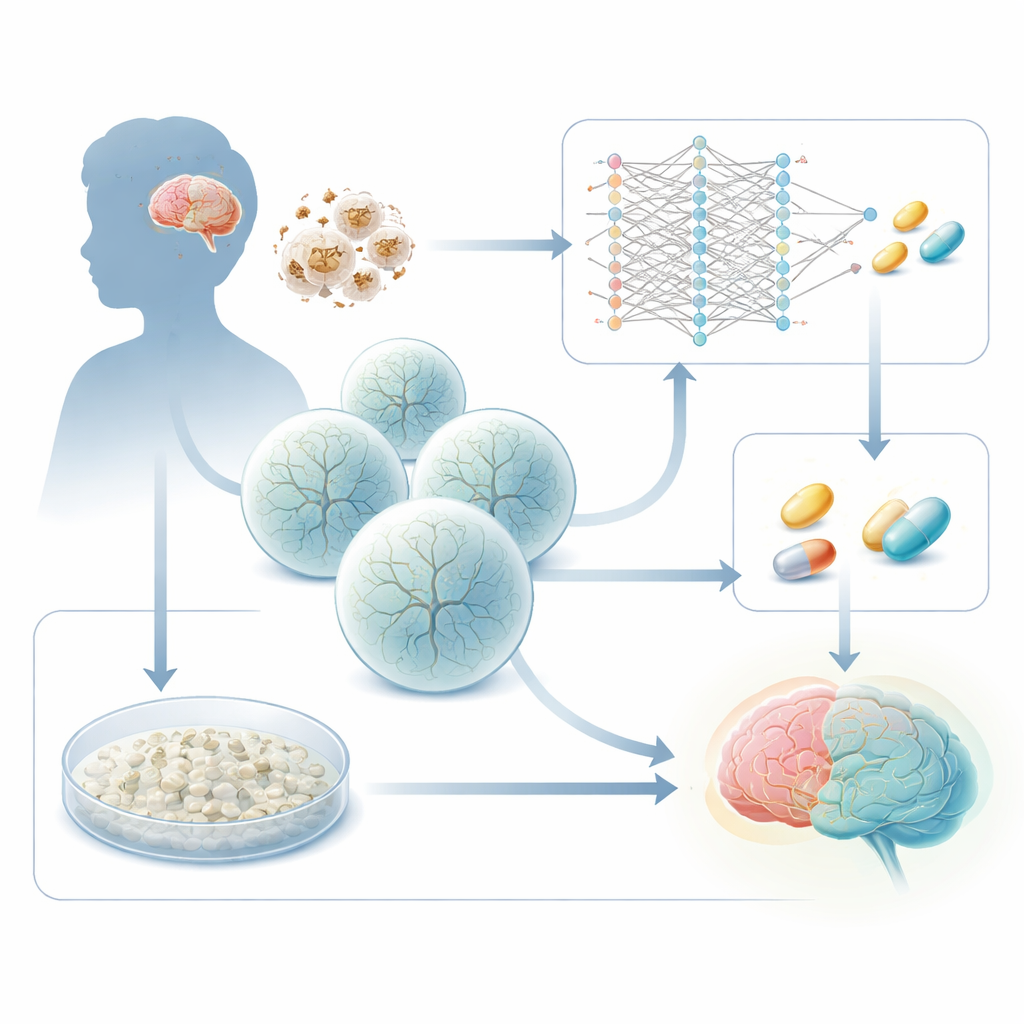
Comment la défaillance énergétique nuit au cerveau en développement
Le syndrome de Leigh est causé par des anomalies héréditaires de gènes qui alimentent les mitochondries, les « batteries » de la cellule. Un coupable fréquent est le gène SURF1, nécessaire à une étape clé de la machinerie de production d’énergie cellulaire. Lorsque SURF1 est défectueux, les régions cérébrales très exigeantes en énergie — en particulier des structures profondes du tronc cérébral et des ganglions de la base — commencent à faillir. Des travaux antérieurs de ce groupe ont utilisé des cellules souches dérivées de patients pour cultiver des organoïdes cérébraux 3D et ont montré que les organoïdes de Leigh génèrent mal les neurones, avec des ramifications et des connexions anormales. La nouvelle étude pose une question pratique : ces altérations spécifiques de la maladie peuvent‑elles servir de signal de lecture pour trouver des médicaments qui ramèneraient les cellules malades vers un développement plus normal ?
Apprendre aux ordinateurs à proposer des médicaments utiles
Un volet du projet utilise un cadre d’apprentissage profond conçu spécifiquement pour des cellules non cancéreuses. Plutôt que de simplement mettre en correspondance des signatures génétiques de la maladie avec un catalogue de réponses aux médicaments, l’algorithme apprend comment les réseaux de contrôle génétique évoluent lorsque les jeunes cellules cérébrales progressent de la glie radiale de type souches, aux progéniteurs intermédiaires, puis aux neurones matures. En utilisant le séquençage de l’ARN à cellule unique provenant d’organoïdes cérébraux de Leigh et sains, le modèle infère quels facteurs de transcription doivent être modulés pour faire progresser les cellules malades le long du parcours de développement normal. Il parcourt ensuite une large base de données de médicaments et prédit quels composés devraient « orienter » le réseau d’un état de type Leigh vers un état neuronal plus sain. Parmi des milliers de candidats, il restreint la liste à quelques dizaines de médicaments ayant des effets prometteurs sur le métabolisme cellulaire.
Laisser la levure et les mini‑cerveaux départager les meilleurs candidats
En parallèle, l’équipe effectue un criblage très différent sur de la levure. La levure de boulanger possède sa propre version du gène SURF1, et sa suppression rend les cellules vulnérables quand les nutriments sont rares — un écho du stress énergétique observé dans le syndrome de Leigh. Les chercheurs exposent des levures déficientes en SURF1 à 2 250 médicaments déjà approuvés et mesurent quels composés sauvent le mieux la survie. Fait intrigant, à la fois le criblage par intelligence artificielle et le test de survie chez la levure pointent vers la même famille chimique : les azolés, un groupe mieux connu comme antifongique et utilisé en dermatologie. Parmi ceux‑ci, l’équipe se concentre sur deux composés, le talarozole et la sertaconazole, qui semblent suffisamment sûrs pour une exposition prolongée dans des modèles cellulaires humains et qui améliorent fortement la formation précoce des neurones dans des neurones dérivés de patients en culture.
Tester les médicaments dans des organoïdes de mésencéphale humain
Pour se rapprocher des régions cérébrales affectées chez les patients, les chercheurs génèrent des organoïdes de mésencéphale à partir de cellules progénitrices neurales dérivées de patients. Ces structures 3D contiennent des neurones producteurs de dopamine, des cellules de soutien et des circuits en développement. Par rapport aux organoïdes issus de cellules saines, les organoïdes de Leigh croissent davantage mais présentent une structure neuronale plus pauvre, libèrent davantage d’acide lactique dans le milieu de culture et réagissent de façon anormale lorsqu’ils sont soumis à un stress énergétique aigu. Un traitement des organoïdes de mésencéphale de Leigh pendant plusieurs semaines avec de faibles doses de talarozole ou de sertaconazole freine leur croissance excessive, réduit la libération de lactate d’environ un cinquième et améliore certaines mesures de la fonction neuronale. Le talarozole, en particulier, augmente le nombre de neurones de type dopaminergique et restaure un signal calcique plus fort lorsque les organoïdes sont mis au défi par une privation d’énergie soudaine, suggérant une récupération partielle de la réactivité du réseau.
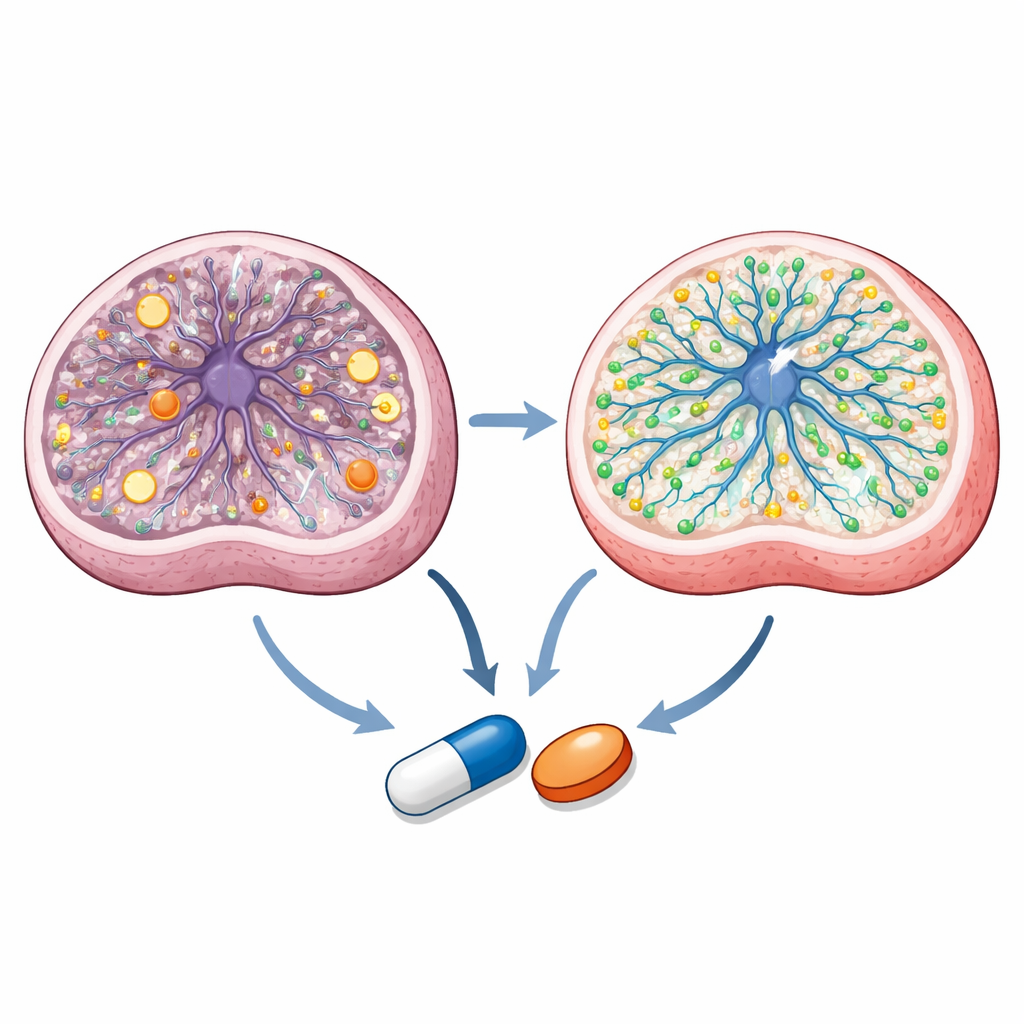
Découvrir comment les composés agissent à l’intérieur des cellules
En creusant davantage, l’équipe constate que les deux médicaments azolés agissent par des voies qui se recoupent mais restent distinctes. Des mesures détaillées des métabolites montrent que les cellules progénitrices neurales de Leigh présentent un état énergétique déséquilibré et une chimie mitochondriale perturbée. Le talarozole normalise des rapports énergétiques clés et plusieurs intermédiaires du cycle métabolique central de la cellule, tandis que les deux médicaments corrigent des goulots d’étranglement métaboliques spécifiques. Le profil lipidique et l’imagerie révèlent que la sertaconazole a un fort impact sur les graisses associées aux membranes et le cholestérol, restaurant certains sphingolipides et augmentant le cholestérol lié aux membranes, qui est réduit dans les cellules de Leigh. Le séquençage de l’ARN à cellule unique des organoïdes traités indique que les deux médicaments favorisent des programmes d’expression génique liés à la genèse neuronale et au métabolisme des lipides tout en atténuant une surexpression des gènes mitochondriaux. Des modélisations de docking computationnel et des essais sur cellules vivantes avec des rapports suggèrent en outre que le talarozole cible des enzymes qui dégradent l’acide rétinoïque — un dérivé de la vitamine A crucial pour le développement cérébral — et active un récepteur nucléaire appelé PPARγ, qui a été impliqué comme levier thérapeutique dans les maladies mitochondriales.
Ce que cela pourrait signifier pour les enfants atteints du syndrome de Leigh
Bien que le talarozole et la sertaconazole ne renversent pas complètement toutes les caractéristiques de la maladie dans ces modèles, ils atténuent de façon cohérente plusieurs marqueurs du syndrome de Leigh dans la levure, des neurones 2D et des organoïdes de mésencéphale humain 3D. Ce travail montre que la combinaison de l’apprentissage profond avec des organoïdes humains et des criblages simples sur levure peut rapidement cibler des médicaments réutilisables pour un trouble pédiatrique rare qui manque actuellement de traitements. Pour les familles, cela ne se traduit pas encore par une thérapie approuvée, mais cela fournit deux candidats médicamenteux concrets et, peut‑être plus important, une stratégie générale : utiliser des calculs avancés pour filtrer d’immenses bibliothèques de médicaments, puis tester les meilleures pistes dans des mini‑cerveaux humains réalistes. Cette approche pourrait raccourcir la route de la biologie fondamentale à des options de traitement significatives pour le syndrome de Leigh et d’autres maladies du développement neurologique ancrées dans un dysfonctionnement mitochondrial.
Citation: Menacho, C., Okawa, S., Álvarez-Merz, I. et al. Accelerating Leigh syndrome drug discovery through deep learning screening in brain organoids. Nat Commun 17, 3570 (2026). https://doi.org/10.1038/s41467-026-71391-2
Mots-clés: Syndrome de Leigh, organoïdes cérébraux, apprentissage profond, réaffectation de médicaments, maladie mitochondriale