Clear Sky Science · es
Acelerando el descubrimiento de fármacos para el síndrome de Leigh mediante cribado por aprendizaje profundo en organoides cerebrales
Encontrar nueva esperanza para una devastadora enfermedad cerebral infantil
El síndrome de Leigh es un trastorno raro y a menudo mortal que afecta a bebés y niños pequeños, privando a sus cerebros de la energía necesaria para crecer y funcionar. Actualmente, las familias no disponen de tratamientos probados, solo de cuidados de apoyo. Este estudio reúne biología de vanguardia e inteligencia artificial para buscar fármacos ya existentes que podrían ayudar. Al combinar predicciones guiadas por ordenador con pequeños modelos cerebrales cultivados en el laboratorio, los investigadores identifican dos medicamentos que restauran parcialmente la actividad similar a la cerebral en modelos del síndrome de Leigh, apuntando a una vía más rápida para descubrir terapias para enfermedades infantiles raras.
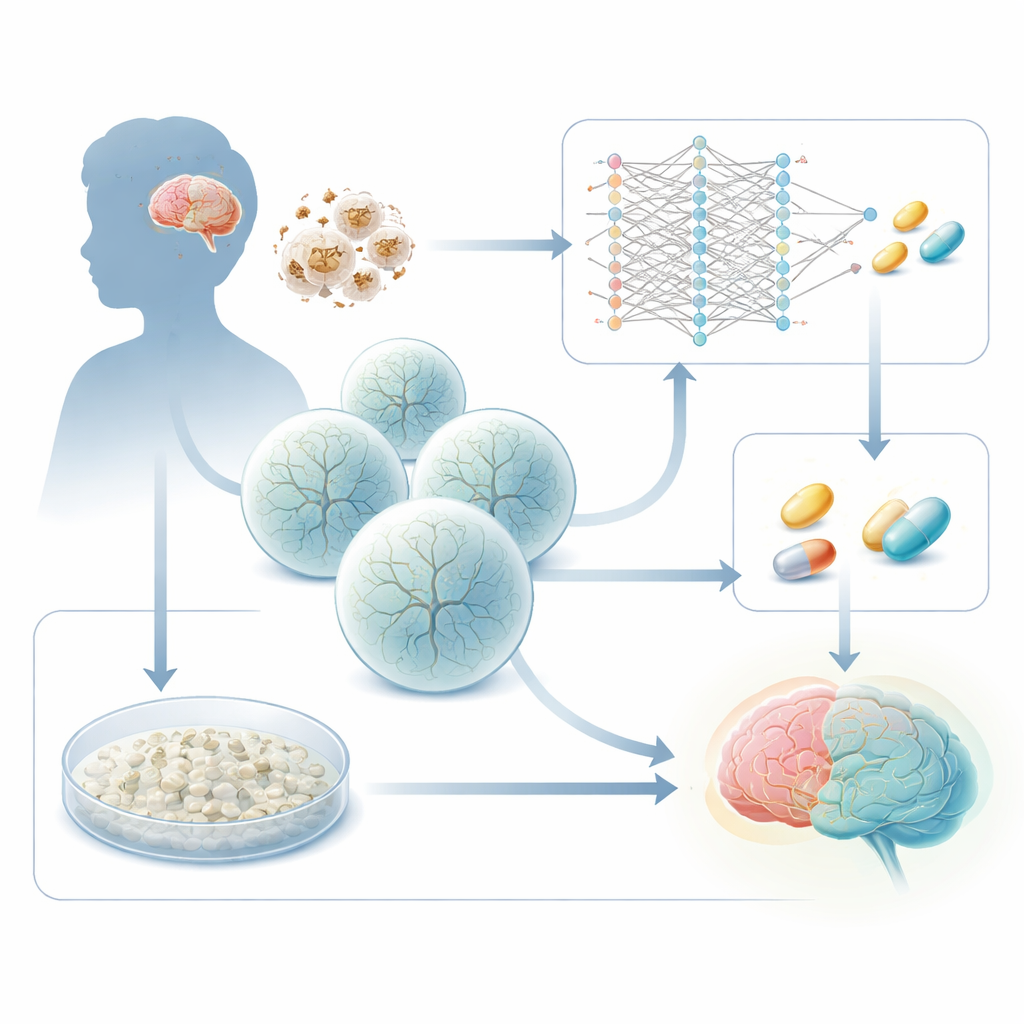
Cómo la falla energética daña el cerebro en desarrollo
El síndrome de Leigh se debe a fallos hereditarios en genes que alimentan las mitocondrias, las “pilas” de la célula. Un culpable común es un gen llamado SURF1, necesario para un paso clave en la maquinaria celular de producción de energía. Cuando SURF1 está defectuoso, las regiones cerebrales que demandan mucha energía—especialmente estructuras profundas del mesencéfalo y los ganglios basales—comienzan a fallar. Trabajos previos de este grupo usaron células madre derivadas de pacientes para cultivar organoides cerebrales tridimensionales y mostraron que los organoides de Leigh forman neuronas de manera deficiente, con ramificación y conexiones anormales. El nuevo estudio plantea una pregunta práctica: ¿pueden aprovecharse estos cambios específicos de la enfermedad como una lectura para encontrar fármacos que empujen a las células enfermas hacia un desarrollo más normal?
Enseñar a las computadoras a sugerir fármacos útiles
Una rama del proyecto utiliza un marco de aprendizaje profundo diseñado específicamente para células no cancerosas. En lugar de limitarse a emparejar firmas génicas de la enfermedad con un catálogo de respuestas a fármacos, el algoritmo aprende cómo cambian las redes de control génico a medida que las células cerebrales jóvenes progresan desde glía radial con características de célula madre, a progenitores intermedios, hasta neuronas maduras. Usando secuenciación de ARN a nivel de célula única de organoides cerebrales de Leigh y sanos, el modelo infiere qué factores de transcripción deben ajustarse para mover las células enfermas a lo largo de la trayectoria de desarrollo normal. A continuación, busca en una gran base de datos de fármacos y predice qué compuestos deberían “dirigir” la red desde un estado tipo Leigh hacia un estado neuronal más sano. De miles de candidatos, reduce la lista a unas pocas decenas de fármacos con efectos prometedores sobre el metabolismo celular.
Dejar que la levadura y los mini‑cerebros voten por los mejores candidatos
En paralelo, el equipo realiza una prueba muy diferente en levadura. La levadura de panadería tiene su propia versión del gen SURF1, y su eliminación hace que las células sean vulnerables cuando los nutrientes escasean—un eco del estrés energético en el síndrome de Leigh. Los investigadores exponen levaduras deficientes en SURF1 a 2.250 fármacos ya aprobados y miden qué químicos rescatan mejor la supervivencia. De manera intrigante, tanto el cribado por inteligencia artificial como la prueba de supervivencia en levadura apuntan a la misma familia química: los azoles, un grupo más conocido por fármacos antifúngicos y de dermatología. De estos, el equipo se centra en dos compuestos, talarozol y sertaconazol, que parecen lo suficientemente seguros para exposiciones prolongadas en modelos celulares humanos y que mejoran de forma marcada la formación temprana de neuronas derivadas de Leigh en placa.
Probar los fármacos en organoides de mesencéfalo humanos
Para acercarse a las regiones cerebrales afectadas en los pacientes, los investigadores generan organoides de mesencéfalo a partir de células progenitoras neuronales derivadas de pacientes. Estas estructuras 3D contienen neuronas productoras de dopamina, células de soporte y circuitos en desarrollo. En comparación con los organoides de células sanas, los organoides de Leigh crecen más pero presentan una estructura neuronal peor, liberan más ácido láctico al medio de cultivo y responden de forma anormal cuando se les somete a estrés energético agudo. Tratar organoides de mesencéfalo de Leigh durante varias semanas con bajas dosis de talarozol o sertaconazol frena su crecimiento excesivo, reduce la liberación de lactato en alrededor de una quinta parte y mejora algunas medidas de función neuronal. Talarozol, en particular, aumenta el número de neuronas de tipo dopaminérgico y restablece una señal de calcio más intensa cuando los organoides son desafiados por una privación súbita de energía, lo que sugiere una recuperación parcial de la capacidad de respuesta de la red.
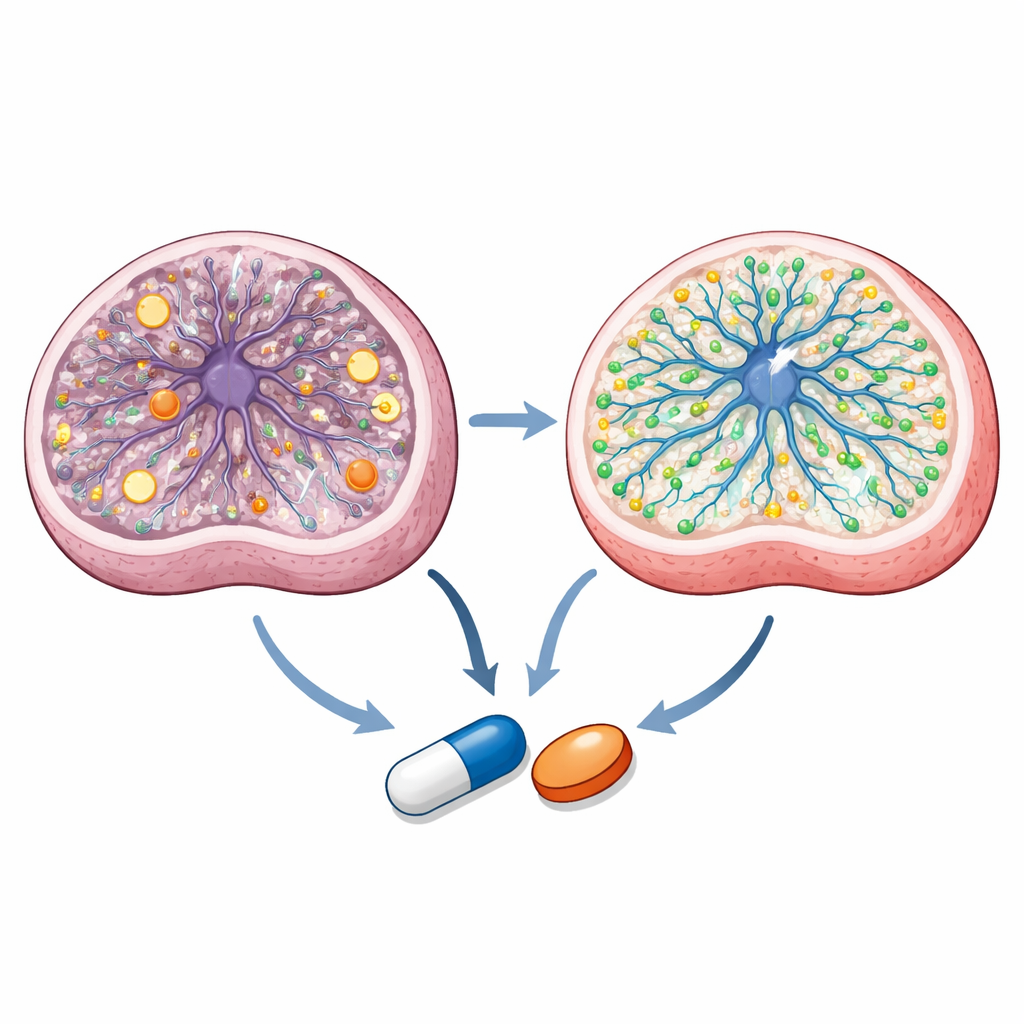
Revelar cómo actúan los compuestos dentro de las células
Indagando más, el equipo encuentra que los dos fármacos azoles actúan por vías superpuestas pero distintas. Mediciones detalladas de metabolitos muestran que las células progenitoras neurales de Leigh presentan un estado energético desequilibrado y una química mitocondrial alterada. Talarozol normaliza ratios energéticos clave y varios intermedios del ciclo metabólico central de la célula, mientras que ambos fármacos corrigen cuellos de botella metabólicos específicos. El perfilado lipídico y la imagenología revelan que sertaconazol tiene un fuerte impacto en las grasas asociadas a membranas y el colesterol, restaurando ciertos esfingolípidos e incrementando el colesterol unido a membrana que está reducido en las células de Leigh. La secuenciación de ARN a célula única de organoides tratados indica que ambos fármacos promueven programas génicos vinculados a la generación de neuronas y al metabolismo lipídico, a la vez que atenúan la expresión mitocondrial sobreactivada. El acoplamiento computacional y ensayos con reporteros en células vivas sugieren además que talarozol interacciona con enzimas que degradan el ácido retinoico—un derivado de la vitamina A crucial para el desarrollo cerebral—y activa un receptor nuclear llamado PPARγ, que se ha implicado como una palanca terapéutica en enfermedades mitocondriales.
Qué podría significar esto para los niños con síndrome de Leigh
Aunque talarozol y sertaconazol no revierten completamente todas las características de la enfermedad en estos modelos, atenúan de manera consistente varios rasgos definitorios del síndrome de Leigh en levadura, neuronas 2D y organoides humanos 3D de mesencéfalo. El trabajo demuestra que combinar aprendizaje profundo con organoides humanos y cribados sencillos en levadura puede señalar rápidamente fármacos reutilizables para un trastorno pediátrico raro que actualmente carece de tratamientos. Para las familias, esto aún no se traduce en una terapia aprobada, pero proporciona dos candidatas concretas y, quizá más importante, una estrategia general: usar la computación avanzada para filtrar enormes bibliotecas de fármacos y luego probar los hallazgos más prometedores en modelos humanos miniaturizados realistas. Este enfoque puede acortar el camino desde la biología básica hasta opciones de tratamiento significativas para el síndrome de Leigh y otras enfermedades del neurodesarrollo con raíz en la disfunción mitocondrial.
Cita: Menacho, C., Okawa, S., Álvarez-Merz, I. et al. Accelerating Leigh syndrome drug discovery through deep learning screening in brain organoids. Nat Commun 17, 3570 (2026). https://doi.org/10.1038/s41467-026-71391-2
Palabras clave: Síndrome de Leigh, organoides cerebrales, aprendizaje profundo, reposicionamiento de fármacos, enfermedad mitocondrial