Clear Sky Science · nl
Versnellen van geneesmiddelenontdekking voor Leigh-syndroom met deep learning-screening in hersenorganoïden
Nieuwe hoop vinden voor een verwoestende hersenziekte bij kinderen
Het Leigh-syndroom is een zeldzame, vaak dodelijke aandoening die zuigelingen en jonge kinderen treft en hun hersenen berooft van de energie die nodig is om te groeien en te functioneren. Voor families zijn er momenteel geen bewezen behandelingen, alleen ondersteunende zorg. Deze studie combineert geavanceerde biologie en kunstmatige intelligentie om bestaande geneesmiddelen te doorzoeken die mogelijk kunnen helpen. Door computergeleide voorspellingen te combineren met klein in het laboratorium gekweekte hersenmodellen identificeren de onderzoekers twee middelen die gedeeltelijk de hersenachtige activiteit in modellen van het Leigh-syndroom herstellen, wat wijst op een snellere weg om therapieën voor zeldzame kinderziekten te vinden.
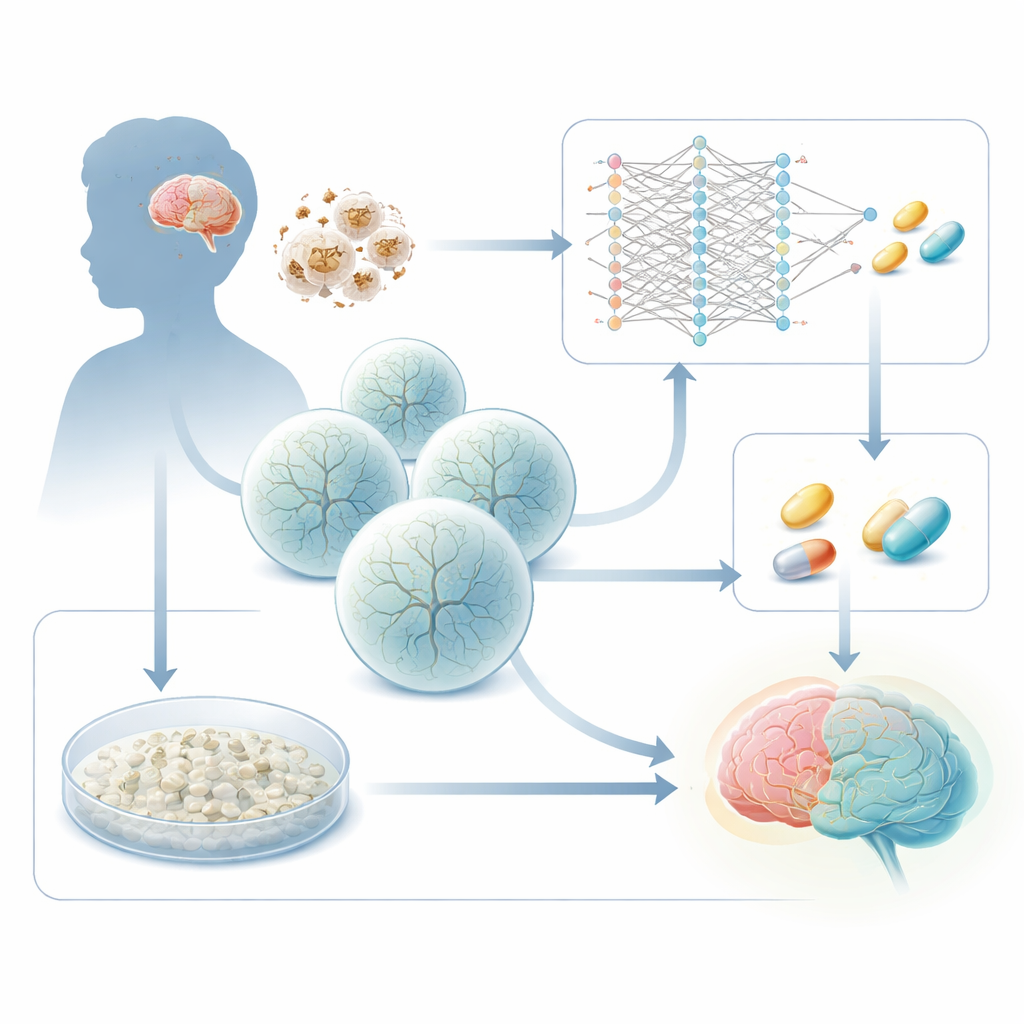
Hoe energietekort het zich ontwikkelende brein schaadt
Het Leigh-syndroom wordt veroorzaakt door erfelijke fouten in genen die de mitochondriën, de “batterijen” van de cel, van energie voorzien. Een veelvoorkomende boosdoener is het gen SURF1, dat nodig is voor een belangrijke stap in de energieproducerende machinerie van de cel. Wanneer SURF1 defect is, falen hersengebieden die veel energie vergen — met name diepe structuren in de middenhersenen en de basale ganglia. Eerder werk van deze groep gebruikte patiëntafgeleide stamcellen om 3D-hersenorganoïden te kweken en toonde aan dat Leigh-organoïden slecht neuronen vormen, met abnormale vertakkingen en bedrading. De nieuwe studie stelt een praktische vraag: kunnen deze ziektespecifieke veranderingen worden gebruikt als meetpunt om geneesmiddelen te vinden die zieke cellen terug naar normale ontwikkeling duwen?
Computers leren nuttige geneesmiddelen aan te bevelen
Een tak van het project gebruikt een deep learning‑kader dat specifiek is ontwikkeld voor niet-kankerachtige cellen. In plaats van alleen ziektegenprofielen simpelweg te matchen met een catalogus van geneesmiddelresponsen, leert het algoritme hoe genregulerende netwerken verschuiven terwijl jonge hersencellen zich ontwikkelen van stamachtige radiale glia, via intermediaire progenitoren, naar rijpe neuronen. Met enkelcel-RNA‑sequencing van Leigh- en gezonde cerebrale organoïden leidt het model af welke transcriptiefactoren moeten worden bijgestuurd om zieke cellen langs het normale ontwikkelingspad te bewegen. Vervolgens zoekt het in een grote database van geneesmiddelen en voorspelt welke verbindingen het netwerk van een Leigh‑achtig naar een gezonder neuronale toestand zouden moeten “sturen”. Uit duizenden kandidaten beperkt het de lijst tot enkele tientallen geneesmiddelen met veelbelovende effecten op cellulaire energiehuishouding.
Gist en mini‑hersenen laten stemmen over de beste kandidaten
Parallel voert het team een heel ander screen uit in gist. Bakkersgist heeft een eigen versie van het SURF1-gen, en het verwijderen daarvan maakt de cellen kwetsbaar wanneer voedingsstoffen schaars zijn — een echo van de energiestress bij het Leigh-syndroom. De onderzoekers stellen SURF1‑deficiënte gist bloot aan 2.250 reeds goedgekeurde geneesmiddelen en meten welke stoffen het beste het overleven herstellen. Intrigerend wijzen zowel het AI‑screen als de gist‑overlevingstest naar dezelfde chemische familie: azolen, een groep die vaker bekend staat als antischimmel- en dermatologische middelen. Hieruit richt het team zich op twee verbindingen, talarozole en sertaconazol, die in humane celmodellen veilig genoeg lijken voor langdurige blootstelling en die vroege neuronvorming in in vitro‑Leigh‑afgeleide neuronen sterk verbeteren.
De geneesmiddelen testen in humane middenhersenenorganoïden
Om dichter bij de aangedane hersengebieden van patiënten te komen, genereren de onderzoekers middenhersenenorganoïden uit patiëntafgeleide neurale progenitorcellen. Deze 3D-structuren bevatten dopamineproducerende neuronen, ondersteunende cellen en zich ontwikkelende circuits. Vergeleken met organoïden uit gezonde cellen groeien Leigh-organoïden groter maar hebben ze een slechtere neurale structuur, geven ze meer melkzuur af aan het kweekmedium en reageren ze abnormaal bij acute energiestress. Behandeling van Leigh-middenhersenenorganoïden gedurende enkele weken met lage doses talarozole of sertaconazol remt hun overmatige groei, vermindert de lactaatafgifte met ongeveer een vijfde en verbetert enkele maten van neuronale functie. Vooral talarozole verhoogt het aantal dopamine‑achtige neuronen en herstelt een sterkere calciumsignaalrespons wanneer de organoïden worden blootgesteld aan plotselinge energieontbering, wat wijst op een gedeeltelijk herstel van netwerkresponsiviteit.
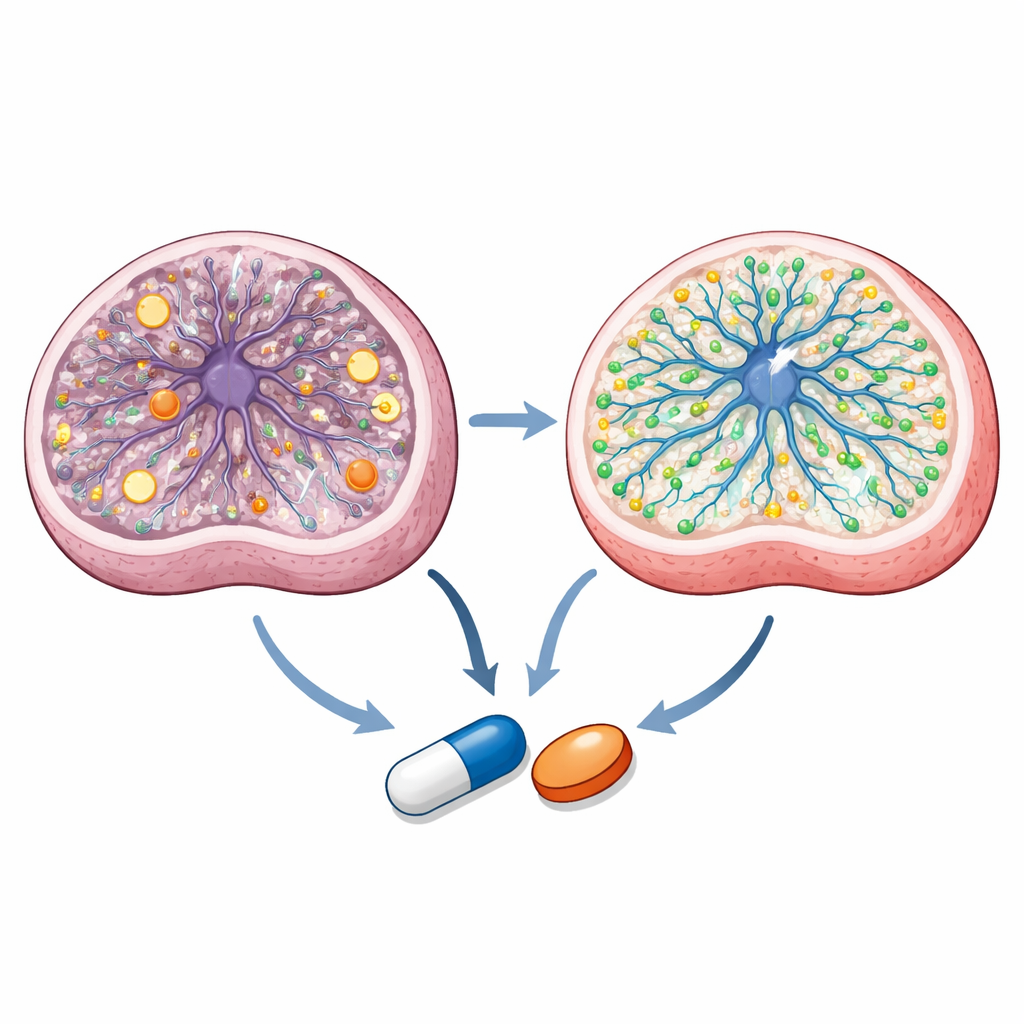
Ontdekken hoe de verbindingen in cellen werken
Dieper graven laat zien dat de twee azoolgeneesmiddelen via overlappende maar onderscheiden routes werken. Gedetailleerde metingen van metabolieten tonen aan dat Leigh‑neurale progenitorcellen een verstoorde energiebalans en ontregelde mitochondriale chemie hebben. Talarozole normaliseert belangrijke energieratio’s en verschillende tussenproducten in de centrale stofwisselingscyclus van de cel, terwijl beide middelen specifieke metabole knelpunten corrigeren. Lipidenprofielen en beeldvorming onthullen dat sertaconazol een sterke invloed heeft op membraangebonden vetten en cholesterol, waarbij bepaalde sphingolipiden worden hersteld en het membraangebonden cholesterol wordt verhoogd dat in Leigh-cellen verminderd is. Enkelcel-RNA‑sequencing van behandelde organoïden geeft aan dat beide middelen genprogramma’s stimuleren die gekoppeld zijn aan neuronvorming en lipidenmetabolisme, terwijl overactieve mitochondriale genexpressie wordt geremd. Computationele docking en levende‑cel reporterassays suggereren verder dat talarozole enzymen beïnvloedt die retinoïnezuur afbreken — een vitamine A‑afgeleide cruciaal voor hersenontwikkeling — en een nucleair receptor genaamd PPARγ activeert, die als therapeutisch aangrijpingspunt bij mitochondriale ziekten is voorgesteld.
Wat dit zou kunnen betekenen voor kinderen met Leigh‑syndroom
Hoewel talarozole en sertaconazol niet alle ziektekenmerken in deze modellen volledig omkeren, verzachten ze consequent meerdere kenmerken van het Leigh‑syndroom in gist, 2D‑neuronen en 3D‑humane middenhersenenorganoïden. Het werk laat zien dat het combineren van deep learning met humane organoïden en eenvoudige gist‑screens snel herbruikbare geneesmiddelen kan identificeren voor een zeldzame pediatrische aandoening waarvoor momenteel geen behandelingen bestaan. Voor families vertaalt dit zich nog niet naar een goedgekeurde therapie, maar het levert twee concrete geneesmiddelkandidaten en, misschien nog belangrijker, een algemene strategie: gebruik geavanceerde computationele methoden om enorme geneesmiddelenbibliotheken te filteren en test vervolgens de meest veelbelovende kandidaten in realistische menselijke mini‑hersmodellen. Deze aanpak kan de weg van fundamentele biologie naar zinvolle behandelopties voor het Leigh‑syndroom en andere neuroontwikkelingsziekten met mitochondriale disfunctie verkorten.
Bronvermelding: Menacho, C., Okawa, S., Álvarez-Merz, I. et al. Accelerating Leigh syndrome drug discovery through deep learning screening in brain organoids. Nat Commun 17, 3570 (2026). https://doi.org/10.1038/s41467-026-71391-2
Trefwoorden: Leigh-syndroom, hersenorganoïden, deep learning, herbestemming van geneesmiddelen, mitochondriale ziekte