Clear Sky Science · sv
Accelerera läkemedelsupptäckt för Leigh‑syndrom genom djupinlärningsscreening i hjärnorganoider
Ny hopp för en förödande barndomsjukdom i hjärnan
Leigh‑syndrom är en sällsynt, ofta dödlig sjukdom som drabbar spädbarn och små barn och berövar deras hjärnor den energi som krävs för att växa och fungera. Familjer har i dagsläget inga bevisat effektiva behandlingar, endast stödjande vård. Denna studie förenar spetsbiologi och artificiell intelligens för att leta efter redan godkända läkemedel som kan vara till nytta. Genom att kombinera datorstyrda prediktioner med små laboratorieodlade hjärnmodeller identifierar forskarna två läkemedel som delvis återställer hjärnlik aktivitet i modeller av Leigh‑syndrom, vilket pekar mot en snabbare väg att hitta terapier för sällsynta barndomssjukdomar.
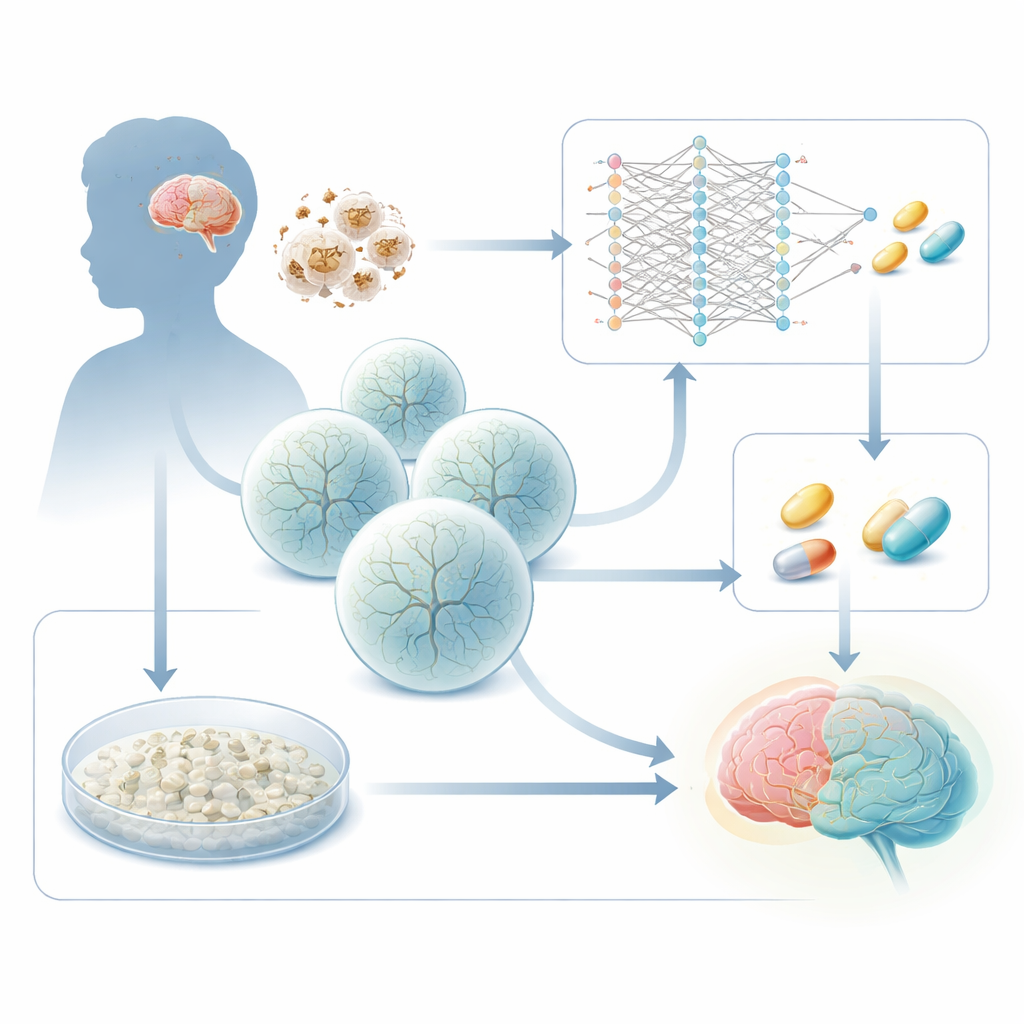
Hur energibrist skadar den utvecklande hjärnan
Leigh‑syndrom orsakas av ärftliga fel i gener som driver mitokondrierna, cellens ”batterier”. En vanlig förövare är en gen kallad SURF1, som behövs för ett viktigt steg i cellens energiproducerande maskineri. När SURF1 är defekt börjar hjärnregioner med stort energibehov — särskilt djupa strukturer i mitthjärnan och basala ganglierna — att svikta. Tidigare arbete från denna grupp använde patient‑härledda stamceller för att odla tredimensionella hjärnorganoider och visade att Leigh‑organoider bildar neuroner dåligt, med onormal förgrening och koppling. Den nya studien ställer en praktisk fråga: kan dessa sjukdomsspecifika förändringar utnyttjas som ett avläsningsmått för att hitta läkemedel som driver sjuka celler tillbaka mot normal utveckling?
Lära datorer att föreslå hjälpsamma läkemedel
En gren av projektet använder ett djupinlärningsramverk byggt specifikt för icke‑cancerceller. Istället för att enbart matcha sjukdomsgensignaturer mot en katalog av läkemedelsresponser lär sig algoritmen hur genregleringsnätverk förändras när unga hjärnceller utvecklas från stamliknande radiell glia, via intermediära progenitorer, till mogna neuroner. Med hjälp av enkelcells‑RNA‑sekvensering från Leigh‑ och friska cerebrala organoider härleder modellen vilka transkriptionsfaktorer som måste skjutas i rätt riktning för att få de sjuka cellerna att följa den normala utvecklingsvägen. Den söker sedan i en stor databas av läkemedel och predicerar vilka föreningar som bör ”styra” nätverket från ett Leigh‑liknande tillstånd mot ett friskare neuronalt tillstånd. Av tusentals kandidater kortar den ner listan till ett par dussin läkemedel med lovande effekter på cellernas metabolism.
Låta jäst och mini‑hjärnor rösta om de bästa kandidaterna
Parallellt kör teamet en mycket annorlunda screening i jäst. Bagarjäst har en egen version av SURF1‑genen, och att ta bort den gör cellerna sårbara när näringsämnen är knappa — en ekon av energistressen i Leigh‑syndrom. Forskarna utsätter SURF1‑defekt jäst för 2 250 redan godkända läkemedel och mäter vilka kemikalier som bäst räddar överlevnaden. Intressant nog pekar både AI‑screeningen och jästtestet mot samma kemiska familj: azoler, en grupp som är bättre känd som antifungala medel och läkemedel för dermatologi. Av dessa fokuserar teamet på två föreningar, talarözol och sertakonazol, som verkar tillräckligt säkra för långvarig exponering i humana cellmodeller och som starkt förbättrar tidig neuronbildning i Leigh‑härledda neuroner i odlingsskålar.
Testa läkemedlen i humana mitthjärneorganoider
För att komma närmare de hjärnområden som är påverkade hos patienter genererar forskarna mitthjärneorganoider från patient‑härledda neurala progenitorceller. Dessa tredimensionella strukturer innehåller dopaminproducerande neuroner, stödjeceller och utvecklande nätverk. Jämfört med organoider från friska celler växer Leigh‑organoiderna större men har sämre neuronal struktur, släpper ut mer mjölksyra i odlingsmediet och svarar onormalt vid akut energistress. Behandling av Leigh‑mitthjärneorganoider under flera veckor med låga doser talarözol eller sertakonazol bromsar deras överdrivna tillväxt, minskar laktatutsläppet med omkring en femtedel och förbättrar vissa mått på neuronal funktion. Talarözol ökar i synnerhet antalet dopaminliknande neuroner och återställer en starkare kalciumsignal när organoiderna utsätts för plötslig energibrist, vilket tyder på en delvis återhämtning av nätverksresponsivitet.
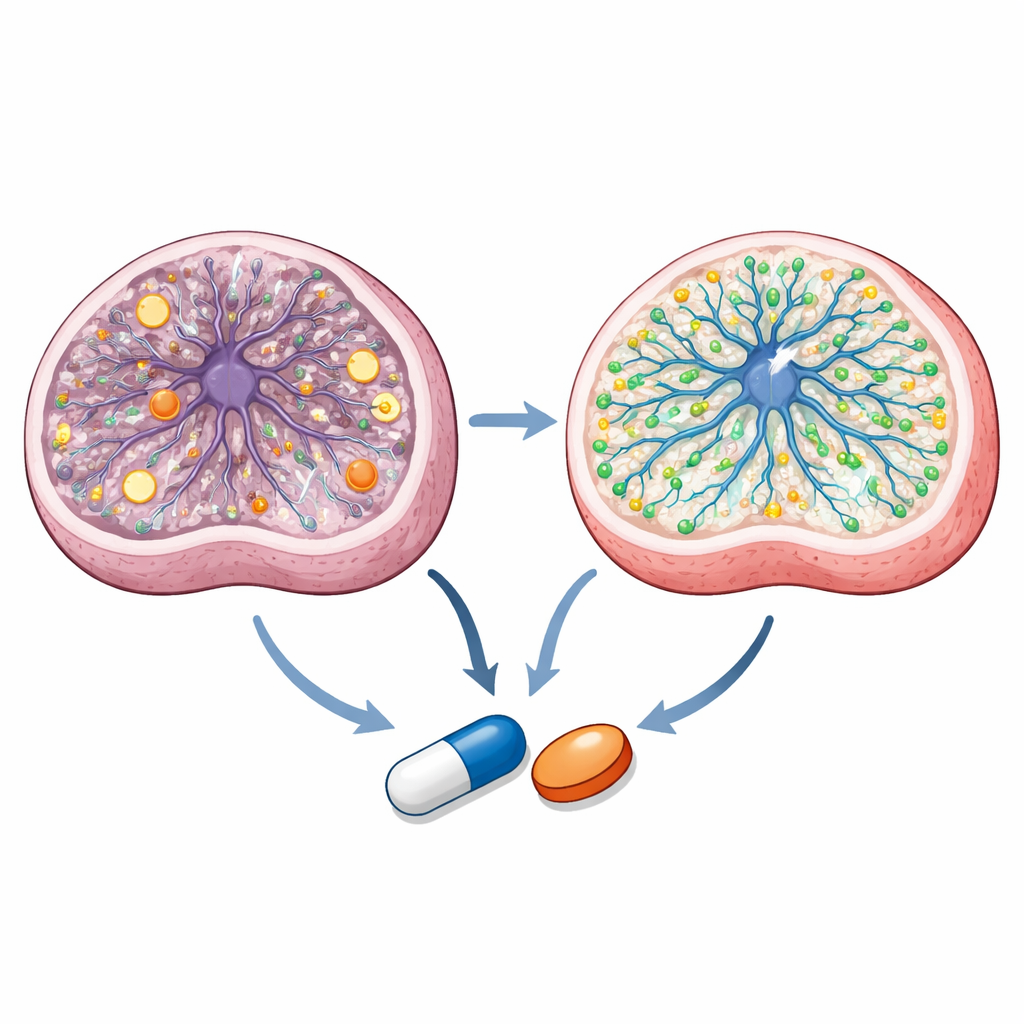
Avslöja hur föreningarna verkar inne i cellerna
Vid djupare analys finner teamet att de två azol‑läkemedlen verkar genom överlappande men distinkta mekanismer. Detaljerade mätningar av metaboliter visar att Leighs neurala progenitorceller har en obalanserad energistatus och störd mitokondrie‑kemi. Talarözol normaliserar viktiga energiförhållanden och flera intermediärer i cellens centrala metaboliska cykel, medan båda läkemedlen korrigerar specifika metaboliska flaskhalsar. Lipidprofilering och avbildning visar att sertakonazol har en stark påverkan på membranassocierade fetter och kolesterol, återställer vissa sfingolipider och ökar membranbundet kolesterol som är minskat i Leigh‑celler. Enkelcells‑RNA‑sekvensering av behandlade organoider indikerar att båda läkemedlen främjar genprogram kopplade till neuronbildning och lipidmetabolism samtidigt som överaktiv mitokondriegenuttryck nedregleras. Datormodellering av bindning och live‑cell‑reporterassayer antyder vidare att talarözol engagerar enzymer som bryter ner retinoinsyra — en A‑vitaminderivat viktig för hjärnans utveckling — och aktiverar en nukleär receptor kallad PPARγ, som har föreslagits som ett terapeutiskt spak i mitokondriesjukdomar.
Vad detta kan innebära för barn med Leigh‑syndrom
Även om talarözol och sertakonazol inte fullständigt vänder alla sjukdomsdrag i dessa modeller, mildrar de konsekvent flera kännetecken för Leigh‑syndrom över jäst, 2D‑neuroner och 3D‑humana mitthjärneorganoider. Arbetet visar att kombinationen av djupinlärning med humana organoider och enkla jäst‑tester snabbt kan rikta in sig på läkemedel som kan återanvändas för en sällsynt pediatrisk sjukdom som för närvarande saknar behandlingar. För familjer översätts detta ännu inte till en godkänd terapi, men det ger två konkreta läkemedelskandidater och, kanske viktigare, en generell strategi: använd avancerad beräkning för att filtrera enorma läkemedelsbibliotek, och testa sedan de mest lovande träffarna i realistiska humana mini‑hjärnmodeller. Detta angreppssätt kan förkorta vägen från grundläggande biologi till meningsfulla behandlingsalternativ för Leigh‑syndrom och andra neuroutvecklingssjukdomar med ursprung i mitokondriell dysfunktion.
Citering: Menacho, C., Okawa, S., Álvarez-Merz, I. et al. Accelerating Leigh syndrome drug discovery through deep learning screening in brain organoids. Nat Commun 17, 3570 (2026). https://doi.org/10.1038/s41467-026-71391-2
Nyckelord: Leigh‑syndrom, hjärnorganoider, djupinlärning, läkemedelsåteranvändning, mitokondriesjukdom