Clear Sky Science · he
האצת גילוי תרופות לתסמונת ליי באמצעות סינון בלמידה עמוקה באורגנואידים מוחיים
מוצאים תקווה חדשה למחלת מוח הרסנית של ילדות
תסמונת ליי היא מחלה נדירה ולעתים קטלנית שפוגעת בתינוקות וילדים קטנים, וגוזלת ממוחותיהם את האנרגיה הדרושה לגדילה ולתפקוד. למשפחות כיום אין טיפולים מוכחים, רק טיפול תומך. המחקר הזה מאחד ביולוגיה מתקדמת ובינה מלאכותית כדי לחפש תרופות קיימות שעשויות לסייע. על ידי שילוב חיזוי מונחה מחשב עם דגמי מעבדה זעירים של מוח, החוקרים זיהו שתי תרופות שמשקמות חלקית פעילות דמויה־מוח באורגנואידים של תסמונת ליי, ומצביעים על דרך מהירה יותר לגלות טיפולים למחלות ילדות נדירות.
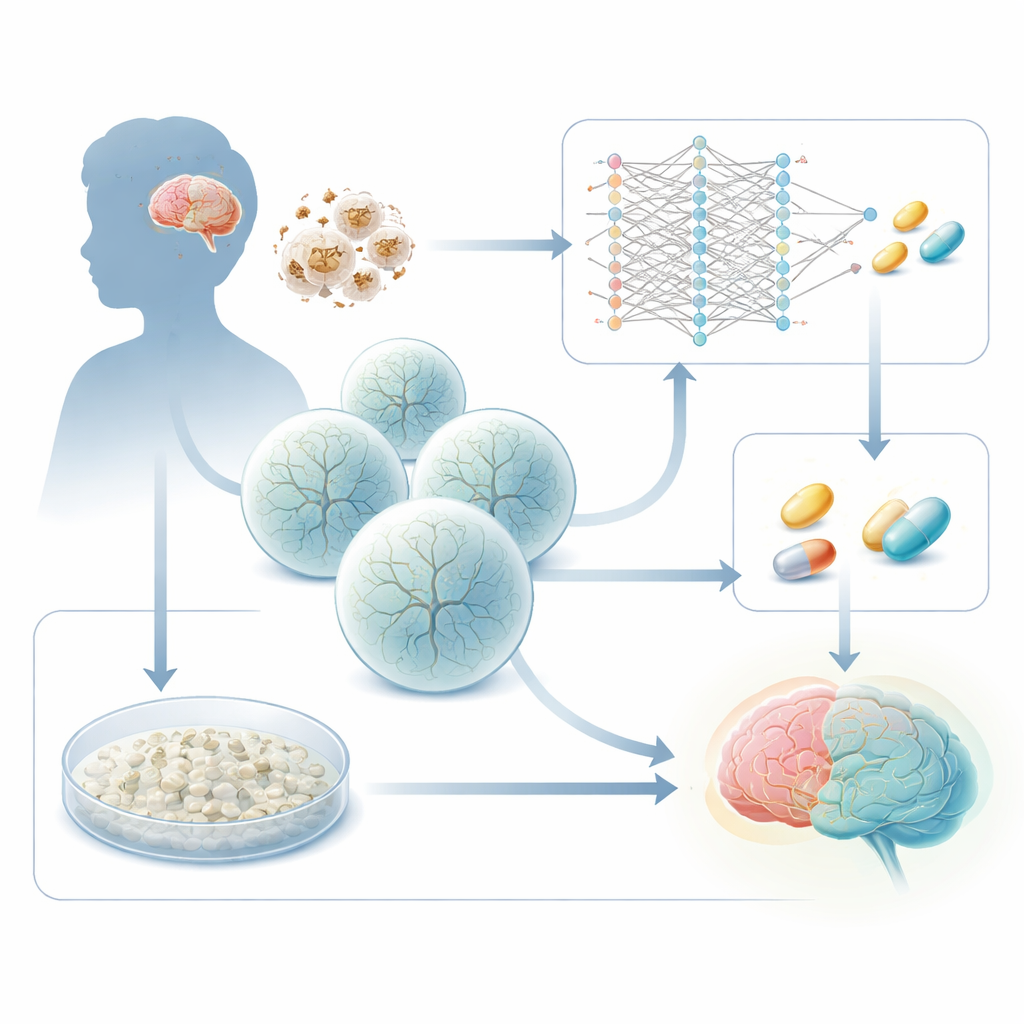
כיצד כישלון אספקת אנרגיה פוגע במוח המתפתח
תסמונת ליי נגרמת על ידי ליקויים תורשתיים בגנים שמספקים אנרגיה למיטוכונדריות, "הסוללות" של התא. גורם שכיח הוא הגן SURF1, הנדרש לשלב מפתח במכונה התאית שמייצרת אנרגיה. כאשר SURF1 פגום, אזורים מוחיים בעלי דרישה אנרגטית גבוהה—במיוחד מבנים עמוקים בגזע המוח ובגרעינים הבזאליים—מתחילים להיכשל. עבודות קודמות של הקבוצה השתמשו בתאי גזע שמקורם בחולים כדי לגדל אורגנואידים מוחיים תלת‑ממדיים והראו שאורגנואידים של ליי יוצרים נוירונים בצורה לקויה, עם הסתעפות וחיבורים חריגים. המחקר החדש שואל שאלה מעשית: האם ניתן לנצל את השינויים הספציפיים למחלה כאות־קריאה כדי למצוא תרופות שמדחפות תאים חולים חזרה להתפתחות נורמלית?
לימוד מחשבים להציע תרופות מועילות
זרוע אחת של הפרויקט משתמשת במסגרת למידה עמוקה שנבנתה במיוחד לתאים שאינם סרטניים. במקום רק להשוות חתימות גנים של המחלה למאגר תגובות לתרופות, האלגוריתם לומד כיצד רשתות בקרה גנטיות משתנות כאשר תאי מוח צעירים מתקדמים מתאי גליה רדיאליים דמויי־גזע, דרך תאי‑ביניים יוצרי‑עצב, ועד לנוירונים בוגרים. באמצעות ריצוף RNA בתא‑יחיד מאורגנואידים של ליי ובריאים, המודל מסיק אילו גורמי שעתוק יש לדחוף כדי להזיז תאים חולים במסלול ההתפתחות הנורמלי. הוא מחפש מאגר גדול של תרופות ומנבא אילו תרכובות אמורות "להטות" את הרשת ממצב הדומה לליי לעבר מצב נוירונלי בריא יותר. מתוך אלפי מועמדים הוא ממצה את הרשימה לכמה עשרות תרופות עם השפעות מבטיחות על מטבוליזם תאי.
לתת לשמרים ולמיני‑מוחות להצביע על המועמדים הטובים ביותר
במקביל, הצוות מריץ סקר שונה לחלוטין בשמרים. לשמרת האפייה יש גרסה של גן SURF1, והסרתו הופכת את התאים לפגיעים כאשר המזון נדיר—הד שמעורר את הלחץ האנרגטי בתסמונת ליי. החוקרים חושפים שמרים חסרי SURF1 ל‑2,250 תרופות שאושרו כבר ומודדים אילו כימיקלים מצילים בצורה הטובה ביותר את ההישרדות. באופן מעניין, גם סקר הבינה המלאכותית וגם מבחן הישרדות השמרים מצביעים על אותה משפחה כימית: האזולים, קבוצה הידועה יותר כתרופות אנטי‑פטרייתיות ולשימוש רופאי עור. מתוך אלה, הצוות מתמקד בשתי תרכובות, טלרוזול וסרטקונאזול, שנראות בטוחות יחסית לחשיפה ארוכת‑טווח במודלי תאים אנושיים ומשפרות באופן משמעותי היווצרות נוירונים מוקדמת בתאים שמקורם בליי בתרבית.
בדיקת התרופות באורגנואידים של גזע־המוח האנושי
כדי להתקרב לאזורים מוחיים הנפגעים בחולים, החוקרים מייצרים אורגנואידים של גזע־המוח מתאים‑מוצא נוירליים שמקורם בחולים. מבנים תלת‑ממדיים אלה מכילים נוירונים המייצרים דופמין, תאי תמיכה ומעגלים מתפתחים. בהשוואה לאורגנואידים מתאים בריאים, אורגנואידים של ליי גדלים יותר אך בעלי מבנה נוירונלי לקוי, משחררים יותר חומצת חלב לתווך הגידול ומגיבים באופן חריג כאשר מושמדים ללחץ אנרגטי חמור. טיפול של מספר שבועות במינונים נמוכים של טלרוזול או סרטקונאזול מאט את הגידול המופרז של אורגנואידים ליי, מצמצם את שחרור החומצה החלבית בכ‑כ־חמישית ומשפר כמה מדדי תפקוד נוירונלי. טלרוזול, בפרט, מעלה את מספר הנוירונים הדמויי‑דופמין ומשקמת אות סידן חזק יותר כאשר האורגנואידים מאוימים במחסור אנרגיה פתאומי, מה שמרמז על התאוששות חלקית של תגובתיות הרשת.
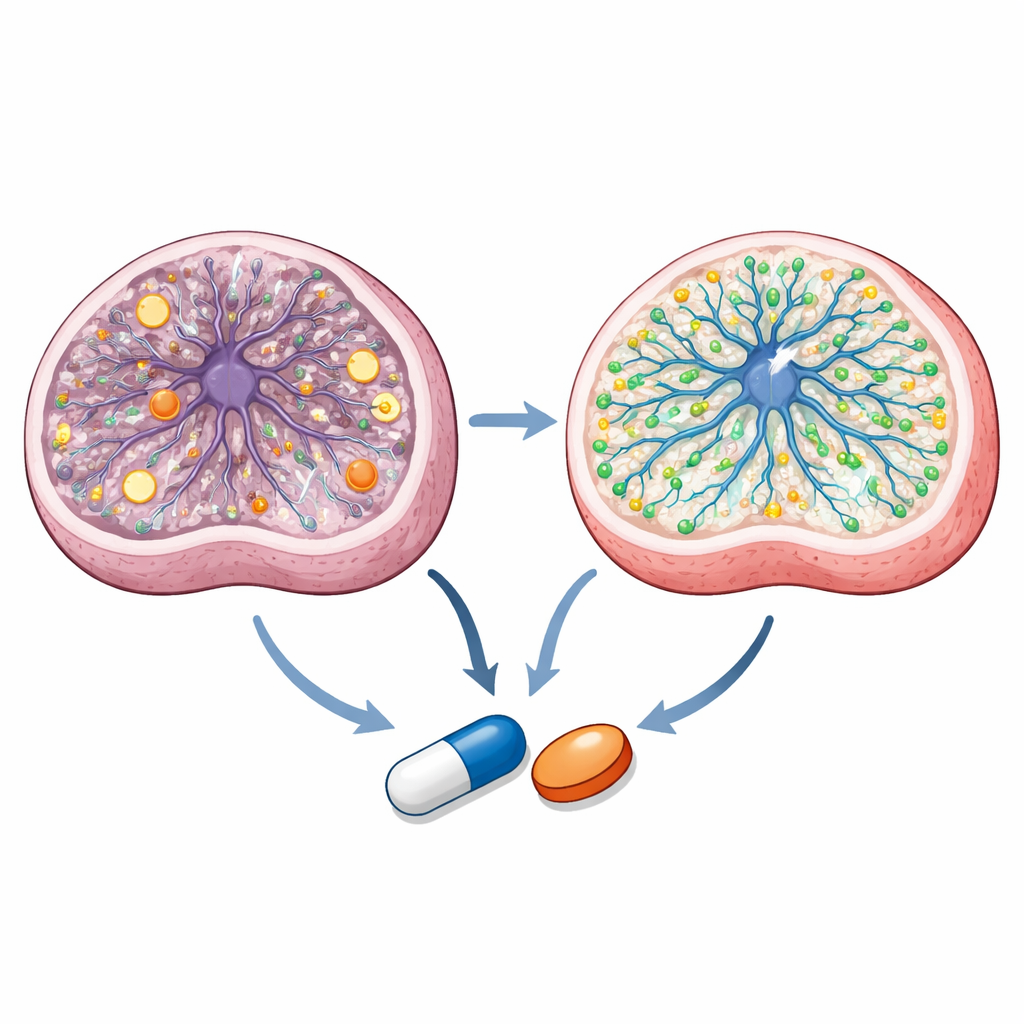
גילוי מנגנוני הפעולה בתוך התאים
בחינה מעמיקה מגלה ששתי תרופות האזול פועלות דרך מסלולים חופפים אך נבדלים. מדידות מטבוליטים מפורטות מראות שתאי‑האב הנוירליים של ליי מציגים מצב אנרגיה לא מאוזן וכימיה מיטוכונדריאלית מופרעת. טלרוזול מנרמל יחסי אנרגיה מרכזיים וכמה מתווכים במחזור המטבולי המרכזי של התא, בעוד ששתי התרופות מתקןות צווארי בקבוק מטבוליים ספציפיים. פרופיל שומנים והדמיה חושפים שסרטקונאזול משפיע חזק על שומנים הקשורים לממברנה ולכולסטרול, משחזר ספינגוליפידים מסוימים ומעלה את הכולסטרול הקשור לממברנה שמופחת בתאי ליי. ריצוף RNA בתא‑יחיד של אורגנואידים מטופלים מצביע על כך ששתי התרופות מקדמות תכניות גנטיות הקשורות ליצירת נוירונים ולמטבוליזם שומנים ומורידות ביטוי יתר של גנים מיטוכונדריאליים. דוקינג חישובי ובדיקות מדווחות בחיות תאים מרמזות שטלרוזול קשור לאנזימים שמפרקים חומצה רטינואית—נגזרת של ויטמין A החשובה בהתפתחות המוח—ומפעיל קולטן גרעיני בשם PPARγ, שהועלה כיעד טיפולי במחלות מיטוכונדריאליות.
מה יכול הדבר לייצג עבור ילדים עם תסמונת ליי
למרות שטלרוזול וסרטקונאזול אינם מבטלים לחלוטין את כל מאפייני המחלה במודלים אלה, הן מרככות בעקביות מספר סימני מפתח של תסמונת ליי בשמרים, נוירונים דו‑מימדיים ואורגנואידים תלת‑ממדיים של גזע־המוח האנושי. העבודה מראה ששילוב למידה עמוקה עם אורגנואידים אנושיים וסקרי שמרים פשוטים יכול במהירות להתמקד בתרופות שניתן להשתמש בהן מחדש למחלה פאראדיגמתית בילדים שאין לה כיום טיפולים. למשפחות, המשמעות שלבינתיים איננה המרה לטיפול מאושר, אך היא מספקת שני מועמדי תרופות קונקרטיים—and, perhaps more importantly, אסטרטגיה כללית: להשתמש בחישוב מתקדם לסינון מאגרים עצומים של תרופות, ואז לבדוק את הממצאים המבטיחים ביותר במודלי מיני‑מוח אנושיים ריאליסטיים. גישה זו עשויה לקצר את הדרך מביולוגיה בסיסית לאפשרויות טיפול משמעותיות לתסמונת ליי ולמחלות נוירו‑התפתחותיות נוספות הנובעות מפגיעה במיטוכונדריה.
ציטוט: Menacho, C., Okawa, S., Álvarez-Merz, I. et al. Accelerating Leigh syndrome drug discovery through deep learning screening in brain organoids. Nat Commun 17, 3570 (2026). https://doi.org/10.1038/s41467-026-71391-2
מילות מפתח: תסמונת ליי, אורגנואידים מוחיים, למידה עמוקה, שימוש חוזר בתרופות, מחלות מיטוכונדריאליות