Clear Sky Science · tr
Leigh sendromu için ilaç keşfini beyin organoidlerinde derin öğrenme ile hızlandırmak
Yıkıcı Bir Çocukluk Beyin Hastalığı İçin Yeni Umutlar Bulmak
Leigh sendromu, bebekleri ve küçük çocukları hedef alan nadir ve sıklıkla ölümcül bir bozukluktur; beyinlerinin büyümek ve işlev görmek için ihtiyaç duyduğu enerjiyi çalar. Ailelerin şu anda kanıtlanmış bir tedavisi yoktur, yalnızca destekleyici bakım sağlanmaktadır. Bu çalışma, mevcut ilaçları araştırmak için son teknoloji biyoloji ve yapay zekayı bir araya getiriyor. Bilgisayar destekli tahminleri laboratuvarda üretilen küçük beyin modelleriyle birleştirerek, araştırmacılar Leigh sendromu modellerinde beyin benzeri aktiviteyi kısmen geri kazandıran iki ilacı belirliyor ve nadir çocukluk hastalıkları için daha hızlı tedavi keşfine işaret ediyor.
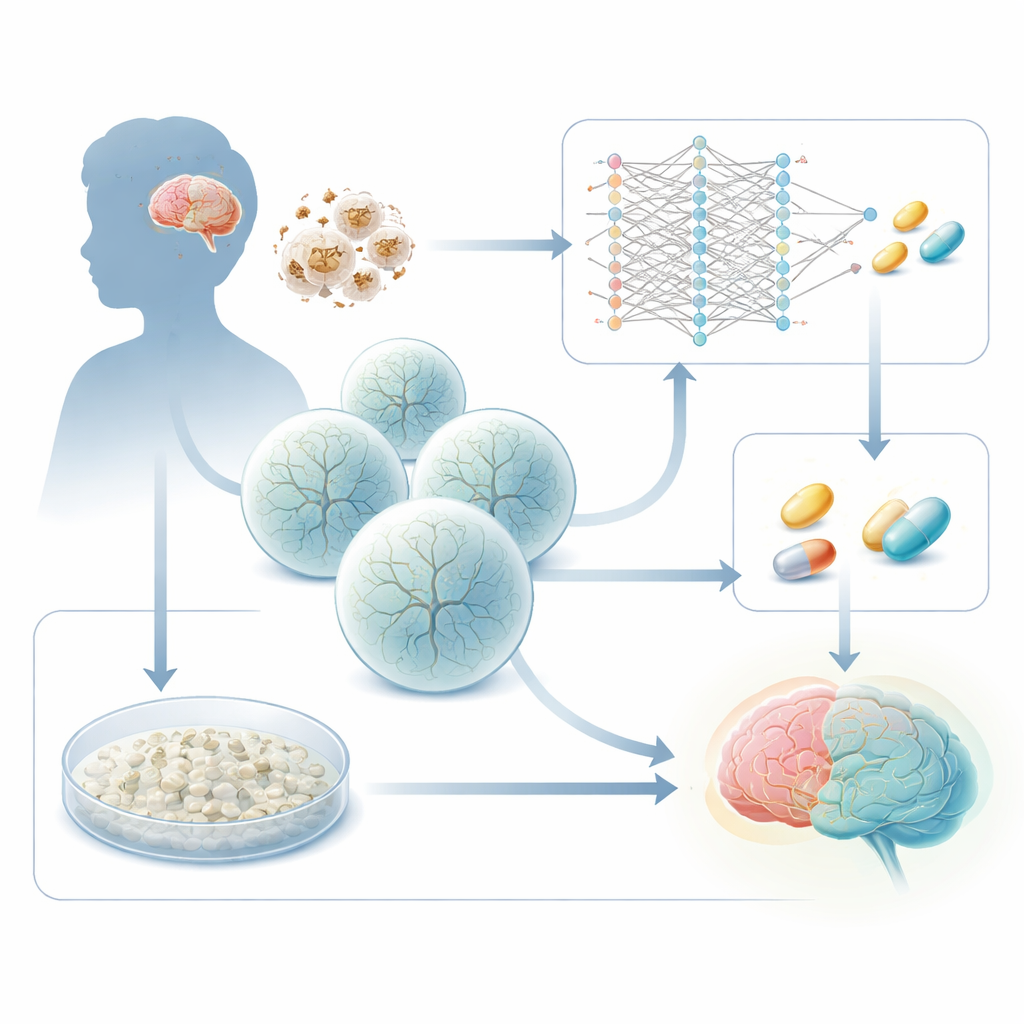
Enerji Yetmezliğinin Gelişen Beyne Zarar Vermesi
Leigh sendromu, mitokondrileri — hücrenin “pilleri”ni — çalıştıran genlerde kalıtsal kusurlardan kaynaklanır. Yaygın suçlulardan biri, hücrenin enerji üreten mekanizmasında kritik bir adıma ihtiyaç duyan SURF1 adlı gendir. SURF1 kusurlu olduğunda, özellikle orta beyin ve bazal gangliyonlardaki yüksek enerji talep eden beyin bölgeleri başarısız olmaya başlar. Bu gruptan önceki çalışmalar, hastadan türetilmiş kök hücreleri kullanarak 3B beyin organoidleri üretmiş ve Leigh organoidlerinin nöron oluşturmakta zayıf olduğunu, anormal dallanma ve bağlantı gösterdiğini ortaya koymuştur. Yeni çalışma ise pratik bir soru soruyor: bu hastalığa özgü değişiklikler, hasta hücreleri normal gelişime doğru iten ilaçları bulmak için bir ölçüt (read‑out) olarak kullanılabilir mi?
Bilgisayarları Yararlı İlaçlar Önermeye Öğretmek
Projenin bir kolu, kanser dışı hücreler için özel olarak geliştirilmiş bir derin öğrenme çerçevesi kullanıyor. Hastalık gen imzalarını doğrudan ilaç yanıtları kataloğuna eşleştirmek yerine, algoritma genç beyin hücreleri kök‑benzeri radyal glia’dan ara progenitörlere, oradan olgun nöronlara ilerlerken gen denetim ağlarının nasıl kaydığına dair öğrenme gerçekleştiriyor. Leigh ve sağlıklı serebral organoidlerden elde edilen tek hücre RNA sekanslama verilerini kullanarak model, hastalıklı hücreleri normal gelişim yoluna taşımak için hangi transkripsiyon faktörlerinin uyarılması gerektiğini çıkarıyor. Ardından büyük bir ilaç veritabanında arama yapıp hangi bileşiklerin ağı Leigh‑benzeri durumdan daha sağlıklı bir nöronal duruma “yönlendirmesi” gerektiğini tahmin ediyor. Binlerce aday arasından, hücresel metabolizma üzerinde umut verici etkileri olan birkaç düzine ilaca daraltıyor.
Maya ve Mini Beyinlerin En İyi Adaylara Oy Vermesi
Eşzamanlı olarak ekip, mayada çok farklı bir tarama yürütüyor. Ekmeğe kullanılan maya (Saccharomyces cerevisiae) kendi SURF1 benzerine sahiptir ve bu gen silindiğinde hücreler besin kıtlığı altında savunmasız hale gelir — Leigh sendromundaki enerji stresinin bir yansıması. Araştırmacılar SURF1 eksik mayaları 2.250 onaylı ilaca maruz bırakıp hangi kimyasalların hayatta kalmayı en iyi şekilde kurtardığını ölçüyor. İlginç biçimde, yapay zekâ taraması ve maya hayatta kalma testi aynı kimyasal aileye işaret ediyor: antimikotik ve dermatoloji ilaçları olarak daha çok bilinen azoller grubu. Bunlardan ekip, insan hücre modellerinde uzun süreli maruziyet için yeterince güvenli görünen ve kültürde Leigh türevi nöronlarda erken nöron oluşumunu güçlü şekilde iyileştiren talarozol ve sertakonazol olmak üzere iki bileşiğe odaklanıyor.
İlaçları İnsan Orta Beyin Organoidlerinde Test Etmek
Hastaların etkilenen beyin bölgelerine daha yakın olmak için araştırmacılar hasta kökenli nöral progenitör hücrelerden orta beyin organoidleri üretiyor. Bu 3B yapılar dopamin üreten nöronlar, destek hücreleri ve gelişmekte olan devreleri içeriyor. Sağlıklı hücrelerden üretilen organoidlerle karşılaştırıldığında, Leigh organoidleri daha büyük büyüme gösteriyor fakat nöronal yapı bakımından daha zayıf, kültür ortamına daha fazla laktik asit salgılıyor ve akut enerji stresine maruz kaldıklarında anormal yanıt veriyor. Leigh orta beyin organoidlerini birkaç hafta düşük doz talarozol veya sertakonazol ile tedavi etmek, aşırı büyümelerini yavaşlatıyor, laktat salınımını yaklaşık beşte bir azaltıyor ve bazı nöronal işlev ölçütlerini iyileştiriyor. Özellikle talarozol, dopamin‑benzeri nöron sayısını artırıyor ve organoidler ani enerji yoksunluğuna maruz kaldığında daha güçlü bir kalsiyum sinyali geri getirerek ağ yanıt verebilirliğinde kısmi bir toparlanma olduğunu düşündürüyor.
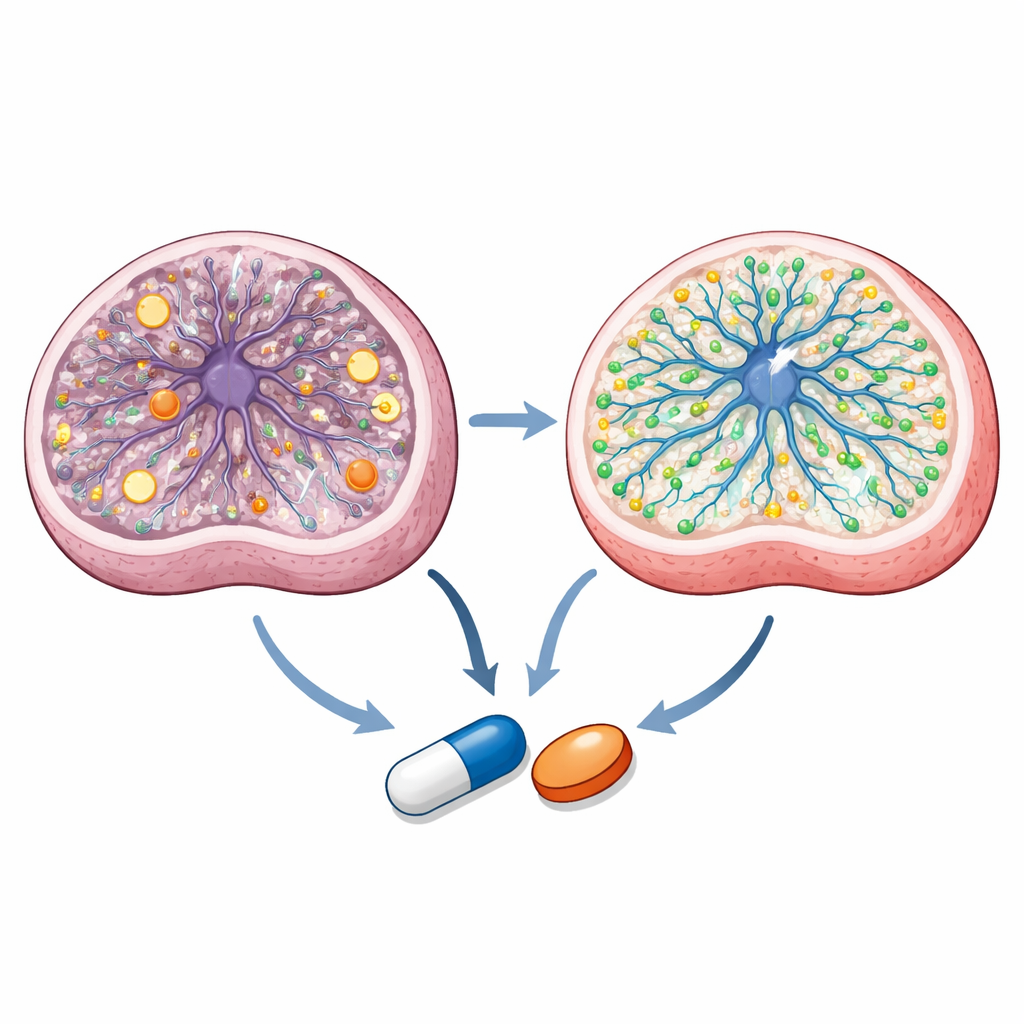
Bileşiklerin Hücre İçinde Nasıl İşlediğini Ortaya Çıkarmak
Daha derine inildiğinde, ekip iki azol ilacın örtüşen ama farklı yollarla etki ettiğini buluyor. Ayrıntılı metabolit ölçümleri, Leigh nöral progenitör hücrelerinin dengesiz bir enerji durumuna ve bozulmuş mitokondriyal kimyaya sahip olduğunu gösteriyor. Talarozol, hücrenin merkezi metabolik döngüsündeki kilit enerji oranlarını ve birkaç ara ürünü normale getirirken, her iki ilaç da belirli metabolik darboğazları düzeltiyor. Lipid profilleme ve görüntüleme, sertakonazolün membranla ilişkili yağlar ve kolesterol üzerinde güçlü etkisi olduğunu; belirli sphingolipidleri yeniden oluşturduğunu ve Leigh hücrelerinde azalmış olan membrana bağlı kolesterolü artırdığını ortaya koyuyor. Tedavi edilen organoidlerin tek hücre RNA sekanslaması, her iki ilacın da nöron oluşumuna ve lipid metabolizmasına bağlı gen programlarını teşvik ettiğini ve aşırı aktif mitokondriyal gen ifadesini düşürdüğünü gösteriyor. Hesaplamalı doklama ve canlı hücre raporlayıcı denemeleri ayrıca talarozolün beyin gelişimi için kritik olan bir A vitamini türevi olan retinoik asidi parçalayan enzimleri hedefleyebileceğini ve mitokondriyal hastalıklarda terapötik hedef olarak öne sürülen nükleer reseptör PPARγ’yi aktive edebileceğini düşündürüyor.
Leigh Sendromlu Çocuklar İçin Bunun Anlamı Ne Olabilir
Talarozol ve sertakonazol bu modellerde hastalığın tüm özelliklerini tamamen tersine çevirmese de, maya, 2B nöronlar ve 3B insan orta beyin organoidleri genelinde Leigh sendromunun birkaç temel özelliğini tutarlı biçimde hafifletiyor. Çalışma, derin öğrenmeyi insan organoidleri ve basit maya taramalarıyla birleştirmenin, şu anda tedavi seçeneği olmayan nadir bir pediatrik bozukluk için yeniden kullanılabilir ilaçları hızla bulabileceğini gösteriyor. Aileler için bu henüz onaylanmış bir tedaviye dönüşmüyor, fakat iki somut ilaç adayı ve belki daha da önemlisi genel bir strateji sunuyor: büyük ilaç kütüphanelerini ileri hesaplamayla filtreleyip en umut veren adayları gerçekçi insan mini‑beyin modellerinde test etmek. Bu yaklaşım, temel biyolojiden Leigh sendromu ve mitokondriyal işlev bozukluğuna dayalı diğer nörogelişimsel hastalıklar için anlamlı tedavi seçeneklerine giden yolu kısaltabilir.
Atıf: Menacho, C., Okawa, S., Álvarez-Merz, I. et al. Accelerating Leigh syndrome drug discovery through deep learning screening in brain organoids. Nat Commun 17, 3570 (2026). https://doi.org/10.1038/s41467-026-71391-2
Anahtar kelimeler: Leigh sendromu, beyin organoidleri, derin öğrenme, ilaç yeniden kullanımı, mitokondriyal hastalık