Clear Sky Science · it
Accelerare la scoperta di farmaci per la sindrome di Leigh mediante screening con deep learning in organoidi cerebrali
Trovare nuova speranza per una devastante malattia cerebrale dell’infanzia
La sindrome di Leigh è una malattia rara, spesso fatale, che colpisce neonati e bambini piccoli, privando il cervello dell’energia necessaria per crescere e funzionare. Attualmente le famiglie non dispongono di terapie comprovate, solo di cure di supporto. Questo studio unisce biologia all’avanguardia e intelligenza artificiale per cercare farmaci già esistenti che potrebbero aiutare. Combinando previsioni guidate dal computer con piccoli modelli cerebrali coltivati in laboratorio, i ricercatori identificano due medicinali che ripristinano parzialmente l’attività simile a quella cerebrale nei modelli della sindrome di Leigh, indicando una via più rapida per scoprire terapie per malattie pediatriche rare.
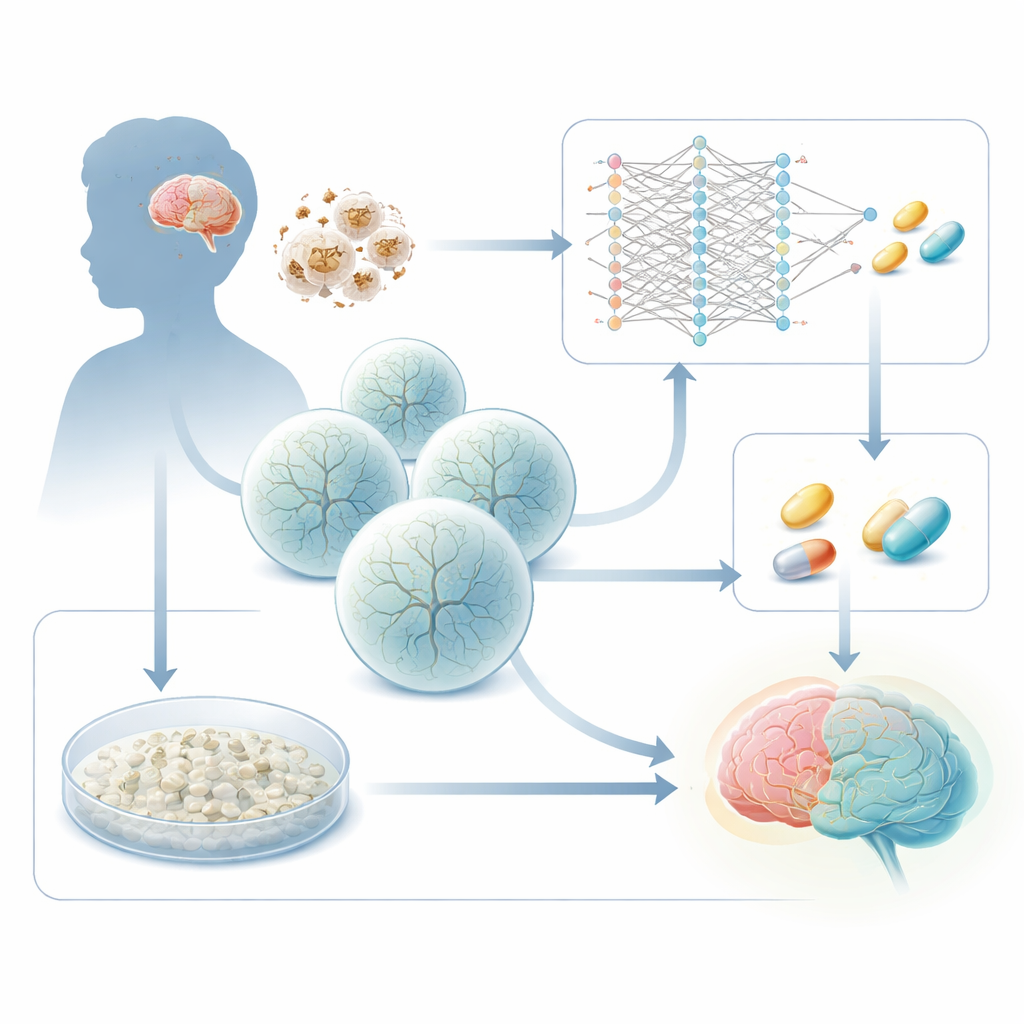
Come il fallimento energetico danneggia il cervello in sviluppo
La sindrome di Leigh è causata da difetti ereditari in geni che alimentano i mitocondri, le “batterie” della cellula. Un colpevole comune è un gene chiamato SURF1, necessario per un passaggio chiave nel macchinario cellulare che produce energia. Quando SURF1 è difettoso, le regioni cerebrali con alto fabbisogno energetico—in particolare strutture profonde del mesencefalo e dei gangli della base—cominciano a cedere. Lavori precedenti di questo gruppo, usando cellule staminali derivate da pazienti per coltivare organoidi cerebrali 3D, hanno mostrato che gli organoidi di Leigh formano neuroni in modo inefficace, con ramificazioni e connessioni anomale. Il nuovo studio pone una domanda pratica: questi cambiamenti specifici della malattia possono essere sfruttati come lettura per trovare farmaci che spingano le cellule malate verso uno sviluppo più normale?
Insegnare ai computer a suggerire farmaci utili
Un braccio del progetto utilizza un framework di deep learning costruito specificamente per cellule non tumorali. Invece di limitarsi ad abbinare le firme geniche della malattia a un catalogo di risposte ai farmaci, l’algoritmo impara come le reti di controllo genico cambiano mentre le cellule cerebrali giovani progrediscono da glia radiale simili a cellule staminali, a progenitori intermedi, fino a neuroni maturi. Utilizzando dati di RNA-seq a singola cellula da organoidi cerebrali di Leigh e sani, il modello inferisce quali fattori di trascrizione devono essere modulati per spostare le cellule malate lungo il percorso di sviluppo normale. Cerca quindi in un ampio database di farmaci e predice quali composti dovrebbero “indirizzare” la rete da uno stato simile a Leigh verso uno stato neuronale più sano. Da migliaia di candidati restringe la lista a poche dozzine di farmaci con effetti promettenti sul metabolismo cellulare.
Lasciare che lievito e mini‑cervelli votino i migliori candidati
In parallelo, il team conduce uno screening molto diverso nel lievito. Il lievito di birra possiede una sua versione del gene SURF1 e la sua delezione rende le cellule vulnerabili quando i nutrienti scarseggiano—un’eco dello stress energetico nella sindrome di Leigh. I ricercatori espongono il lievito privo di SURF1 a 2.250 farmaci già approvati e misurano quali sostanze chimiche meglio ne salvano la sopravvivenza. In modo intrigante, sia lo screening con intelligenza artificiale sia il test di sopravvivenza del lievito indicano la stessa famiglia chimica: le azolo, un gruppo noto soprattutto come antifungini e farmaci per la dermatologia. Tra questi, il team si concentra su due composti, talarozolo e sertaconazolo, che sembrano sufficientemente sicuri per un’esposizione prolungata nei modelli cellulari umani e che migliorano marcatamente la formazione precoce dei neuroni derivati da pazienti con Leigh in coltura.
Testare i farmaci negli organoidi del mesencefalo umano
Per avvicinarsi alle regioni cerebrali colpite nei pazienti, i ricercatori generano organoidi del mesencefalo a partire da cellule progenitrici neurali derivate dai pazienti. Queste strutture 3D contengono neuroni produttori di dopamina, cellule di supporto e circuiti in sviluppo. Rispetto agli organoidi derivati da cellule sane, gli organoidi di Leigh crescono più grandi ma presentano una struttura neuronale peggiore, rilasciano più acido lattico nel mezzo di coltura e rispondono in modo anomalo quando sottoposti a stress energetico acuto. Il trattamento degli organoidi del mesencefalo di Leigh per diverse settimane con basse dosi di talarozolo o sertaconazolo rallenta la loro crescita eccessiva, riduce il rilascio di lattato di circa un quinto e migliora alcune misure della funzione neuronale. Il talarozolo, in particolare, aumenta il numero di neuroni di tipo dopaminergico e ripristina un segnale di calcio più forte quando gli organoidi vengono sfidati con una privazione energetica improvvisa, suggerendo un recupero parziale della reattività della rete.
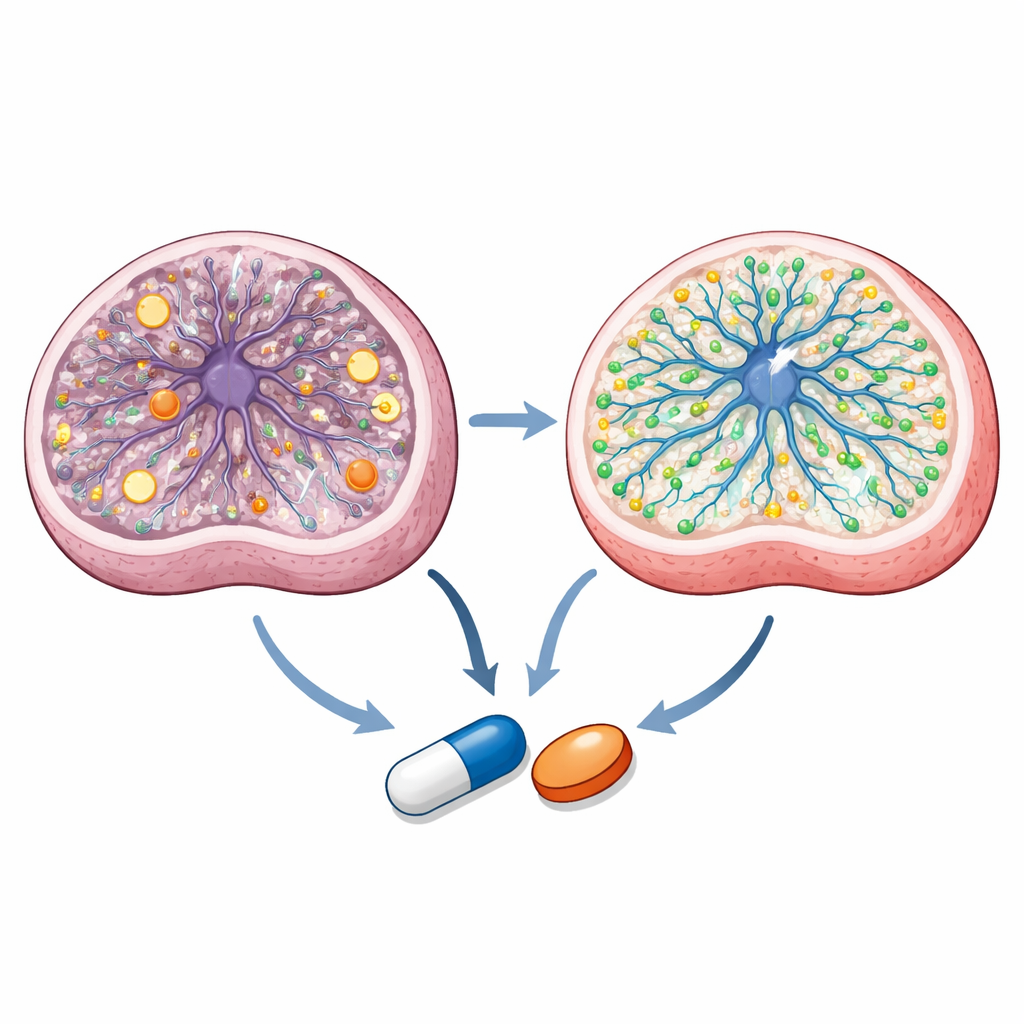
Scoprire come i composti agiscono all’interno delle cellule
Approfondendo, il team scopre che i due farmaci azolici agiscono attraverso vie sovrapposte ma distinte. Misurazioni dettagliate dei metaboliti mostrano che le cellule progenitrici neurali di Leigh presentano uno stato energetico squilibrato e una chimica mitocondriale alterata. Il talarozolo normalizza rapporti energetici chiave e diversi intermedi del ciclo metabolico centrale della cellula, mentre entrambi i farmaci correggono specifici colli di bottiglia metabolici. Il profilo dei lipidi e l’imaging rivelano che il sertaconazolo ha un impatto marcato sui grassi associati alle membrane e sul colesterolo, ripristinando alcuni sfingolipidi e aumentando il colesterolo legato alla membrana, ridotto nelle cellule di Leigh. L’RNA-seq a singola cellula degli organoidi trattati indica che entrambi i farmaci promuovono programmi genici legati alla generazione di neuroni e al metabolismo lipidico, attenuando al contempo l’espressione mitocondriale iperattiva. Docking computazionale e saggi con reporter in cellule vive suggeriscono inoltre che il talarozolo interagisce con enzimi che degradano l’acido retinoico—un derivato della vitamina A cruciale per lo sviluppo cerebrale—e attiva un recettore nucleare chiamato PPARγ, implicato come possibile leva terapeutica nelle malattie mitocondriali.
Cosa potrebbe significare per i bambini con sindrome di Leigh
Pur non invertendo completamente tutte le caratteristiche della malattia in questi modelli, talarozolo e sertaconazolo attenuano con coerenza diversi segni distintivi della sindrome di Leigh in lievito, neuroni 2D e organoidi del mesencefalo umano 3D. Il lavoro dimostra che combinare deep learning con organoidi umani e semplici screening nel lievito può rapidamente individuare farmaci riutilizzabili per un raro disturbo pediatrico attualmente privo di terapie. Per le famiglie ciò non si traduce ancora in una terapia approvata, ma fornisce due candidati farmaci concreti e, forse più importante, una strategia generale: usare calcoli avanzati per filtrare enormi librerie di farmaci e poi testare i colpi più promettenti in modelli umani mini‑cerebrali realistici. Questo approccio potrebbe accorciare il percorso dalla biologia di base a opzioni terapeutiche significative per la sindrome di Leigh e altre malattie neuroevolutive radicate in disfunzioni mitocondriali.
Citazione: Menacho, C., Okawa, S., Álvarez-Merz, I. et al. Accelerating Leigh syndrome drug discovery through deep learning screening in brain organoids. Nat Commun 17, 3570 (2026). https://doi.org/10.1038/s41467-026-71391-2
Parole chiave: Sindrome di Leigh, organoidi cerebrali, deep learning, riutilizzo di farmaci, malattia mitocondriale