Clear Sky Science · pt
Acelerando a descoberta de medicamentos para a síndrome de Leigh por meio de triagem com aprendizado profundo em organoides cerebrais
Encontrando Nova Esperança para uma Devastadora Doença Cerebral Infantil
A síndrome de Leigh é um distúrbio raro, frequentemente fatal, que atinge bebês e crianças pequenas, privando o cérebro da energia necessária para crescer e funcionar. Atualmente, as famílias não dispõem de tratamentos comprovados, apenas de cuidados de suporte. Este estudo reúne biologia de ponta e inteligência artificial para procurar medicamentos já existentes que possam ajudar. Ao combinar previsões guiadas por computador com pequenos modelos cerebrais cultivados em laboratório, os pesquisadores identificam dois fármacos que restauram parcialmente a atividade semelhante à cerebral em modelos da síndrome de Leigh, indicando um caminho mais rápido para descobrir terapias para doenças pediátricas raras.
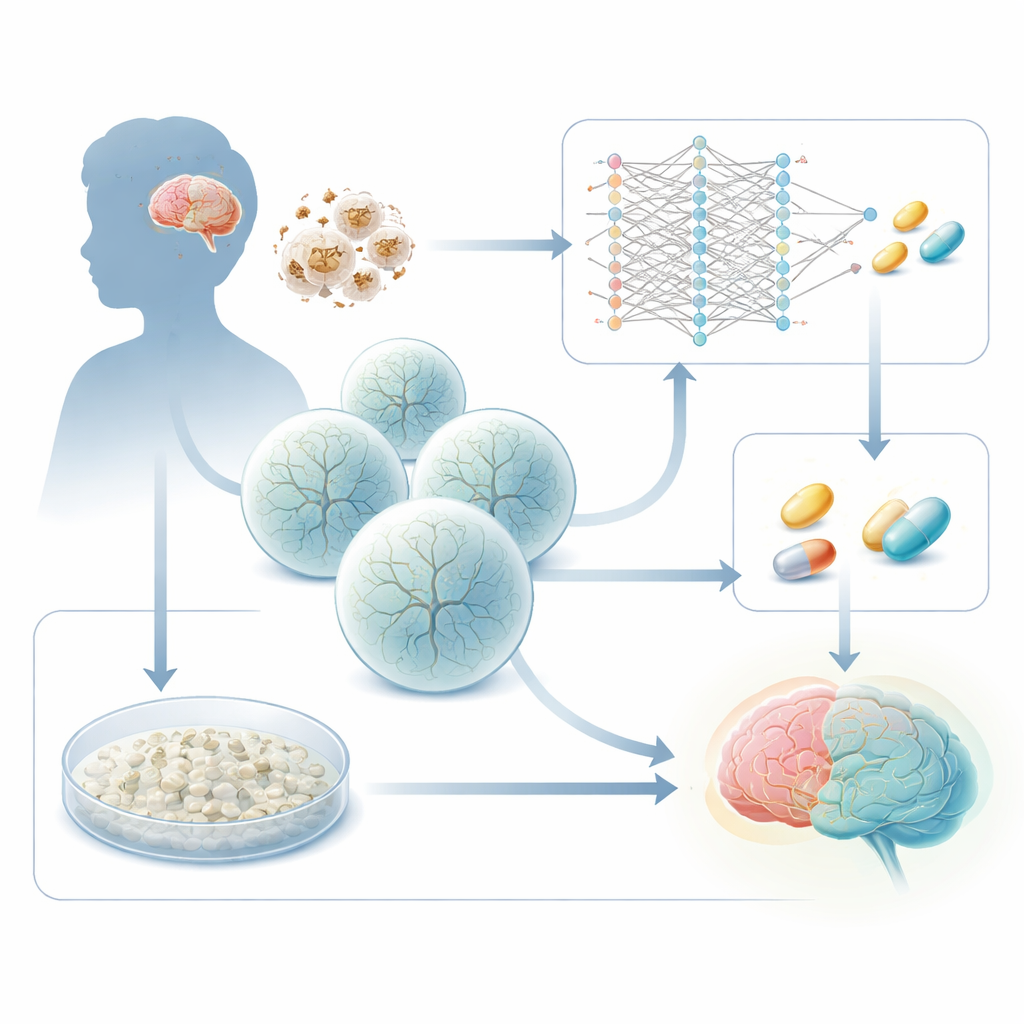
Como a Falha Energética Prejudica o Cérebro em Desenvolvimento
A síndrome de Leigh é causada por defeitos herdados em genes que abastecem as mitocôndrias, as “baterias” da célula. Um culpado comum é um gene chamado SURF1, necessário para uma etapa-chave na maquinaria produtora de energia celular. Quando o SURF1 está defeituoso, regiões cerebrais que demandam muita energia — especialmente estruturas profundas do mesencéfalo e dos gânglios basais — começam a falhar. Trabalhos anteriores deste grupo usaram células-tronco derivadas de pacientes para cultivar organoides cerebrais 3D e mostraram que os organoides da Leigh formam neurônios de forma deficiente, com ramificações e conexões anormais. O novo estudo faz uma pergunta prática: essas alterações específicas da doença podem ser exploradas como um sinal para encontrar medicamentos que empurrem as células doentes de volta ao desenvolvimento normal?
Ensinando Computadores a Sugerir Medicamentos Úteis
Um braço do projeto usa uma estrutura de aprendizado profundo construída especificamente para células não cancerígenas. Em vez de simplesmente comparar assinaturas gênicas da doença com um catálogo de respostas a fármacos, o algoritmo aprende como as redes de controle gênico mudam à medida que células cerebrais jovens progridem de glia radial semelhante a tronco, para progenitores intermediários, até neurônios maduros. Usando sequenciamento de RNA de célula única de organoides cerebrais de Leigh e saudáveis, o modelo infere quais fatores de transcrição precisam ser ajustados para mover as células doentes ao longo do caminho de desenvolvimento normal. Em seguida, ele vasculha um grande banco de dados de medicamentos e prevê quais compostos devem “guiar” a rede de um estado semelhante ao da Leigh para um estado neuronal mais saudável. De milhares de candidatos, reduz a lista a algumas dezenas de medicamentos com efeitos promissores no metabolismo celular.
Deixando Leveduras e Mini‑Cérebros Votarem nos Melhores Candidatos
Em paralelo, a equipe realiza uma triagem muito diferente em levedura. A levedura de padeiro tem sua própria versão do gene SURF1, e deletá‑lo torna as células vulneráveis quando os nutrientes são escassos — um eco do estresse energético na síndrome de Leigh. Os pesquisadores expõem leveduras deficientes em SURF1 a 2.250 medicamentos já aprovados e medem quais produtos químicos melhor resgatam a sobrevivência. Intrigantemente, tanto a triagem por inteligência artificial quanto o teste de sobrevivência em levedura apontam para a mesma família química: os azóis, um grupo mais conhecido como antifúngicos e medicamentos de dermatologia. Dentre esses, a equipe foca em dois compostos, talarozol e sertaconazol, que parecem seguros o suficiente para exposição prolongada em modelos celulares humanos e que melhoram fortemente a formação inicial de neurônios derivados de Leigh em cultura.
Testando os Medicamentos em Organoides de Mesencéfalo Humanos
Para se aproximar das regiões cerebrais afetadas nos pacientes, os pesquisadores geram organoides de mesencéfalo a partir de células progenitoras neurais derivadas de pacientes. Essas estruturas 3D contêm neurônios produtores de dopamina, células de suporte e circuitos em desenvolvimento. Em comparação com organoides de células saudáveis, os organoides de Leigh crescem mais, mas têm estrutura neuronal pior, liberam mais ácido lático no meio de cultura e respondem de forma anormal quando submetidos a estresse energético agudo. Tratar organoides de mesencéfalo de Leigh por várias semanas com baixas doses de talarozol ou sertaconazol desacelera seu crescimento excessivo, reduz a liberação de lactato em cerca de um quinto e melhora algumas medidas de função neuronal. O talarozol, em particular, aumenta o número de neurônios semelhantes aos produtores de dopamina e restaura um sinal de cálcio mais forte quando os organoides são desafiados com privação súbita de energia, sugerindo uma recuperação parcial da responsividade da rede.
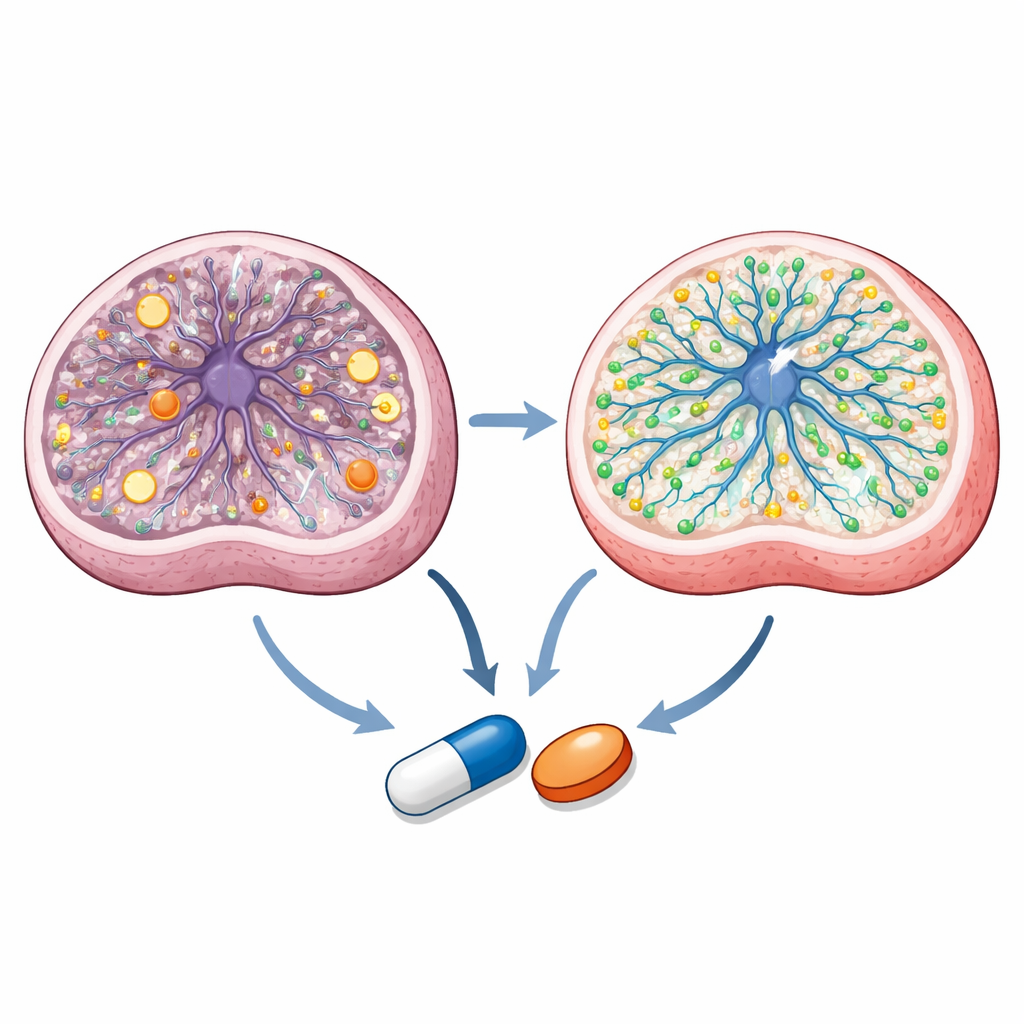
Descobrindo Como os Compostos Agem Dentro das Células
Aprofundando, a equipe descobre que os dois fármacos azóis atuam por vias sobrepostas, porém distintas. Medições detalhadas de metabólitos mostram que as células progenitoras neurais de Leigh apresentam um estado energético desequilibrado e química mitocondrial alterada. O talarozol normaliza razões energéticas-chave e vários intermediários do ciclo metabólico central da célula, enquanto ambos os fármacos corrigem gargalos metabólicos específicos. Perfilagem lipídica e imagens revelam que o sertaconazol tem forte impacto nas gorduras e no colesterol associados à membrana, restaurando certos esfingolipídios e aumentando o colesterol ligado à membrana que está reduzido nas células de Leigh. O sequenciamento de RNA de célula única de organoides tratados indica que ambos os medicamentos promovem programas gênicos ligados à geração de neurônios e ao metabolismo lipídico, ao mesmo tempo em que reduzem a expressão mitocondrial hiperativa. Acoplamento computacional e ensaios com repórteres em células vivas sugerem ainda que o talarozol interage com enzimas que degradam o ácido retinoico — um derivado da vitamina A crucial para o desenvolvimento cerebral — e ativa um receptor nuclear chamado PPARγ, implicado como uma alavanca terapêutica em doenças mitocondriais.
O Que Isso Pode Significar para Crianças com Síndrome de Leigh
Embora o talarozol e o sertaconazol não revertam totalmente todas as características da doença nesses modelos, eles atenuam consistentemente vários marcos da síndrome de Leigh em leveduras, neurônios 2D e organoides humanos 3D de mesencéfalo. O trabalho demonstra que combinar aprendizado profundo com organoides humanos e triagens simples em levedura pode rapidamente identificar medicamentos reaproveitáveis para um distúrbio pediátrico raro que atualmente não tem tratamentos. Para as famílias, isso ainda não se traduz em uma terapia aprovada, mas fornece dois candidatos a fármaco concretos e, talvez mais importante, uma estratégia geral: usar computação avançada para filtrar enormes bibliotecas de medicamentos e então testar os acertos mais promissores em modelos humanos realistas de mini‑cérebro. Essa abordagem pode encurtar o caminho da biologia básica até opções de tratamento significativas para a síndrome de Leigh e outras doenças do neurodesenvolvimento enraizadas na disfunção mitocondrial.
Citação: Menacho, C., Okawa, S., Álvarez-Merz, I. et al. Accelerating Leigh syndrome drug discovery through deep learning screening in brain organoids. Nat Commun 17, 3570 (2026). https://doi.org/10.1038/s41467-026-71391-2
Palavras-chave: síndrome de Leigh, organoides cerebrais, aprendizado profundo, reutilização de medicamentos, doença mitocondrial