Clear Sky Science · ar
تسريع اكتشاف أدوية متلازمة لي عبر فحص بالتعلّم العميق في العضويات الدماغية
البحث عن أمل جديد لمرض دماغي طفولي مدمر
متلازمة لي هي اضطراب نادر وغالبًا ما يكون قاتلًا يصيب الرضع والأطفال الصغار، ويسلب أدمغتهم الطاقة اللازمة للنمو والأداء. لا تتوفر عائلات المرضى علاجات مثبتة في الوقت الحالي، بل رعاية داعمة فقط. تجمع هذه الدراسة بين أحدث أساليب البيولوجيا والذكاء الاصطناعي للبحث عن أدوية موجودة قد تفيد. من خلال الجمع بين التنبؤات الموجهة بالحاسوب ونماذج دماغية صغيرة مزروعة مخبريًا، يحدد الباحثون دوائين يعيدان جزئيًا نشاطًا شبيهًا بالدماغ في نماذج متلازمة لي، مما يشير إلى طريقة أسرع لاكتشاف علاجات للأمراض الطفولية النادرة.
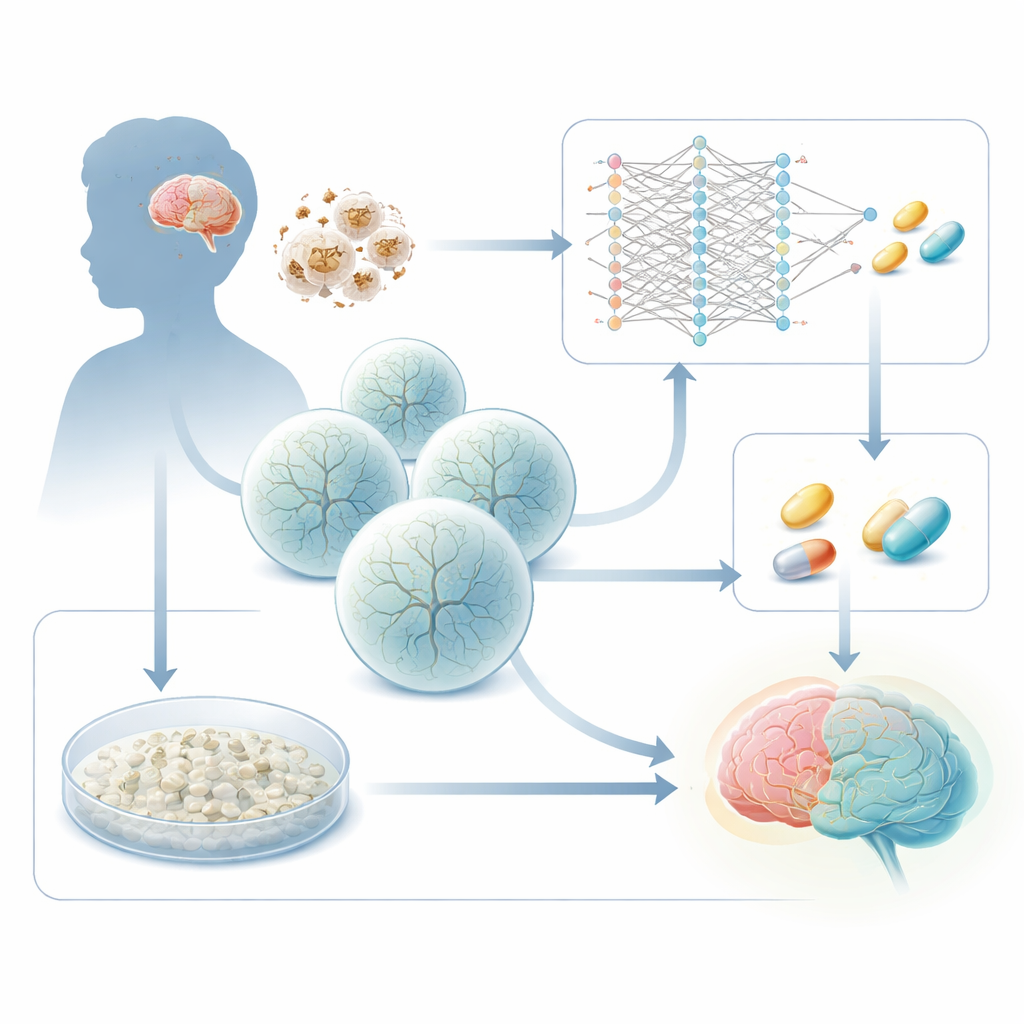
كيف يضر فشل الطاقة الدماغ النامي
تنتج متلازمة لي عن عيوب وراثية في جينات تزود الميتوكوندريا بالطاقة، التي تعتبر "بطاريات" الخلية. أحد المذنبين الشائعين هو جين اسمه SURF1، الضروري لخطوة رئيسية في آلية الخلية لإنتاج الطاقة. عندما يكون SURF1 معيبًا، تبدأ مناطق دماغية ذات طلب طاقي عالٍ—وخاصة الهياكل العميقة في منتصف الدماغ والعقد القاعدية—في الفشل. أظهرت أعمال سابقة لهذه المجموعة، باستخدام خلايا جذعية مشتقة من مرضى، أن العضويات الدماغية لمرضى لي تكوّن خلايا عصبية بشكل ضعيف مع تشعبات وتوصيلات غير طبيعية. تطرح الدراسة الجديدة سؤالًا عمليًا: هل يمكن استغلال هذه التغيرات الخاصة بالمرض كقراءة لونية لاكتشاف أدوية تعيد الخلايا المريضة نحو التطور الطبيعي؟
تعليم الحواسيب لاقتراح أدوية مفيدة
يستخدم أحد فروع المشروع إطار تعلّم عميق بُنِي خصيصًا للخلايا غير السرطانية. بدلًا من مطابقة تواقيع الجينات المرضية ببساطة مع فهرس استجابات الأدوية، يتعلم الخوارزم كيف تتغير شبكات التحكم الجيني مع تقدم خلايا الدماغ الصغيرة من الخلايا الجذعية الشُعاعية إلى الخلايا الوليدة الوسيطة ثم إلى الخلايا العصبية الناضجة. باستخدام تتبّع التعبير الجيني على مستوى الخلية المفردة من العضويات الدماغية لمرضى لي والعضويات السليمة، يستنتج النموذج عوامل النسخ التي يجب تعديلها لدفع الخلايا المريضة على طول المسار التطوري الطبيعي. ثم يبحث في قاعدة بيانات كبيرة للأدوية ويتنبأ بأي المركبات ينبغي أن «توجّه» الشبكة من حالة تشبه لي نحو حالة عصبية أكثر صحة. ومن بين آلاف المرشحين، يضيق القائمة إلى بضعة عشرات من الأدوية ذات التأثيرات الواعدة على أيض الخلية.
السماح للخَمِيرة والعضيات الصغيرة بالتصويت على أفضل المرشحين
بالتوازي، تُجري الفريق فحصًا مختلفًا تمامًا في الخميرة. لخميرة الخباز نسخة من جين SURF1، وإزالته تجعل الخلايا أكثر ضعفًا عند ندرة المغذيات—وهو صدى لضغط الطاقة في متلازمة لي. يعرض الباحثون خميرة ناقصة SURF1 إلى 2250 دواءً معتمدًا مسبقًا ويقيسون أي المواد الكيميائية تنقذ البقاء بشكل أفضل. والمثير أن كلًا من فحص الذكاء الاصطناعي واختبار بقاء الخميرة أشارا إلى نفس العائلة الكيميائية: الأزولات، وهي مجموعة تُعرف أكثر كأدوية مضادة للفطريات ومستحضرات جلدية. من بينها يركز الفريق على مركبين، تالاروزول وسيرتاكونازول، اللذين يبدوان آمنين بما يكفي للتعرض طويل الأمد في نماذج الخلايا البشرية ويُحسّنان بقوة تكوّن الخلايا العصبية المبكرة في خلايا مشتقة من مرضى لي في طبق مخبري.
اختبار الأدوية في عضويات منتصف الدماغ البشرية
للاقتراب من مناطق الدماغ المتأثرة لدى المرضى، يولّد الباحثون عضويات منتصف الدماغ من خلايا سلف عصبية مشتقة من المرضى. تحتوي هذه البنى ثلاثية الأبعاد على خلايا عصبية منتجة للدوبامين، وخلايا داعمة، ودارات في طور التطور. بالمقارنة مع عضويات الخلايا السليمة، تنمو عضويات لي أكبر حجمًا لكنها أقل جودة في البنية العصبية، وتفرز حمض اللاكتيك أكثر في الوسط المزروع، وتستجيب بشكل غير طبيعي عند تعريضها لضغط طاقة حاد. علاج عضويات منتصف الدماغ الخاصة بلي لعدة أسابيع بجرعات منخفضة من تالاروزول أو سيرتاكونازول يبطئ نموها المفرط، ويقلل إفراز اللاكتات بحوالي خُمس، ويحسّن بعض مقاييس وظيفة الخلايا العصبية. يزيد تالاروزول، على وجه الخصوص، من عدد الخلايا الشبيهة بالدوبامين ويعيد إشارة كالسيوم أقوى عند تحدّي العضويات بنقص طاقة مفاجئ، مما يشير إلى تعاف جزئي في استجابة الشبكة.
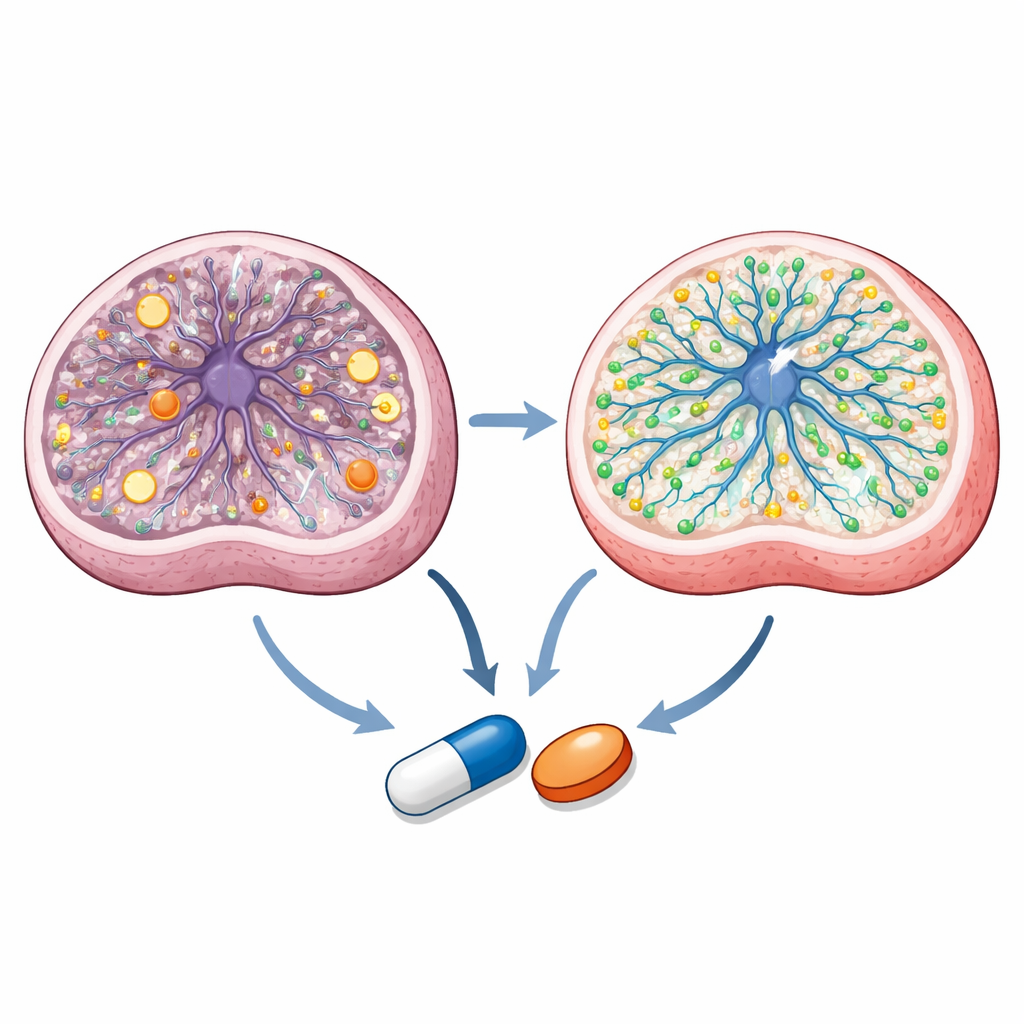
كشف كيفية عمل المركبات داخل الخلايا
بالتعمق أكثر، يجد الفريق أن الدوائين من فئة الأزولات يعلمان عبر طرق متداخلة لكن مميزة. تُظهر قياسات مستفيضة للمواد الأيضية أن الخلايا السلف العصبية لمرضى لي تتمتع بحالة طاقية غير متوازنة وكيمياء ميتوكوندرية معطلة. يعمل تالاروزول على تطبيع نسب الطاقة الرئيسية وبعض الوسطاء في دورة الأيض المركزية للخلية، بينما يصحح كلا الدوائين اختناقات أيضية محددة. يكشف تحليل الدهون والتصوير أن سيرتاكونازول له تأثير قوي على الدهون المرتبطة بالغشاء والكوليسترول، مستعيدًا بعض السفينجوليبيدات وزيادة الكوليسترول المرتبط بالغشاء الذي يكون منخفضًا في خلايا لي. يشير تتبّع التعبير الجيني على مستوى الخلية المفردة للعضويات المعالجة إلى أن كلا الدوائين يعززان برامج جينية مرتبطة بتكوين الخلايا العصبية وأيض الدهون مع تخفيف التعبير المفرط للجينات الميتوكوندرية. وتقترح دراسات التشكيل الحسابي وتجارب مؤشرات الخلايا الحية أن تالاروزول يتداخل مع إنزيمات تكسر حمض الريتينويك—مشتق فيتامين أ الحيوي لتطور الدماغ—وينشط مستقبلًا نوويًا يسمى PPARγ، الذي ارتبط كآلية علاجية محتملة في أمراض الميتوكوندريا.
ما الذي قد يعنيه هذا للأطفال المصابين بمتلازمة لي
رغم أن تالاروزول وسيرتاكونازول لا يعيدان بشكل كامل كل مظاهر المرض في هذه النماذج، إلا أنهما يخففان باستمرار عدة سمات مميزة لمتلازمة لي عبر الخميرة والخلايا ثنائية الأبعاد وعضويات منتصف الدماغ البشرية ثلاثية الأبعاد. تُظهر الدراسة أن الجمع بين التعلّم العميق والعضويات البشرية وفحوص الخميرة البسيطة يمكن أن يحدد بسرعة أدوية قابلة لإعادة الاستخدام لاضطراب طفولي نادر يفتقر حاليًا لعلاجات. بالنسبة للعائلات، لا يعني هذا ترجمة فورية إلى علاج معتمد، لكنه يقدّم مرشحين دوائيين ملموسين وربما الأهم من ذلك، استراتيجية عامة: استخدام الحسابات المتقدمة لترشيح مكتبات دوائية شاسعة، ثم اختبار أفضل النتائج في نماذج بشرية واقعية لدماغ صغير. قد يقصر هذا النهج الطريق من البيولوجيا الأساسية إلى خيارات علاجية ذات مغزى لمتلازمة لي وغيرها من أمراض التطور العصبي الجذريّة في اختلال وظائف الميتوكوندريا.
الاستشهاد: Menacho, C., Okawa, S., Álvarez-Merz, I. et al. Accelerating Leigh syndrome drug discovery through deep learning screening in brain organoids. Nat Commun 17, 3570 (2026). https://doi.org/10.1038/s41467-026-71391-2
الكلمات المفتاحية: متلازمة لي, العضويات الدماغية, التعلّم العميق, إعادة توظيف الأدوية, أمراض الميتوكوندريا