Clear Sky Science · zh
儿茶酚胺类G蛋白偶联受体的天然配体选择性的分子机制
细胞如何分辨相似信号
我们的大脑和身体依赖微小的化学信使——如多巴胺和肾上腺素——在细胞之间传递指令。这些分子外观极其相似,但每一种必须在正确的地点触发恰当的反应,无论是提高注意力、加快心率,还是改善情绪。本研究提出了一个貌似简单的问题:几乎相同的分子如何能“拨打”不同的细胞电话号码,且我们能否有意重接这些号码以用于医学和生物工程?
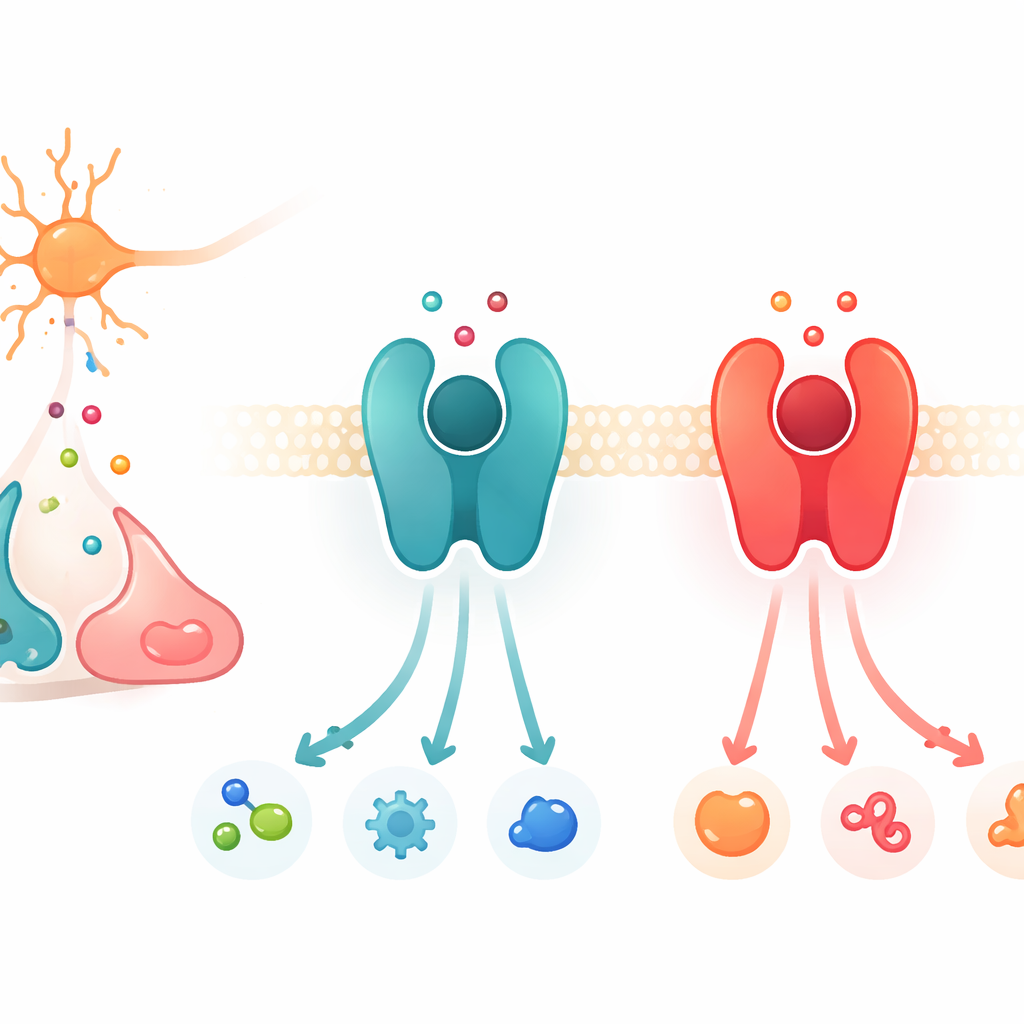
细胞表面的信号交换机
本工作聚焦于一类大型蛋白质家族,称为G蛋白偶联受体(GPCR)。这些蛋白嵌入细胞膜,像交换机一样工作:当外部化学信使结合时,受体形状改变并激活内部的伴侣蛋白,发起信号级联。在众多GPCR中,有一部分对儿茶酚胺——相互关联的信使多巴胺、肾上腺素和去甲肾上腺素——做出响应。两个关键例子是偏好肾上腺素和去甲肾上腺素的β2-肾上腺素能受体,以及偏好多巴胺的D1多巴胺受体。尽管这些受体及其结合口袋在结构上惊人地相似,但每一种对它最敏感的信使都有高度选择性。
通过少量改变交换偏好
研究者结合进化比较、结构生物学和细胞测量,定位决定这种化学偏好的“热点”区域。通过比对来自多种物种的成百上千条受体序列,并评分β2和D1家族持续不同的位点,他们得出了一份突出的氨基酸位置清单。其中一些热点位于主要结合口袋——信使对接之处;另一些则位于蛋白内部较深处,与化学物质没有直接接触。团队随后系统性地突变这些位点,测试了一百多种受体变体对多巴胺、肾上腺素和去甲肾上腺素的响应强度,使用细胞信号输出作为读数。
调节口袋与深层控制旋钮
仅改变接触信使的残基确实改变量化选择性,但常常付出沉重代价:受体变得弱或几乎无反应,即便它们开始偏向新的配体。真正的突破出现在将结合口袋的突变与位于两个更深层相互咬合区域的突变结合时,这些区域像内部控制旋钮。在β2受体中,三螺旋界面的调整提高了其敏感性并将其向有利于多巴胺的模式推动,而未破坏功能。在D1受体中,另一个内部界面的编辑重组了一组侧链网络,间接重塑了口袋。通过合适的组合,研究者成功互换了偏好:改造后的β2受体现在偏好多巴胺,而改造后的D1受体偏好肾上腺素和去甲肾上腺素——且两者仍然能强烈发信号。
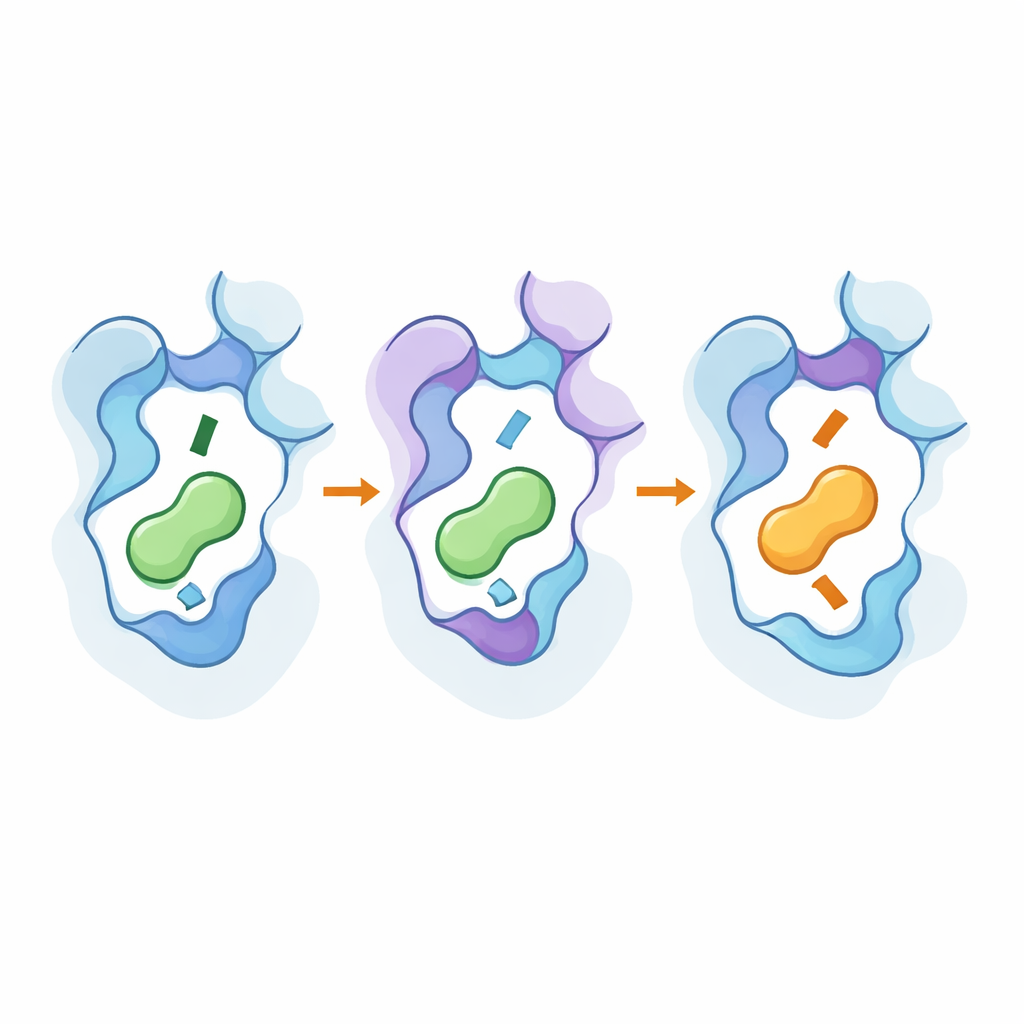
用高分辨率工具窥探内部机理
为了看到这些改变在原子层面的作用,团队使用冷冻电镜解析了工程化受体与其新偏好信使结合的三维结构,并进行了大量分子动力学模拟。结构显示关键突变微妙地移动了受体第七螺旋的部分区域和一个保守的“开关”残基,改变了口袋的深浅以及信使胺端的安置方式。远端热点有助于稳定类似激活的构象并强化将结合事件传递到蛋白内部的通路。模拟证实,一系列相互作用残基将这些外部和内部区域连接起来,并且同一小组位点可在相关受体亚型间重复使用,以在不使受体广泛多配的情况下翻转选择性。
对医学与进化的意义
通俗来说,这项研究表明,受体中的少数精心选择的“原子”像调节螺丝一样决定蛋白主要听多巴胺还是肾上腺素。这些螺丝并不全在信使对接的表面;有些埋得更深,稳定整个结构在信号到来时的弯曲方式。由于相同的设计逻辑在受体家族中反复出现,进化可以通过先通过内部调整提升响应性,再微调结合口袋,反复将相似蛋白骨架重新用于新的信使。对于药物发现,这些见解指出了精确位点——在结合位点及其周围——化学家可以针对以设计打击某一受体亚型而不影响其他亚型的药物,并可用于设计只对特定信号响应的定制受体,应用于治疗和生物传感器。
引用: Kahlous, N.A., Rinne, M.K., Zhang, X. et al. Molecular mechanisms of native ligand selectivity in catecholamine G protein-coupled receptors. Nat Commun 17, 4112 (2026). https://doi.org/10.1038/s41467-026-71361-8
关键词: G蛋白偶联受体, 多巴胺, 肾上腺素, 配体选择性, 药物设计