Clear Sky Science · nl
Moleculaire mechanismen van native ligandselectiviteit in catecholamine G-eiwit-gekoppelde receptoren
Hoe cellen vergelijkbare signalen uit elkaar houden
Onze hersenen en ons lichaam zijn afhankelijk van kleine chemische boodschappers—zoals dopamine en adrenaline—om instructies tussen cellen over te brengen. Deze moleculen lijken opmerkelijk veel op elkaar, maar elk moet op de juiste plaats het juiste antwoord oproepen, of het nu gaat om het aanscherpen van aandacht, het versnellen van het hart of het verbeteren van stemming. Deze studie stelt een bedrieglijk eenvoudige vraag: hoe weten bijna identieke moleculen verschillende ‘telefoonnummers’ van cellen aan te zetten, en kunnen we die nummers doelbewust herschakelen voor geneeskunde en bio-engineering?
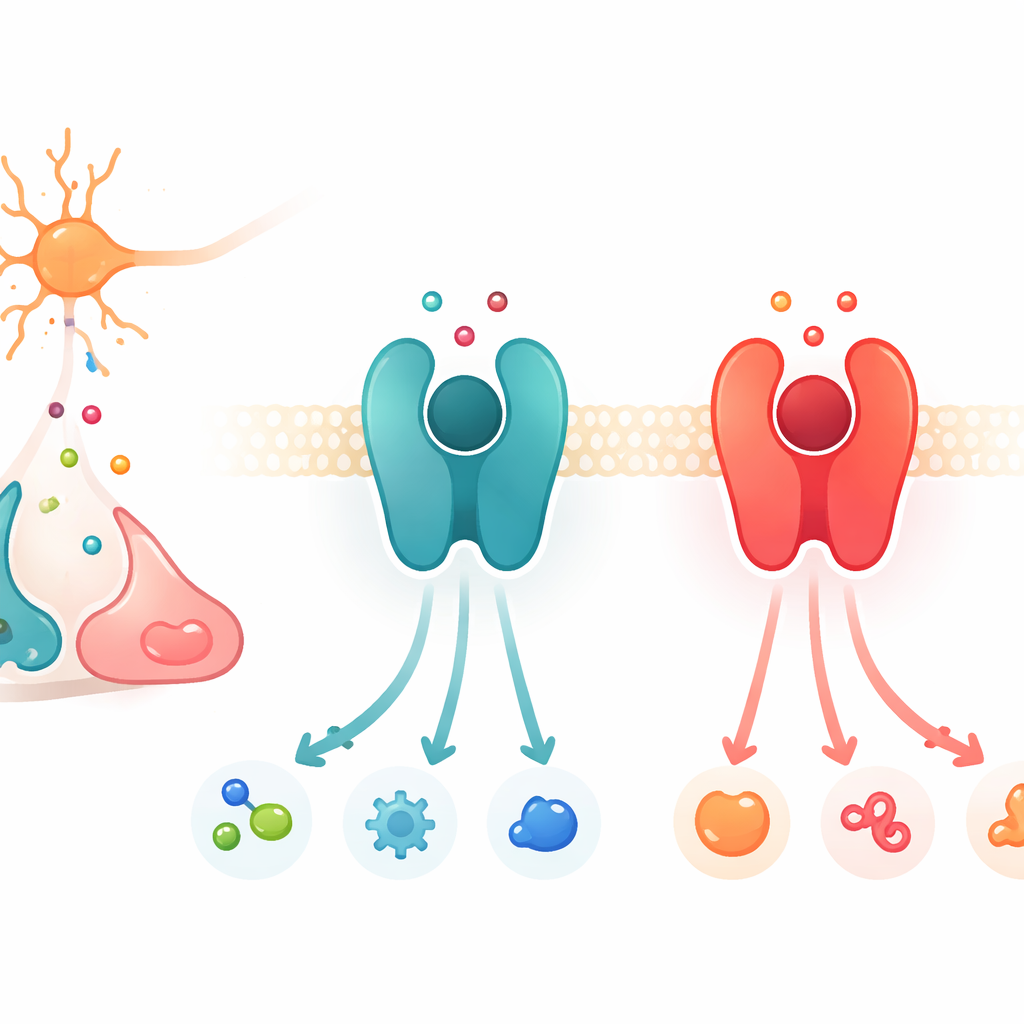
Schakelborden voor signalen op celoppervlakken
Het werk richt zich op een grote eiwitfamilie die G-eiwit–gekoppelde receptoren, of GPCRs, wordt genoemd. Deze eiwitten zitten in het celmembraan en fungeren als schakelborden: wanneer een chemische boodschapper buiten bindt, verandert de receptor van vorm en activeert partner-eiwitten binnenin, wat een keten van signalen in gang zet. Onder de vele GPCRs reageert een subgroep op catecholaminen, de nauwe verwanten dopamine, adrenaline en noradrenaline. Twee belangrijke voorbeelden zijn de β2-adrenerge receptor, die adrenaline en noradrenaline prefereert, en de D1-dopaminereceptor, die de voorkeur geeft aan dopamine. Hoewel deze receptoren en hun bindingsvakken in structuur opvallend op elkaar lijken, is elk uiterst kieskeurig over op welke boodschapper het sterkst gereageerd wordt.
Voorkeuren verwisselen met slechts een paar veranderingen
De onderzoekers combineerden evolutionaire vergelijkingen, structurele biologie en metingen in cellen om ‘hotspot’-gebieden te vinden die deze chemische voorkeur bepalen. Door honderden receptorsequenties van vele soorten uit te lijnen en te scoren waar de β2- en D1-families consequent van elkaar verschillen, stelden ze een korte lijst aminozuurposities op die eruit sprongen. Sommige van deze hotspots liggen direct in het hoofdbindingsvak, waar de boodschapper andockt, terwijl andere iets dieper in het eiwit zitten, weg van direct contact met het molecuul. Het team muteerde deze posities systematisch en testte meer dan honderd receptorvarianten op hoe goed ze reageerden op dopamine, adrenaline en noradrenaline met behulp van cellulaire afleeswaarden voor signaalsterkte.
Afstellen van holen en diepe regelknoppen
Alleen de residuen veranderen die het molecuul aanraken, wijzigde de selectiviteit, maar vaak met een hoge prijs: de receptoren werden zwak of bijna ongevoelig, zelfs wanneer ze begonnen een nieuwe ligand te prefereren. De echte doorbraak kwam toen mutaties in het bindingsvak werden gecombineerd met mutaties in twee dieper gelegen vergrendelde regio’s die als interne regelknoppen fungeren. In de β2-receptor verhoogden aanpassingen in een tri-helixinterface de gevoeligheid en duwden die richting een dopaminevriendelijke modus zonder de functie te vernietigen. In de D1-receptor reorganiseerden wijzigingen in een aparte interne interface een netwerk van zijketens dat indirect het pocketvorm verandert. Met de juiste combinaties wisselden de onderzoekers de voorkeuren volledig om: een gewijzigde β2-receptor prefereerde nu dopamine, terwijl een gewijzigde D1-receptor adrenaline en noradrenaline prefereerde—maar beide gaven nog steeds robuuste signalen.
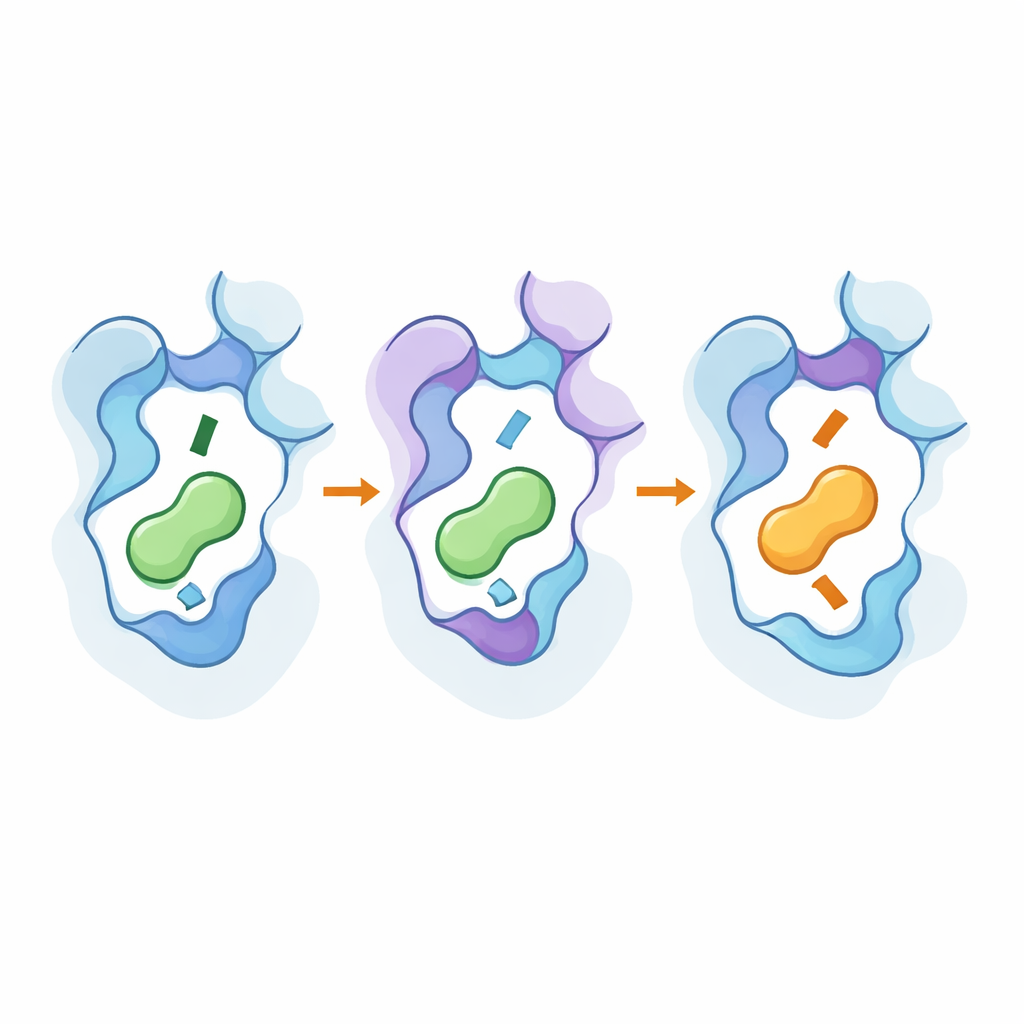
Onder de motorkap kijken met hoogresolutietools
Om te zien hoe deze veranderingen op atomair niveau werkten, gebruikte het team cryo-elektronenmicroscopie om 3D-structuren op te lossen van de gemodificeerde receptoren gebonden aan hun nieuwvoorkeursboodschappers, en voerden uitgebreide moleculaire dynamica-simulaties uit. De structuren toonden aan dat sleutelmutaties delen van de zevende helix en een geconserveerd ‘toggle’-residu subtiel verschoven, waardoor het pocket dieper of ondieper werd en de positie van het amine-einde van de boodschapper veranderde. De verre hotspots hielpen om actief-achtige vormen te stabiliseren en versterkten paden die het bindingsgebeuren naar de binnenzijde van het eiwit overbrengen. Simulaties bevestigden dat netwerken van interagerende residuen deze buiten- en binnenregio’s verbinden, en dat dezelfde kleine set posities herbruikbaar is tussen verwante receptor-subtypen om selectiviteit om te schakelen zonder de receptoren algemeen promiscu te maken.
Wat dit betekent voor geneeskunde en evolutie
In eenvoudige bewoordingen laat de studie zien dat een handvol zorgvuldig gekozen ‘atomen’ in deze receptoren fungeert als afstelschroeven die bepalen of een eiwit vooral naar dopamine of naar adrenaline luistert. Deze schroeven liggen niet allemaal aan de oppervlakte waar de boodschapper andockt; sommige zijn dieper begraven en stabiliseren hoe de hele structuur buigt wanneer een signaal binnenkomt. Omdat dezelfde ontwerplogica steeds terugkeert binnen receptorfamilies, kan evolutie vergelijkbare eiwitraamwerken herhaaldelijk herbestemmen voor nieuwe boodschappers door eerst de responsiviteit intern te verhogen en vervolgens het pocket fijn af te stemmen. Voor geneesmiddelenontdekking wijzen deze inzichten op precieze plekken—zowel in als rond de bindingsplaats—die chemici kunnen targeten om medicijnen te ontwerpen die één receptor-subtype raken terwijl andere gespaard blijven, en om aangepaste receptoren te bouwen die alleen op ontworpen signalen reageren in therapieën en biosensoren.
Bronvermelding: Kahlous, N.A., Rinne, M.K., Zhang, X. et al. Molecular mechanisms of native ligand selectivity in catecholamine G protein-coupled receptors. Nat Commun 17, 4112 (2026). https://doi.org/10.1038/s41467-026-71361-8
Trefwoorden: G-eiwit-gekoppelde receptoren, dopamine, adrenaline, ligandselectiviteit, geneesmiddelenontwerp