Clear Sky Science · ru
Молекулярные механизмы селективности нативных лигандов в катехоламиновых G-белок-связанных рецепторах
Как клетки различают похожие сигналы
Наш мозг и организм полагаются на крошечные химические мессенджеры — такие как дофамин и адреналин — которые передают указания между клетками. Эти молекулы внешне удивительно похожи, но каждая должна вызывать правильный ответ в нужном месте: будь то усиление внимания, учащение сердечного ритма или улучшение настроения. В этом исследовании задаётся на вид простейший вопрос: как почти идентичные молекулы умудряются «набирать» разные клеточные номера, и можно ли сознательно перенастроить эти номера для медицины и биоинженерии?
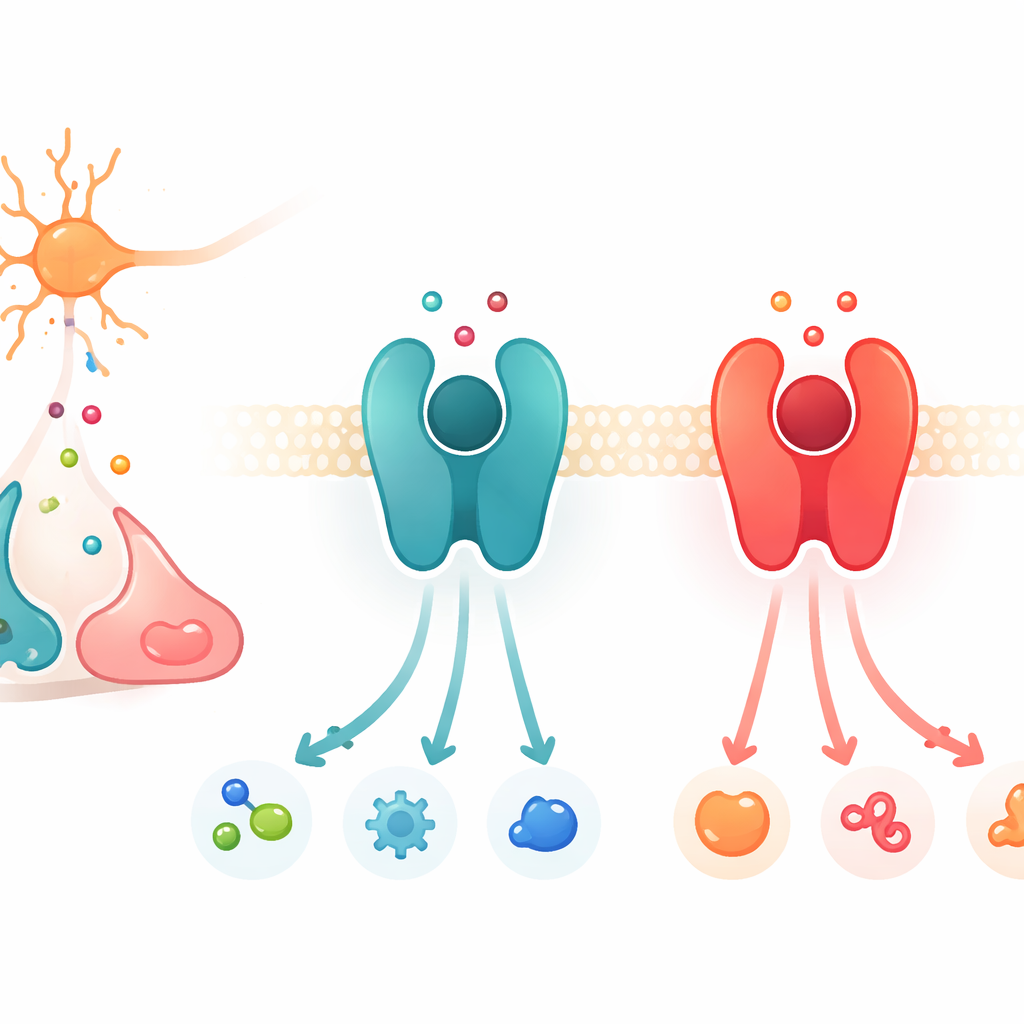
Переключатели сигналов на поверхности клетки
Работа сосредоточена на большой семье белков, называемых G-белок–связанными рецепторами, или GPCR. Эти белки сидят в мембране клетки и действуют как телефонные станции: когда снаружи связывается химический мессенджер, рецептор меняет конформацию и активирует партнёрские белки внутри клетки, запуская каскад сигналов. Среди множества GPCR есть подгруппа, реагирующая на катехоламины — близкородственные мессенджеры дофамин, адреналин и норадреналин. Два ключевых примера — β2-адренергический рецептор, который предпочитает адреналин и норадреналин, и D1-допаминовый рецептор, который отдаёт предпочтение дофамину. Хотя эти рецепторы и их карманы связывания по структуре выглядят поразительно схожими, каждый из них чрезвычайно разборчив в отношении того, на какой мессенджер он реагирует сильнее всего.
Смена предпочтений всего несколькими изменениями
Исследователи объединили эволюционные сравнения, структурную биологию и клеточные измерения, чтобы выявить «горячие точки», определяющие это химическое предпочтение. Сравнивая сотни последовательностей рецепторов из разных видов и фиксируя позиции, где семейства β2 и D1 последовательно различаются, они получили короткий список аминокислотных позиций, выделявшихся на фоне остальных. Некоторые из этих горячих точек лежат непосредственно в основном кармане связывания, где «пришвартовывается» мессенджер, тогда как другие расположены немного глубже в белке, вне прямого контакта с молекулой. Затем команда систематически мутировала эти позиции, протестировав более ста вариантов рецепторов по реакции на дофамин, адреналин и норадреналин с помощью клеточных чтений силы сигнала.
Настройка карманов и глубокие рукоятки управления
Изменение только остатков, соприкасающихся с мессенджером, действительно меняло селективность, но часто ценой существенной потери функции: рецепторы становились слабыми или почти неактивными, даже если начинали отдавать предпочтение новому лиганду. Настоящий прорыв произошёл, когда мутации в кармане связывания были объединены с изменениями в двух более глубоких взаимосвязанных областях, которые действуют как внутренние регуляторы. В β2-рецепторе корректировки в интерфейсе трёх спиралей повысили чувствительность и сместили предпочтение в сторону дофаминовой активности без разрушения функции. В D1-рецепторе правки в другом внутреннем интерфейсе перестроили сеть боковых цепей, косвенно меняя форму кармана. При правильных комбинациях исследователи полностью поменяли предпочтения: модифицированный β2-рецептор теперь предпочитал дофамин, а модифицированный D1 — адреналин и норадреналин — при этом оба продолжали давать сильный сигнал.
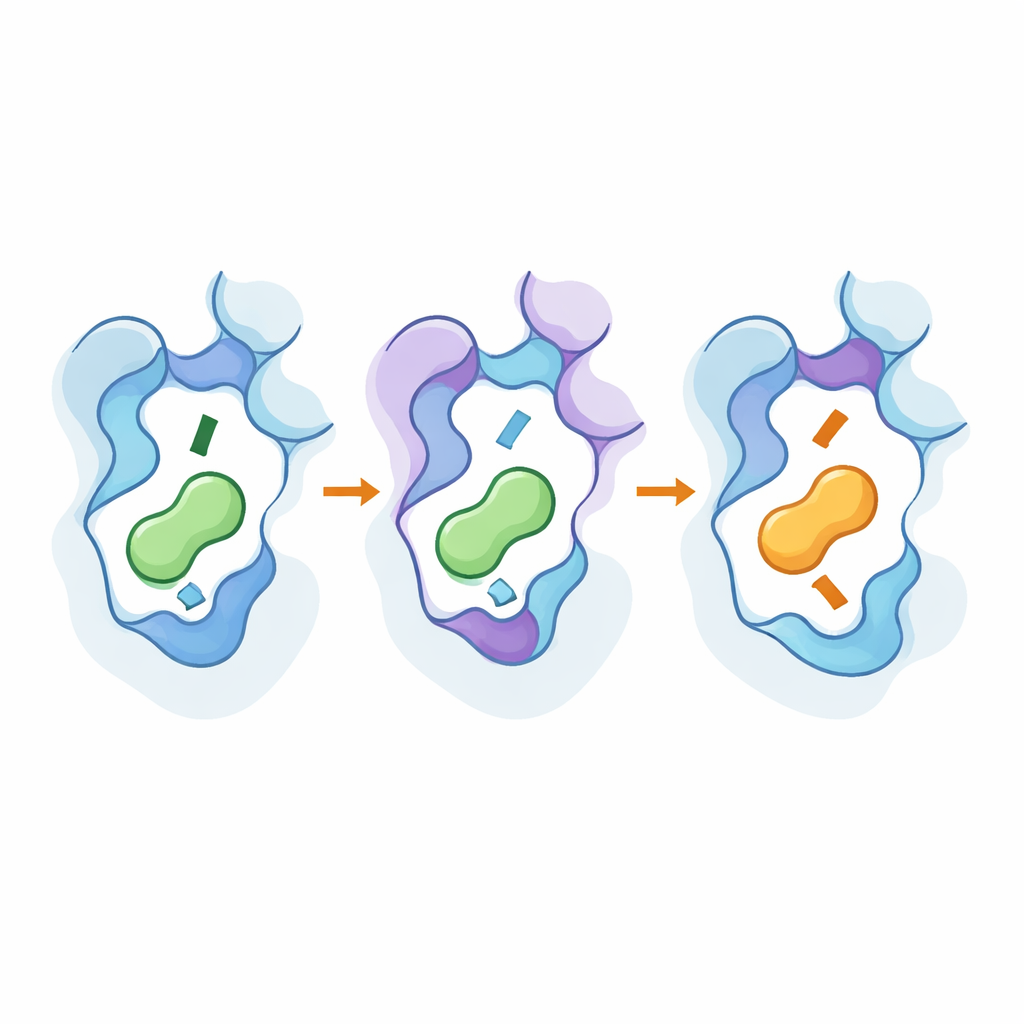
Заглянуть под капот с помощью инструментов высокого разрешения
Чтобы понять, как эти изменения действовали на атомистическом уровне, команда использовала крио-электронную микроскопию для решения трёхмерных структур инженерных рецепторов, связанных с их новыми предпочтительными лигандами, и провела обширные молекулярно-динамические симуляции. Структуры показали, что ключевые мутации едва заметно смещают части седьмой спирали рецептора и консервативный «тумблерный» остаток, углубляя или делая мельче карман и меняя позиционирование аминного конца мессенджера. Удалённые горячие точки помогали стабилизировать активоподобные конформации и усиливали пути передачи сигнала внутрь белка. Симуляции подтвердили, что сети взаимодействующих остатков связывают внешние и внутренние области, и что тот же небольшой набор позиций может повторно использоваться в родственных подтипах рецепторов для переключения селективности без превращения рецепторов в нечётких «всёядных» белков.
Что это значит для медицины и эволюции
Проще говоря, исследование показывает, что горстка грамотно выбранных «атомов» в этих рецепторах действует как винтики настройки, которые решают, будет ли белок в основном слушать дофамин или адреналин. Эти винтики находятся не только на поверхности, где швартуется мессенджер; некоторые зарыты глубже и стабилизируют то, как вся структура сгибается, когда приходит сигнал. Поскольку тот же принцип проектирования повторяется в разных семействах рецепторов, эволюция может многократно перенаправлять похожие белковые каркасы на новые мессенджеры, сначала усиливая отзывчивость внутренними изменениями, а затем доводя форму кармана до нужного состояния. Для поиска лекарств эти наблюдения указывают на точечные места — как в самом кармане, так и вокруг него — которые химики могут целенаправленно использовать, чтобы создать препараты, нацеленные на один подтип рецептора, минуя другие, а также чтобы сконструировать кастомные рецепторы, реагирующие только на заданные сигналы в терапиях и биосенсорах.
Цитирование: Kahlous, N.A., Rinne, M.K., Zhang, X. et al. Molecular mechanisms of native ligand selectivity in catecholamine G protein-coupled receptors. Nat Commun 17, 4112 (2026). https://doi.org/10.1038/s41467-026-71361-8
Ключевые слова: G-белок-связанные рецепторы, дофамин, адреналин, селективность лиганда, дизайн лекарств