Clear Sky Science · pl
Mechanizmy molekularne selektywności rodzimych ligandów w receptorach sprzężonych z białkiem G dla katecholamin
Jak komórki rozróżniają podobne sygnały
Nasz mózg i ciało polegają na małych chemicznych przekaźnikach — takich jak dopamina i adrenalina — które przenoszą instrukcje między komórkami. Te cząsteczki wyglądają zaskakująco podobnie, a mimo to każda musi wywołać właściwą odpowiedź we właściwym miejscu: czy to wzmocnienie uwagi, przyspieszenie pracy serca, czy poprawa nastroju. W tym badaniu pada pozornie proste pytanie: jak niemal identyczne cząsteczki potrafią „wykręcać” różne numery komórkowe, i czy można celowo przeprogramować te numery w celach medycznych i inżynieryjnych?
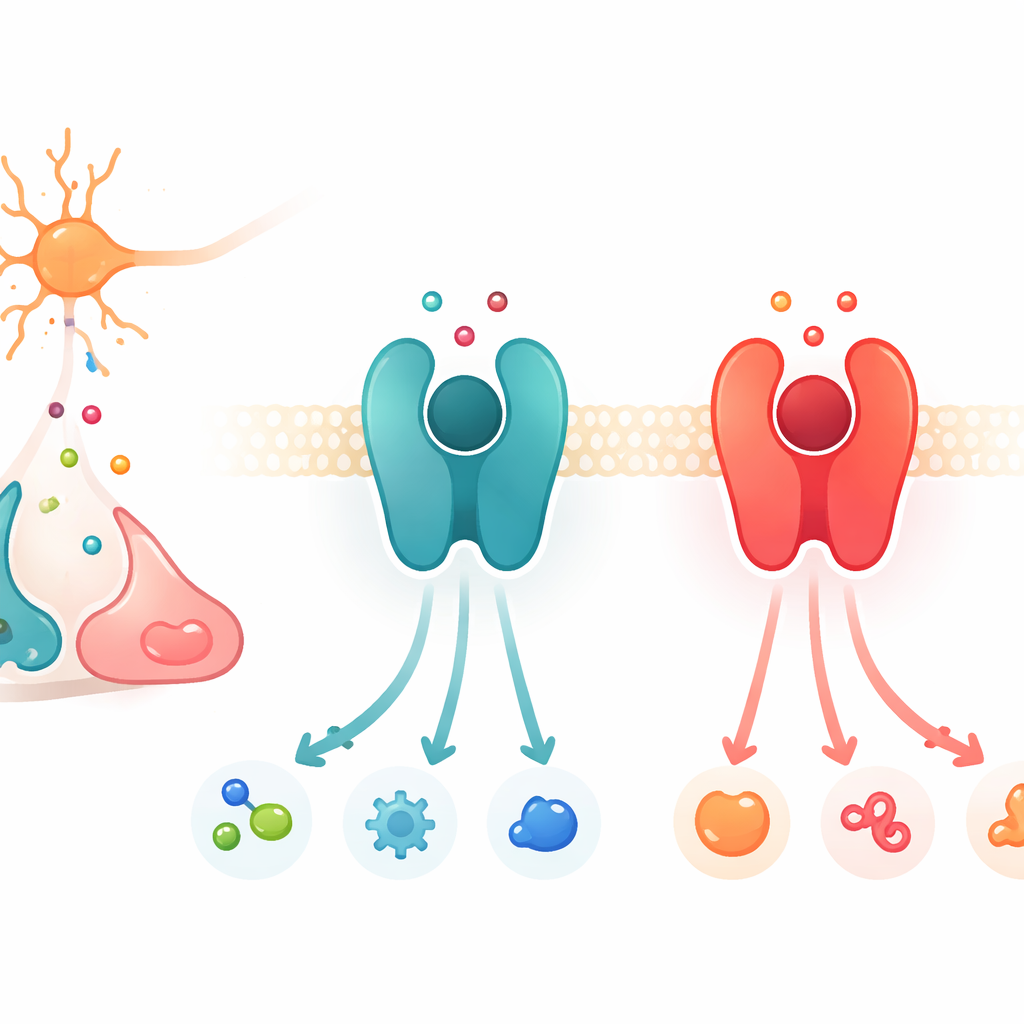
Centralki sygnałów na powierzchni komórek
Praca koncentruje się na dużej rodzinie białek zwanych receptorami sprzężonymi z białkiem G, w skrócie GPCR. Białka te osadzają się w błonie komórkowej i pełnią rolę centralek: gdy przekaźnik chemiczny przyłącza się z zewnątrz, receptor zmienia konformację i aktywuje partnerskie białka wewnątrz komórki, uruchamiając łańcuch sygnałowy. Wśród wielu GPCR znajduje się podgrupa reagująca na katecholaminy — blisko spokrewnione przekaźniki dopamina, adrenalina i noradrenalina. Dwa kluczowe przykłady to receptor β2-adrenergiczny, który preferuje adrenalinę i noradrenalinę, oraz receptor D1 dopaminowy, który faworyzuje dopaminę. Choć te receptory i ich kieszenie wiążące są strukturalnie uderzająco podobne, każdy z nich jest wysoce wybiórczy względem tego, na który przekaźnik silniej reaguje.
Zmiana preferencji za pomocą kilku modyfikacji
Naukowcy połączyli analizy ewolucyjne, biologię strukturalną i pomiary w komórkach, aby wyśledzić „gorące miejsca” determinujące tę chemiczną preferencję. Porównując setki sekwencji receptorów z wielu gatunków i punktując miejsca, gdzie rodziny β2 i D1 konsekwentnie się różnią, wyłonili krótką listę pozycji aminokwasowych, które wyróżniały się najbardziej. Niektóre z tych hotspotów leżą bezpośrednio w głównej kieszeni wiążącej, gdzie przyłącza się przekaźnik, inne znajdują się nieco głębiej w białku, z dala od bezpośredniego kontaktu z cząsteczką. Zespół systematycznie mutował te pozycje, testując ponad sto wariantów receptorów, mierząc ich odpowiedź na dopaminę, adrenalinę i noradrenalinę za pomocą komórkowych odczytów siły sygnalizacji.
Dostrajanie kieszeni i głębokie pokrętła regulacyjne
Zmienianie wyłącznie reszt, które stykają się z przekaźnikiem, faktycznie modyfikowało selektywność, ale często kosztem: receptory stawały się słabe lub prawie nieaktywne, nawet jeśli zaczynały faworyzować nowy ligand. Przełom nastąpił, gdy mutacje w kieszeni wiążącej połączono z modyfikacjami w dwóch głębszych, zazębiających się regionach działających jak wewnętrzne pokrętła regulacyjne. W receptorze β2 korekty w interfejsie trzech helis zwiększyły jego czułość i przesunęły preferencję w kierunku dopaminy bez zniszczenia funkcji. W receptorze D1 zmiany w innym wewnętrznym interfejsie przeorganizowały sieć łańcuchów bocznych, które pośrednio przekształciły kształt kieszeni. Przy odpowiednich kombinacjach badacze w pełni zamienili preferencje: zmodyfikowany receptor β2 preferował teraz dopaminę, podczas gdy zmodyfikowany receptor D1 wolał adrenalinę i noradrenalinę — i oba nadal przekazywały sygnał z dużą siłą.
Zajrzeć pod maskę za pomocą narzędzi wysokiej rozdzielczości
Aby zobaczyć, jak te zmiany działają na poziomie atomowym, zespół użył krio-elektronowej mikroskopii do rozwiązania struktur 3D inżynierowanych receptorów związanych z ich nowymi ulubionymi przekaźnikami i przeprowadził obszerne symulacje dynamiki molekularnej. Struktury pokazały, że kluczowe mutacje subtelnie przesunęły fragmenty siódmej helisy receptora i zachowany „przełącznikowy” reszt, pogłębiając lub spłycając kieszeń i zmieniając ułożenie końca aminowego przekaźnika. Odległe hotspoty pomagały stabilizować konformacje przypominające stan aktywny i wzmacniały ścieżki przenoszące informację o związaniu na wnętrze białka. Symulacje potwierdziły, że sieci oddziałujących reszt łączą te zewnętrzne i wewnętrzne regiony, oraz że ten sam niewielki zestaw pozycji można ponownie wykorzystać w pokrewnych podtypach receptorów, by odwrócić selektywność bez uczynienia receptorów szeroko promiskuitywnymi.
Co to znaczy dla medycyny i ewolucji
Mówiąc prosto, badanie wykazuje, że garść starannie wybranych „atomów” w tych receptorach działa jak śrubki regulacyjne, które decydują, czy białko przede wszystkim „słucha” dopaminy, czy adrenaliny. Te śrubki nie znajdują się tylko na powierzchni, gdzie przyczepia się przekaźnik; niektóre są pogrzebane głębiej i stabilizują, jak cała struktura ugina się, gdy przychodzi sygnał. Ponieważ ta logika projektowa powtarza się w różnych rodzinach receptorów, ewolucja może wielokrotnie przekształcać podobne rusztowania białkowe dla nowych przekaźników, najpierw zwiększając responsywność przez wewnętrzne modyfikacje, a potem dopracowując kieszeń. Dla odkrywania leków wnioski te wskazują precyzyjne miejsca — zarówno w obrębie, jak i wokół miejsca wiązania — które chemicy mogą celować, aby zaprojektować leki trafiające w jeden podtyp receptora przy oszczędzeniu innych, oraz by konstruować niestandardowe receptory reagujące tylko na zaprojektowane sygnały w terapii i biosensorach.
Cytowanie: Kahlous, N.A., Rinne, M.K., Zhang, X. et al. Molecular mechanisms of native ligand selectivity in catecholamine G protein-coupled receptors. Nat Commun 17, 4112 (2026). https://doi.org/10.1038/s41467-026-71361-8
Słowa kluczowe: Receptory sprzężone z białkiem G, dopamina, adrenalina, selektywność liganda, projektowanie leków