Clear Sky Science · pt
Mecanismos moleculares da seletividade de ligantes nativos em receptores acoplados à proteína G para catecolaminas
Como as Células Diferenciam Sinais Semelhantes
Nosso cérebro e corpo dependem de pequenos mensageiros químicos — como dopamina e adrenalina — para transmitir instruções entre células. Essas moléculas se parecem surpreendentemente, mas cada uma precisa desencadear a resposta correta no lugar certo, seja aguçar a atenção, acelerar o coração ou elevar o humor. Este estudo faz uma pergunta aparentemente simples: como moléculas quase idênticas conseguem “discarem” números celulares diferentes, e podemos reprogramar esses números deliberadamente para fins médicos e de bioengenharia?
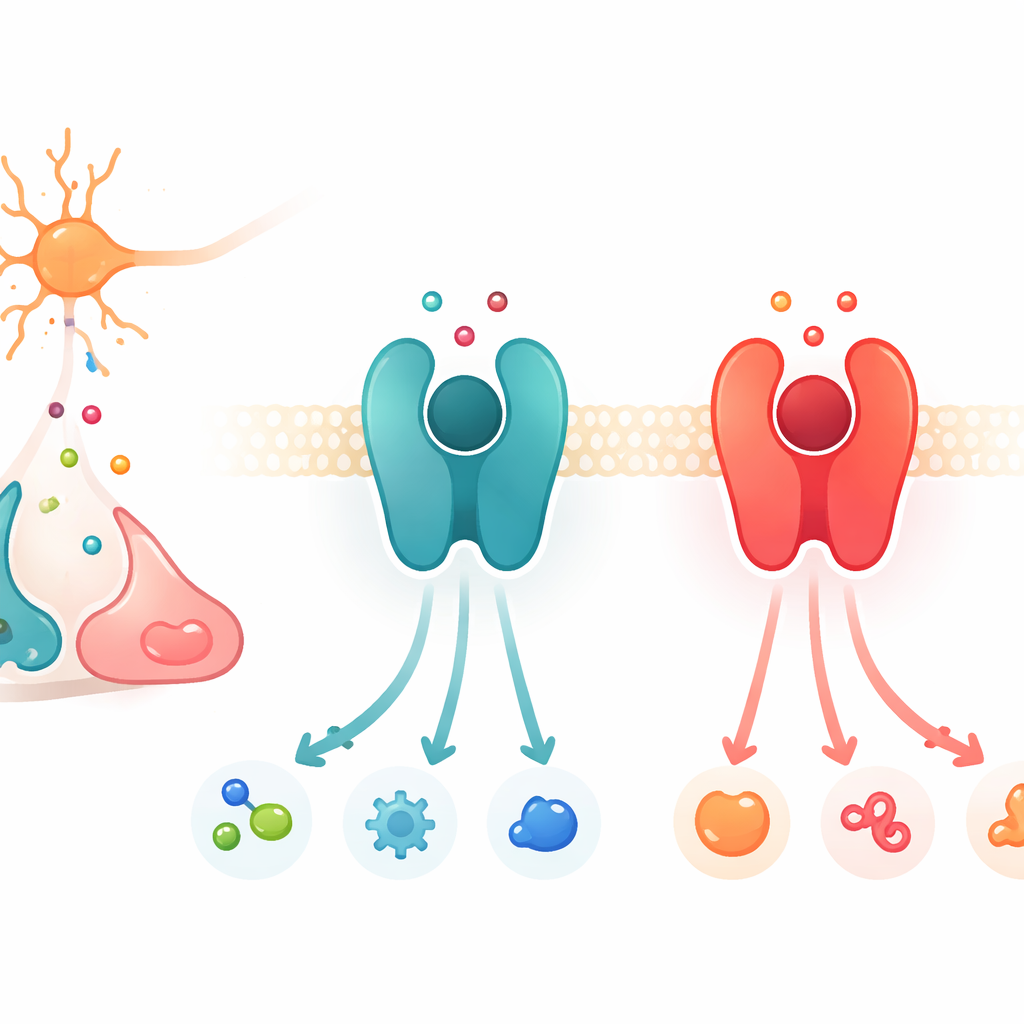
Centrais de Comutação de Sinal na Superfície Celular
O trabalho foca em uma grande família de proteínas chamadas receptores acoplados à proteína G, ou GPCRs. Essas proteínas ficam na membrana celular e funcionam como centrais de comutação: quando um mensageiro químico se liga do lado de fora, o receptor muda de forma e ativa proteínas parceiras no interior, iniciando uma cascata de sinais. Entre os muitos GPCRs, um subconjunto responde às catecolaminas, os mensageiros estreitamente relacionados dopamina, adrenalina e noradrenalina. Dois exemplos principais são o receptor β2-adrenérgico, que prefere adrenalina e noradrenalina, e o receptor D1 de dopamina, que favorece dopamina. Embora esses receptores e seus bolsos de ligação sejam estruturalmente muito semelhantes, cada um é extremamente seletivo quanto ao mensageiro ao qual responde com maior intensidade.
Trocando Preferências com Poucas Mudanças
Os pesquisadores combinaram comparações evolutivas, biologia estrutural e medidas em células para localizar regiões “quentes” que determinam essa preferência química. Ao alinhar centenas de sequências de receptores de muitas espécies e pontuar onde as famílias β2 e D1 diferem de forma consistente, eles encontraram uma lista curta de posições de aminoácidos que se destacavam. Algumas dessas regiões estão diretamente no bolso de ligação principal, onde o mensageiro se ancora, enquanto outras ficam um pouco mais profundas na proteína, longe do contato direto com o químico. A equipe então mutou sistematicamente essas posições, testando mais de cem variantes de receptores para avaliar quão bem respondiam à dopamina, adrenalina e noradrenalina usando leituras celulares da intensidade do sinal.
Ajustando Bolsos e Botões de Controle Internos
Alterar apenas os resíduos que tocam o mensageiro mudou a seletividade, mas frequentemente com um custo alto: os receptores ficavam fracos ou quase não responsivos, mesmo quando começavam a favorecer um novo ligante. O verdadeiro avanço veio quando mutações no bolso de ligação foram combinadas com mutações em duas regiões internas entrelaçadas que funcionam como botões de controle internos. No receptor β2, ajustes em uma interface de três hélices aumentaram sua sensibilidade e o inclinaram para um modo mais favorável à dopamina sem destruir a função. No receptor D1, edições em uma interface interna separada reorganizaram uma rede de cadeias laterais que indiretamente remodelam o bolso. Com as combinações corretas, os pesquisadores inverteram completamente as preferências: um receptor β2 modificado agora preferia dopamina, enquanto um receptor D1 modificado favorecia adrenalina e noradrenalina — ainda assim ambos continuavam a sinalizar de forma robusta.
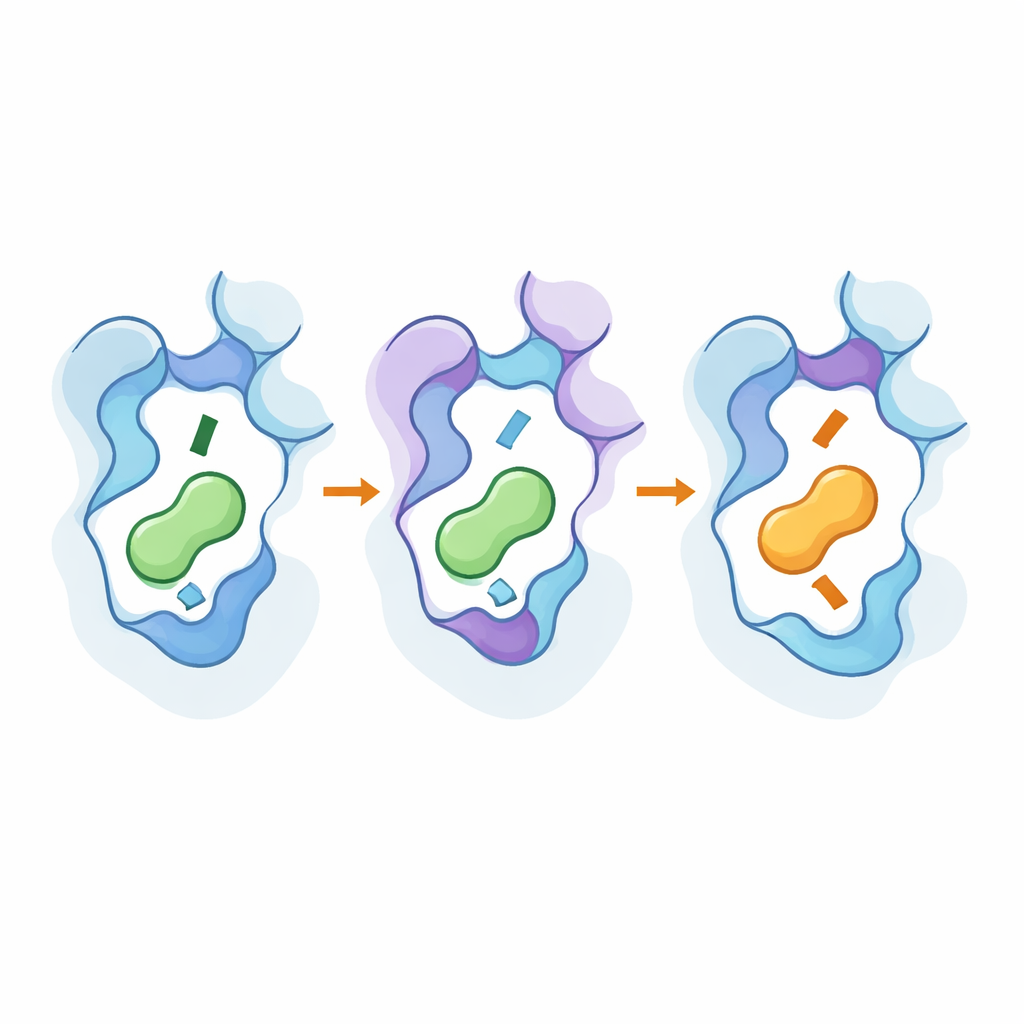
Olhando por Trás do Capô com Ferramentas de Alta Resolução
Para ver como essas mudanças funcionavam em nível atômico, a equipe usou crio-microscopia eletrônica para resolver estruturas 3D dos receptores projetados ligados aos seus novos mensageiros preferidos, e executou extensas simulações de dinâmica molecular. As estruturas mostraram que mutações-chave deslocaram sutilmente partes da sétima hélice do receptor e um resíduo conservado que atua como “chave”, aprofundando ou tornando mais raso o bolso e mudando como a extremidade amina do mensageiro se posiciona. As regiões distantes ajudaram a estabilizar formas semelhantes às ativas e fortaleceram vias que transmitem o evento de ligação para o interior da proteína. As simulações confirmaram que redes de resíduos interagentes ligam essas regiões externas e internas, e que o mesmo pequeno conjunto de posições pode ser reutilizado entre subtipos relacionados de receptores para inverter a seletividade sem tornar os receptores amplamente promíscuos.
O Que Isso Significa para a Medicina e a Evolução
Em termos simples, o estudo mostra que um punhado de “átomos” bem escolhidos nesses receptores age como parafusos de ajuste que decidem se uma proteína atende principalmente à dopamina ou à adrenalina. Esses parafusos não estão todos na superfície onde o mensageiro se ancora; alguns estão enterrados mais profundamente, estabilizando como toda a estrutura se flexiona quando um sinal chega. Como a mesma lógica de projeto reaparece entre famílias de receptores, a evolução pode reaproveitar repetidamente andaimes proteicos semelhantes para novos mensageiros, primeiro aumentando a responsividade por meio de ajustes internos e depois afinando o bolso. Para descoberta de fármacos, esses insights apontam para pontos precisos — tanto dentro quanto ao redor do sítio de ligação — que químicos podem visar para criar medicamentos que atinjam um subtipo de receptor enquanto poupam outros, e para projetar receptores personalizados que respondam apenas a sinais desenhados em terapias e biossensores.
Citação: Kahlous, N.A., Rinne, M.K., Zhang, X. et al. Molecular mechanisms of native ligand selectivity in catecholamine G protein-coupled receptors. Nat Commun 17, 4112 (2026). https://doi.org/10.1038/s41467-026-71361-8
Palavras-chave: Receptores acoplados à proteína G, dopamina, adrenalina, seletividade de ligante, design de fármacos