Clear Sky Science · tr
Katekolamin G protein-eşleşik reseptörlerinde doğal ligant seçiciliğinin moleküler mekanizmaları
Hücreler Benzer Sinyalleri Nasıl Ayırt Ediyor
Beynimiz ve vücudumuz, hücreler arasında talimat taşıyan küçük kimyasal haberci moleküllere—dopamin ve adrenalin gibi—dayanır. Bu moleküller şaşırtıcı derecede benzer görünür, ancak her biri dikkat keskinleştirmek, kalbi hızlandırmak veya ruh halini yükseltmek gibi doğru yanıtı doğru yerde tetiklemelidir. Bu çalışma basit görünen bir soruyu soruyor: neredeyse özdeş moleküller farklı hücresel telefon numaralarını nasıl “çeviriyor”, ve biz bu numaraları tıp ve biyomühendislik için kasıtlı olarak yeniden kablolayabilir miyiz?
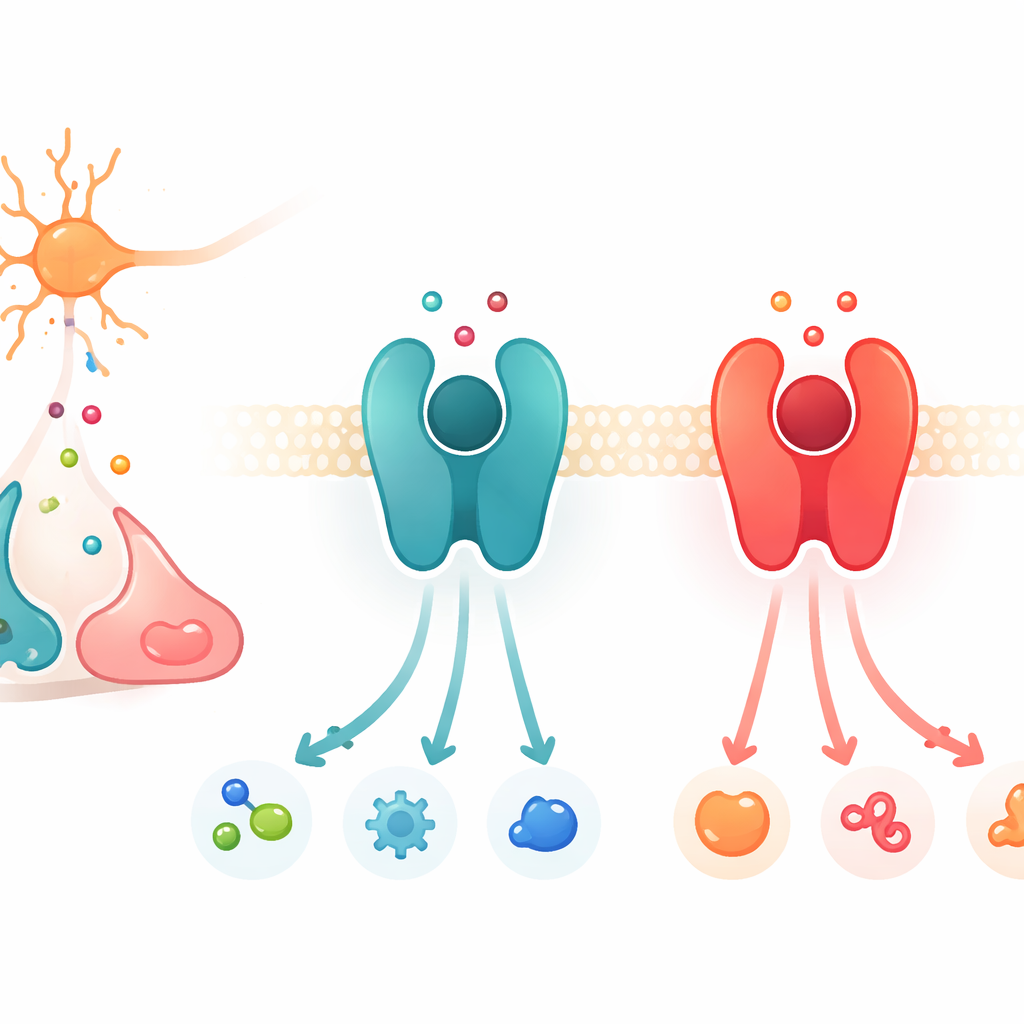
Hücre Yüzeyindeki Sinyal Santralleri
Çalışma, G protein–eşleşik reseptörler veya GPCR olarak adlandırılan büyük bir protein ailesine odaklanıyor. Bu proteinler hücre zarında yer alır ve dışarıda bir kimyasal haberci bağlandığında reseptörün şeklinin değişmesine ve içerdeki partner proteinleri aktifleştirerek bir sinyal zincirini başlatmasına benzer şekilde santraller gibi davranır. Çok sayıda GPCR arasında, dopamin, adrenalin ve noradrenalin gibi birbirine yakın habercilere yanıt veren bir alt grup vardır. İki önemli örnek, adrenalin ve noradrenaline tercih gösteren β2-adrenerjik reseptör ile dopamini tercih eden D1 dopamin reseptörüdür. Bu reseptörler ve bağlanma cepleri yapısal olarak çarpıcı şekilde benzer olmasına rağmen, her biri en güçlü yanıt verdiği haberci konusunda son derece seçicidir.
Sadece Birkaç Değişiklikle Tercihleri Değiştirmek
Araştırmacılar, kimyasal tercihleri belirleyen “sıcak nokta” bölgelerini belirlemek için evrimsel karşılaştırmalar, yapısal biyoloji ve hücre tabanlı ölçümleri birleştirdiler. Birçok türden yüzlerce reseptör dizisini hizalayarak ve β2 ile D1 ailelerinin tutarlı olarak farklılık gösterdiği yerleri puanlayarak öne çıkan birkaç amino asit pozisyonu buldular. Bu sıcak noktalardan bazıları haberci yerleşen ana bağlanma cebinin içinde doğrudan yer alırken, bazıları proteinin biraz daha derininde, kimyasal ile doğrudan temastan uzakta konumlanıyordu. Ekip daha sonra bu pozisyonları sistematik olarak mutasyona uğratarak, sinyal gücünün hücresel ölçümlerini kullanarak dopamin, adrenalin ve noradrenaline karşı nasıl yanıt verdiklerini test etmek üzere yüzün üzerinde reseptör varyantını değerlendirdi.
Cep Ayarı ve Derin Kontrol Düğmeleri
Yalnızca haberciye dokunan kalıntıları değiştirmek seçiciliği değiştirdi, ama sıklıkla yüksek bir maliyetle: reseptörler zayıf ya da neredeyse yanıtsız hale geldi, yeni bir liganta yönelme başlasa bile. Gerçek atılım, bağlanma cebindeki mutasyonların, iç içe geçen iki daha derin bölgedeki mutasyonlarla birleştirildiğinde ortaya çıktı; bu bölgeler iç kontrol düğmeleri gibi davranıyordu. β2 reseptöründe üçlü-heliks arayüzündeki ayarlamalar hassasiyeti artırdı ve işlevi yok etmeden dopamin dostu bir moda doğru itekledi. D1 reseptöründe ayrı bir iç arayüzde yapılan düzenlemeler ise cebin dolaylı olarak yeniden şekillenmesine yol açan bir yan zinciri ağını yeniden organize etti. Doğru kombinasyonlarla araştırmacılar tercihleri tamamen değiştirdiler: modifiye edilmiş bir β2 reseptörü artık dopamini tercih ederken, değiştirilmiş bir D1 reseptörü adrenalin ve noradrenalini tercih etti—bununla birlikte her ikisi de güçlü şekilde sinyal vermeye devam etti.
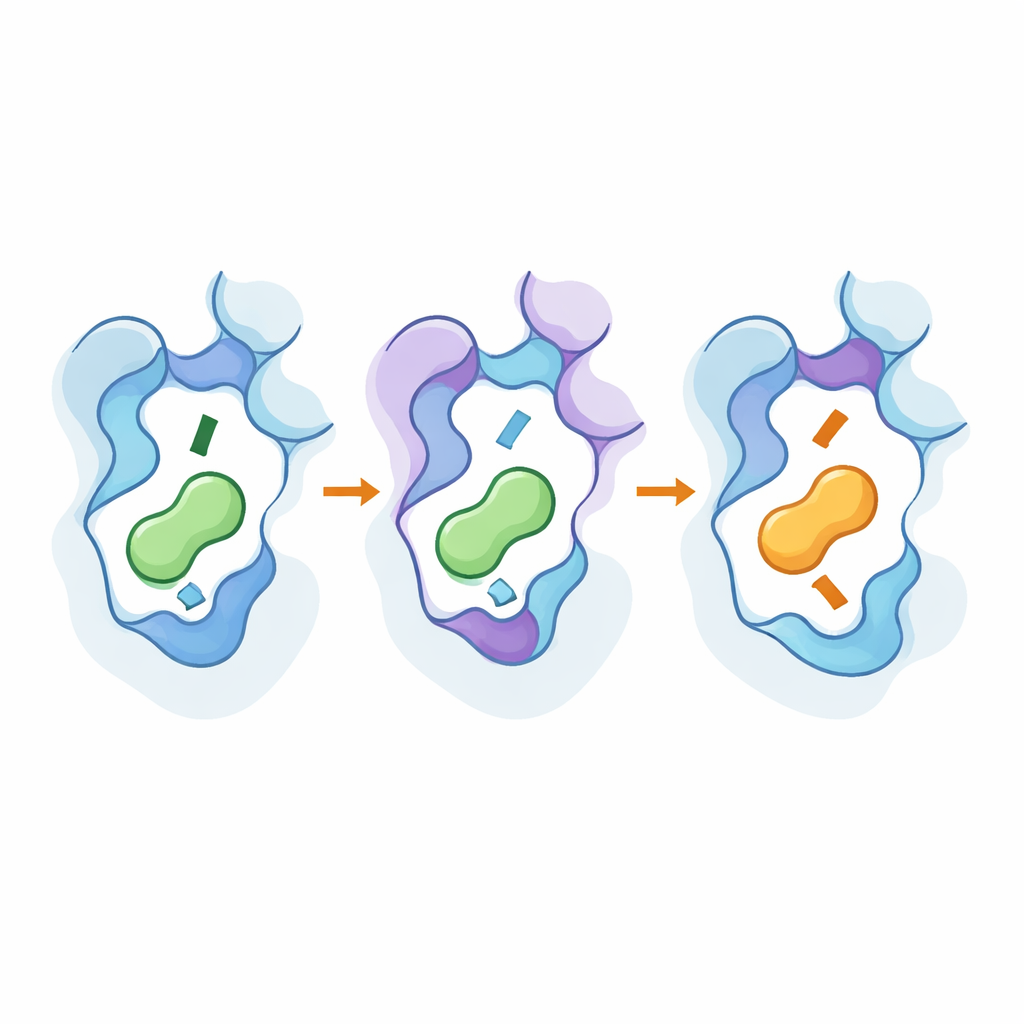
Yüksek Çözünürlüklü Araçlarla Kapağın Altına Bakmak
Bu değişikliklerin atom düzeyinde nasıl işlediğini görmek için ekip, mühendislik yapılmış reseptörlerin yeni tercih ettikleri habercilerle bağlı 3B yapılarını çözmek üzere kriyo-elektron mikroskobu kullandı ve kapsamlı moleküler dinamik simülasyonları yürüttü. Yapılar, anahtar mutasyonların reseptörün yedinci heliksinin bazı kısımlarını ve korunmuş bir “togg le” kalıntısını ince ayarda kaydırdığını; cebi derinleştirdiğini veya sığlaştırdığını ve haberci amin ucunun yerleşimini değiştirdiğini gösterdi. Uzaktaki sıcak noktalar aktif benzeri şekilleri stabilize etmeye yardımcı oldu ve bağlanma olayını proteinin iç kısmına ileten yolları güçlendirdi. Simülasyonlar, etkileşen kalıntı ağlarının bu dış ve iç bölgeleri birbirine bağladığını ve aynı küçük pozisyon setinin, reseptör alt tipleri arasında tercihleri geniş çapta çok eşsiz hale getirmeden tersine çevirmek için yeniden kullanılabileceğini doğruladı.
Bu Bulgunun Tıp ve Evrim İçin Anlamı
Düz bir ifadeyle, çalışma bu reseptörlerde seçimi belirleyen, proteinin esas olarak dopamin mi yoksa adrenalin mi dinleyeceğine karar veren bir avuç iyi seçilmiş “atom”un ayar vidaları gibi davrandığını gösteriyor. Bu vidaların hepsi habercinin yanaştığı yüzeyde değil; bazıları daha derine gömülüdür ve bir sinyal geldiğinde tüm yapının nasıl esneyeceğini stabilize eder. Aynı tasarım mantığı reseptör aileleri arasında tekrarlandığı için, evrim benzer protein iskeletlerini önce içsel ince ayarlarla duyarlılığı artırıp sonra cebi hassaslaştırarak tekrar tekrar yeni habercilere uyarlayabilir. İlaç keşfi açısından, bu bulgular kimyagerlerin bir reseptör alt tipini hedef alırken diğerlerini koruyacak ilaçlar geliştirmek ve terapiler ile biyosensörlerde yalnızca tasarlanmış sinyallere yanıt veren özel reseptörler üretmek için hedefleyebileceği, bağlanma sitesi içinde ve çevresinde hassas noktaları işaret ediyor.
Atıf: Kahlous, N.A., Rinne, M.K., Zhang, X. et al. Molecular mechanisms of native ligand selectivity in catecholamine G protein-coupled receptors. Nat Commun 17, 4112 (2026). https://doi.org/10.1038/s41467-026-71361-8
Anahtar kelimeler: G proteinine bağlı reseptörler, dopamin, adrenalin, ligant seçiciliği, ilaç tasarımı